Устройство экспериментальной установки и методика измерений
Экспериментальная установка (рис. 9.1) состоит из стеклянного баллона 1, соединенного с водяным манометром 2 и ручным насосом (на рис. 9.1 не показан). Посредством крана 3 баллон может соединяться с атмосферой.
 Обозначим атмосферное давление во время опыта
Обозначим атмосферное давление во время опыта 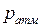 , абсолютную температуру
, абсолютную температуру 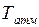 (температура в комнате), объем газа (равен постоянному объему баллона)
(температура в комнате), объем газа (равен постоянному объему баллона) 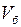 , а его массу
, а его массу 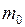 . Назовем это начальным (нулевым) состоянием. При помощи насоса можно в баллон добавлять некоторое количество воздуха, и тем самым повышать его давление.
. Назовем это начальным (нулевым) состоянием. При помощи насоса можно в баллон добавлять некоторое количество воздуха, и тем самым повышать его давление.
Запишем уравнение состояния идеального газа в следующем виде:
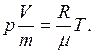
Величина 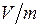 называется удельным объемом. В данном эксперименте объем газа
называется удельным объемом. В данном эксперименте объем газа 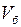 остается неизменным, поэтому накачивание в баллон воздуха (увеличение его массы до значения
остается неизменным, поэтому накачивание в баллон воздуха (увеличение его массы до значения 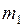 ) приводит к уменьшению удельного объема от
) приводит к уменьшению удельного объема от 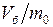 до
до 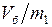 . Несложно показать, что уравнение Пуассона (9.2) справедливо и для удельных объемов, т.е.
. Несложно показать, что уравнение Пуассона (9.2) справедливо и для удельных объемов, т.е.
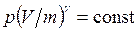 (9.3)
(9.3)
Рассмотрим процессы, которые происходят с газом при выполнении данного эксперимента, и характерные его состояния.
При накачивании воздуха в баллон (первый процесс; рис. 9.2) внешними силами совершается определенная работа. Если процесс накачивания газа проводить быстро, то процессом теплообмена с атмосферой можно пренебречь. Поэтому данный процесс можно считать близким к адиабатическому. Следовательно, за счет работы внешних сил увеличивается внутренняя энергия газа, при этом его температура увеличивается до значения 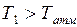 , давление принимает значение
, давление принимает значение 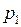 , а масса станет равной
, а масса станет равной 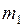 (первое состояние; рис. 9.2).
(первое состояние; рис. 9.2).

После прекращения накачивания неизменная масса 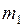 изохорически охлаждается (второй процесс; рис. 9.2) до комнатной температуры
изохорически охлаждается (второй процесс; рис. 9.2) до комнатной температуры 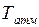 за счет теплообмена с окружающей средой через стенки баллона. В конце этого процесса устанавливается второе состояние, характеризуемое давлением
за счет теплообмена с окружающей средой через стенки баллона. В конце этого процесса устанавливается второе состояние, характеризуемое давлением
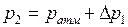 , (9.4)
, (9.4)
температурой 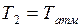 и удельным объемом
и удельным объемом 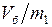 . Под
. Под 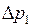 понимается избыточное давление газа в этом состоянии, измеряемое с помощью манометра (второе состояние; рис. 9.2).
понимается избыточное давление газа в этом состоянии, измеряемое с помощью манометра (второе состояние; рис. 9.2).
Теперь если быстро соединить баллон с атмосферой (третий процесс; рис. 9.2), открыв кран, воздух начнет выходить из баллона. После сравнивания давлений в баллоне с атмосферным (равенство уровней в коленях водяного манометра), кран следует закрыть. Этот процесс расширения газа, в силу выше указанных обстоятельств для первого процесса, также можно в первом приближении считать адиабатическим. При этом воздух совершает положительную работу против внешних сил (сил атмосферного давления) что, согласно первому закону термодинамики, приведет при данном процессе к уменьшению его внутренней энергии (адиабатическому понижению температуры). Установившееся третье состояние газа в конце этого процесса (третье состояние; рис. 9.2) характеризуется параметрами: давлением
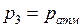 , (9.5)
, (9.5)
температурой 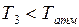 и удельным объемом
и удельным объемом 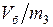 (
( 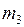 – масса газа, оставшаяся в баллоне).
– масса газа, оставшаяся в баллоне).
После этого в течение некоторого времени происходит нагревание газа (четвертый процесс; рис. 9.2) за счет теплообмена с окружающей атмосферой до ее температуры. Давление при этом несколько увеличивается на величину 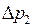 , которое измеряется манометром. Новое, четвертое состояние (рис. 9.2), характеризуется параметрами: давлением
, которое измеряется манометром. Новое, четвертое состояние (рис. 9.2), характеризуется параметрами: давлением 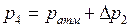 , температурой
, температурой 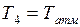 , удельным объемом
, удельным объемом 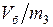 .
.
Из пройденных газом выше описанных процессов и состояний (рис. 9.2) несложно рассчитать коэффициент Пуассона 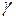 . Запишем уравнение (9.3) для третьего адиабатического процесса охлаждения газа
. Запишем уравнение (9.3) для третьего адиабатического процесса охлаждения газа
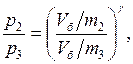
или с учетом (9.4) и (9.5)
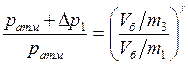 . (9.6)
. (9.6)
Используя уравнение Бойля – Мариотта (изотермический процесс 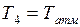 ) для установившихся второго и четвертого состояний, можно записать:
) для установившихся второго и четвертого состояний, можно записать:
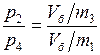 . (9.7)
. (9.7)
Из уравнений (9.6) и (9.7) следует:
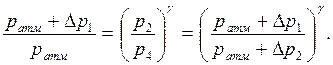
Логарифмируя выражение (9.6) получим
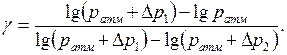
Из-за незначительного отличия давлений 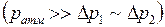 , стоящих под функциями логарифмов, в первом приближении логарифмы величин можно заменить их численными значениями. В таком случае
, стоящих под функциями логарифмов, в первом приближении логарифмы величин можно заменить их численными значениями. В таком случае
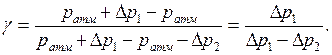
Учитывая, что 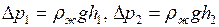
где 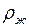 =103 кг/м3 – плотность жидкости в манометре,
=103 кг/м3 – плотность жидкости в манометре,
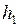 и
и 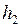 – разность уровней в коленях манометра (рис. 9.1) в состояниях 2 и 4 соответственно.
– разность уровней в коленях манометра (рис. 9.1) в состояниях 2 и 4 соответственно.
Таким образом, выражение для расчета коэффициента Пуассона будет иметь вид
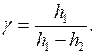 (9.8)
(9.8)
Дата добавления: 2015-02-19; просмотров: 501;
