К изопроцессам
Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых один из основных параметров состояния сохраняется постоянным.
Изохорный процесс (V= const). Диаграмма этого процесса (нзохора) в координатах р,К изображается прямой, параллельной оси ординат (рис. 81), где процесс 1—2есть изохорное нагревание, а 1—3— изохорное охлаждение. При изохорном процессе газ не совершает работы над внешними телами, т. е.
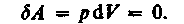
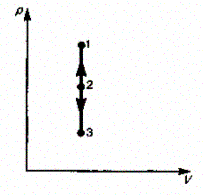
Рис. 81
Как уже указывалось в § 53, из первого начала термодинамики (dQ = dU + dA) дляизохорного процесса следует, что вся теплота, сообщаемая газу, идет на увеличение его внутренней энергии:

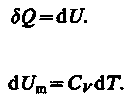
Тогда для произвольной массы газа получим
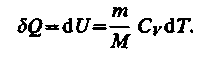 (54.1)
(54.1)
Изобарный процесс (р—const). Диаграмма этого процесса (изобара) в координатах р, Vизображается прямой, параллельной оси V. При изобарном процессе работа газа (см. (52.2)) при увеличении объема от V1 до V2равна
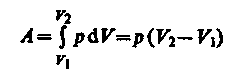 (54.2)
(54.2)
и определяется площадью заштрихованного прямоугольника (рис. 82).
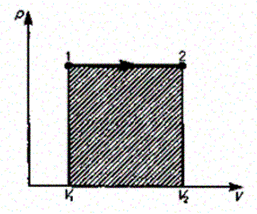
Рис. 82
Если использовать уравнение (42.5) Клапейрона — Менделеева для выбранных нами двух состояний, то

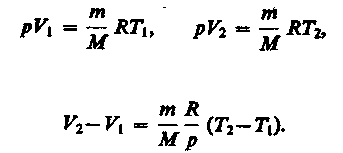
Тогда выражение (54.2) для работы изобарного расширения примет вид (54.3)
Из этого выражения вытекает физический смысл молярной газовой постоянной R:если (Т2 – Т1 = l К, то для 1 моль газа R=A, т. е. R численно равна работе изобарного расширения 1 моль идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой m количества теплоты
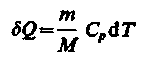
его внутренняя энергия возрастает на величину (согласно формуле (53.4))
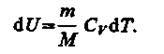
При этом газ совершит работу, определяемую выражением (54.3). Изотермически* процесс (Г= const). Как уже указывалось § 41, изотермический процесс описывается законом Бойля—Мариотта:
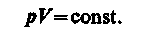
Диаграмма этого процесса (изотерма) в координатах р, Vпредставляет собой гиперболу (см. рис. 60), расположенную на диаграмме тем выше, чем выше температура, при которой происходит процесс.
Исходя из выражений (52.2) и (42.S) найдем работу изотермического расширения газа:
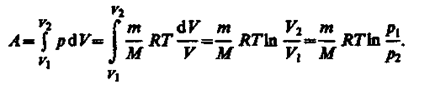
Так как при Т = const внутренняя энергия идеального газа не изменяется:
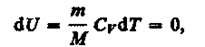
то из первого начала термодинамики (dQ = dU + dA) следует, что для изотермического процесса
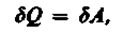
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
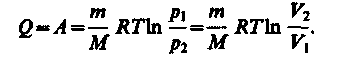 (54.4)
(54.4)
Следовательно, для того чтобы при расширении газа температура не понижалась, к газу в течение изотермического процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.

Дата добавления: 2015-02-13; просмотров: 701;
