Количественное определение витамина С

Количественное определение аскорбиновой кислоты в исследуемом материале часто осуществляют с помощью раствора 2,6-дихлофенолиндофенола натрия, который в щелочной среде имеет синюю окраску, в кислой – розовую. Химизм реакции можно выразить в виде следующего уравнения.
Принцип метода основан на способности аскорбиновой кислоты восстанавливать индофеноловый реактив. При титровании вытяжки исследуемого материала раствором 2,6-дихлорфенолиндофенола происходит окисление аскорбиновой кислоты в дегидроаскорбиновую и восстановление индофенолового реактива. Конец титрования можно установить по изменению окраски. Окисленная форма 2,6-дихлорфенолиндофенола имеет синюю окраску в нейтральной и щелочной среде, восстановленная форма – приобретает розовую окраску в кислой среде.
Аскорбиновую кислоту извлекают из исследуемого материала 1 % раствором соляной кислоты и титруют раствором индофенолового реактива. По количеству краски, затраченной на титрование, рассчитывают содержание аскорбиновой кислоты.
Следует заметить, что точному определению содержания аскорбиновой кислоты в биологических объектах мешают другие, легко окисляемые вещества: глютатион, цистеин и т.п.
7.7.1. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ВИТАМИНА С В
РАСТИТЕЛЬНОМ МАТЕРИАЛЕ
Берут навеску исследуемого материала 5-20 г (в зависимости от предполагаемого содержания аскорбиновой кислоты), нарезают мелкими кусочками (картофель, морковь, черемша, яблоки и т.п.) тщательно растирают в ступке со щепоткой стекла или кварцевого песка, добавляя порциями по 4-5 мл раствора с массовой долей метафосфорной или соляной кислоты 2 % до получения однородной жидкой кашицы. Смесь из ступки количественно, с помощью раствора используемой при растирании кислоты, переносят в мерную колбу вместимостью 100 мл и общий объем экстракта доводят до метки тем же раствором кислоты. Содержимое хорошо перемешивают, настаивают 5-7 мин и фильтруют через бумажный фильтр. Полученный фильтрат должен быть совершенно прозрачным.
Используемые для экстракции кислоты (соляная, метафосфорная, щавелевая) извлекают из исследуемого материала как свободную, так и связанную аскорбиновую кислоту, а также способствуют устойчивости аскорбиновой кислоты в экстрактах.
Берут две конические колбочки вместимостью 100-150 мл и в одну пипеткой вносят 20 мл полученного фильтрата, в другую – 20 мл раствора кислоты, используемой для растирания исследуемого материала. Содержимое колбочек титруют индофеноловым реактивом до слабо-розового цвета, удерживающегося 30 секунд. Результаты записывают, и титрование повторяют с новыми порциями того же фильтрата. На основании средней величины, полученной из 2-3 определений, рассчитывают содержание аскорбиновой кислоты по формуле:
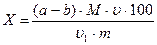 ,
,
где Х – содержание аскорбиновой кислоты в материале, мг/100г продукта;
(a-b) – разность между объемами индофенолового реактива, пошедшими на титрование опытной (а) и контрольной (b) проб, мл;
М – масса аскорбиновой кислоты, соответствующая 1 мл индофенолового реактива (см. пункт 7.7.2.), мг;
u - общий объем экстракта, мл;
u1 – объем фильтрата, взятого для титрования, мл;
m – масса исследуемого материала, г,
100 – пересчет на 100г материала.
В растительных тканях в некоторых количествах содержатся и другие редуцирующие вещества, восстанавливающие 2,6-дихлорфенолиндофенол, поэтому при необходимости проведения особо точного анализа следует принять это в расчет. Для этого к двум другим порциям по 10-20 мл исследуемой вытяжки прибавляют по 0,1 или 0,2 мл 10 % раствора сернокислой меди и нагревают в термостате или сушильном шкафу 10 мин при температуре 110 ˚С. Охлаждают и титруют индофеноловым реактивом. В присутствии солей меди и при нагревании аскорбиновая кислота разрушается полностью. Полученную поправку вычитают из данных титрования опытных проб.
При анализе многих плодов и ягод, некоторых овощей получают окрашенные экстракты, что затрудняет определение аскорбиновой кислоты. Для определения аскорбиновой кислоты, окрашенную вытяжку переносят в широкую пробирку, приливают 2-5 мл дихлорэтана или хлороформа и титруют при взбалтывании раствором индофенолового реактива до появлении в слое дихлорэтана или хлороформа розового окрашивания, не исчезающего 30 сек.
При определении необходимо учитывать редуцирующую способность применяемых для экстракции кислот (смесь 20 мл 1 % соляной кислоты и 80 мл 2 % метафосфорной или 1 % щавелевой кислоты). Для этого две порции смеси кислот по 10 мл титруют индофеноловым реактивом до розового окрашивания. Полученную поправку (обычно не превышающую 0,08-0,10 мл раствора краски) вычитают из данных титрования опытных растворов.
|
2,6-ДИХЛОРФЕНОЛИНДОФЕНОЛА НАТРИЯ (ПО АСКОРБИНОВОЙ КИСЛОТЕ)
|
|
 В две колбочки вносят по 5 мл раствора с массовой долей метафосфорной или соляной кислоты 2 % и по 2 мл стандартного раствора аскорбиновой кислоты (основной опыт). Содержимое каждой колбочки титруют индофеноловым реактивом до слабо-розового окрашивания, сохраняющегося 30 секунд. Параллельно с основным опытом проводят контрольное определение, где также берут две колбочки и в каждую вносят по 7 мл раствора с массовой долей метафосфорной или соляной кислоты 2 % и воду в объеме, равном объему индофенолового реактива, пошедшего на титрование в основном опыте. Содержимое этих колб титруют индофеноловым реактивом до слабо-розового цвета, сохраняющегося 30 секунд.
В две колбочки вносят по 5 мл раствора с массовой долей метафосфорной или соляной кислоты 2 % и по 2 мл стандартного раствора аскорбиновой кислоты (основной опыт). Содержимое каждой колбочки титруют индофеноловым реактивом до слабо-розового окрашивания, сохраняющегося 30 секунд. Параллельно с основным опытом проводят контрольное определение, где также берут две колбочки и в каждую вносят по 7 мл раствора с массовой долей метафосфорной или соляной кислоты 2 % и воду в объеме, равном объему индофенолового реактива, пошедшего на титрование в основном опыте. Содержимое этих колб титруют индофеноловым реактивом до слабо-розового цвета, сохраняющегося 30 секунд.
Мaccy аскорбиновой кислоты (в мг), соответствующую 1 мл индофенолового реактива (раствора 2,6-дихлорфенолиндофенола натрия), рассчитывают пo формуле:
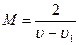 ,
,
где М – масса аскорбиновой кислоты в мг, соответствующая 1 мл индофенолового реактива;
(u-u1) - разность между объемами индофенолового реактива, пошедшими на титрование пробы с аскорбиновой кислотой (u) и пробы без аскорбиновой кислоты (u1), мл;
2 – масса аскорбиновой кислоты в мг, содержащаяся в опытной пробе (основной опыт).
7.7.3. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ВИТАМИНА С В МОЛОКЕ
Для определения аскорбиновой кислоты в молоке предварительно осаждают белки.
В колбочку наливают 50 мл молока и добавляют 4 мл насыщенного раствора щавелевой кислоты, взбалтывают, приливают 10 мл насыщенного раствора хлорида натрия, взбалтывают и оставляют при комнатной температуре на 5 мин. Затем содержимое колбочки фильтруют через бумажный складчатый фильтр, отмеривают пипеткой 20 мл фильтрата и титруют его индофеноловым реактивом до слабо-розового цвета, сохраняющегося 30 секунд. Берут еще 20 мл фильтрата и титрование повторяют. Для расчета берут средний результат.
Параллельно проводят контрольное определение, для чего в колбочке смешивают 50 мл воды, 4 мл насыщенного раствора щавелевой кислоты и 10 мл насыщенного раствора хлорида натрия. Далее поступают как в основном опыте.
Содержание аскорбиновой кислоты (Х мг/100 мл молока) рассчитывают по следующей формуле:
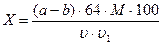 ,
,
где (a-b) – разность между объемами индофенолового реактива, пошедшего на титрование опытной и контрольной проб, мл;
64 – общий объем молока после добавления осадителей белка и жира;
М – масса аскорбиновой кислоты, соответствующая 1 мл индофенолового реактива (см. пункт 7.7.2.), мг;
u - объем фильтрата, взятого для титрования, мл;
u1 - объем молока, взятого для анализа, мл.
РЕАКТИВЫ. Вода дистиллированная; молоко свежее; картофель (лимоны,морковь, яблоки, капуста, черемша и т.п.); раствор с массовой долей метафосфорной или соляной кислоты 2 %; насыщенный раствор щавелевой кислоты; насыщенный раствор хлорида натрия; свежеприготовленный стандартный раствор аскорбиновой кислоты (в мерную колбу вместимостью 100 мл вносят 100 мг аскорбиновой кислоты квалификации «медицинская» и, растворяя, объем доводят до метки раствором с массовой долей метафосфорной или соляной кислоты 2 %; индофеноловый реактив (в мерную колбу вместимостью 500 мл вносят 140-150 мг 2,6-дихлорфенолиндофенола натрия и 200-300 мл воды, энергично встряхивают до растворения краски, объем доводят до метки водой, перемешивают и фильтруют через бумажный фильтр в сухую склянку из темного стекла; раствор хранят в холодильнике не более трех суток).
Дата добавления: 2015-02-13; просмотров: 4769;
