Необходимое условие работы гальванического элемента - разность потенциалов его электродов, она называется электродвижущей силой гальванического элемента- ЭДС.
ЭДС всякого работающего элемента - величина положительная. ЭДС любого биметаллического элемента можно вычислить по разности электродных потенциалов. Для этого надо из величины более положительного потенциала вычесть величину менее положительного. Так, ЭДС медно-цинкового элемента равна разности между потенциалами меди (катода) и цинка (анода), то есть
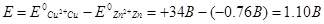
Пример: разобрать работу железо-медного гальванического элемента, если известно, что E°Fe = -0,44В и Е0Сu = 0,337В
Решение: ионы железа имеют в растворе заряд Fe2+, а ионы меди Си2+.
Поэтому железо-медный электрод имеет схему ,
Fe° | Fe2+|| Cu2+| Cu°.
Сравнивая электродные потенциалы, имеем
E°Fe = -0,44В <Е°Cu = +0,337В,
то есть железо - анод, медь - катод.
Тогда
ЭДС=ΔЕ = Е°Cu - E°Fe =+0.337B - (-0,44В) = 0,777 В.
Анодный процесс: Fe° - 2е = Fe2+,
Катодный процесс: Си2+ + е = Си0.
В процессе работы данного гальванического элемента происходит разрушение анода, то есть в данном случае разрушается железный электрод.
ТЕМА 7.3 ПОНЯТИЕ ЭЛЕКТРОЛИЗА
Дата добавления: 2015-02-10; просмотров: 1666;
