А. Кристаллические тела.
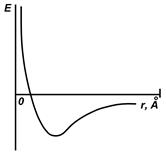
Большинство окружающих нас твердых тел имеет кристаллическую структуру, которая характеризуется трехмерной периодичностью расположения атомов в пространстве. При этом говорят, что такой структуры характерен дальний атомный порядок. Математическим образом кристаллической структуры является пространственная решетка, представляющая собой трехмерную периодическую систему точек. При этом в каждом заданном направлении частицы твердого тела (ионы, атомы, молекулы) располагаются в единственно возможных положениях, отвечающих минимуму энергии (рис. 1).
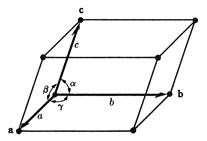
Пространственная решетка может быть описана тремя некомпланарными осевыми трансляциями (переносами) a, b, c и тремя осевыми углами: a, b, g (рис. 2).
| 
|
| Рисунок 1 – Зависимость энергии решетки от расстояния между частицами, находящимися в её узлах. | Рисунок 2 – Элементарная ячейка. |
Трансляция – это вектор, который характеризует минимальное расстояние между идентичными элементами структуры в заданном направлении, т.е при переносе (сдвиге) решетки на трансляцию все её точки попадают в положение, идентичное первичному. Параллелепипед, построенный на трех осевых трансляциях a, b, c учетом осевых углов называется элементарным параллелепипедом или элементарной ячейкой. Выбрав элементарную ячейку, можно, перенося её по соответствующим трем осям, получить весь кристалл, т.е. кристаллическим телам свойственна трансляционная симметрия. (В 80-е годы были открыты квазикристаллы, в которых атомы расположены в пространстве также в определенном порядке, но в квазикристаллах отсутствует трансляционная симметрия).
В зависимости от формы элементарной ячейки все кристаллические тела можно разделит всего на 7 кристаллических систем. Например, большинство очень многие металлы имеют кубическую решетку (рис.3 и 4).

| Рисунок 3. Объемноцентрированная кубическая решетка | Рисунок 4 Гранецентрированная кубическая решетка |
Объемноцентрированную кубическую решетку имеют Мо, W, V, Cr, одна из модификаций Fe (a-Fe) и другие элементы. Гранецентрированная кубическая решетка характерна для Cu, Al, Pd, Au, модификации g-Fe и других металлов. Многим элементам Периодической системы свойствен полиморфизм, т.е. смена кристаллической структуры при изменении внешних условий (температуры, давления). Мы выше уже упомянули о полиморфизме Fe. Данное явление свойственно и «главному» элементу живых систем – углероду. Его кристаллическими модификациями является алмаз (рис.5) и графит (рис.6).
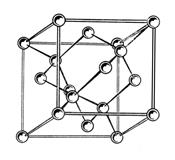 Рисунок 5. Структура алмаза
Рисунок 5. Структура алмаза
|  Рисунок 6. Структура графита
Рисунок 6. Структура графита
|
Конечно, атомная структура определяется особенностями химической связи атомов. Обычно выделяют ионную, ковалентную, металлическую химическую связь, а также связь Ван-дер-Ваальса. Например, металлическая связь характеризуется полным обобществлением части электронов между всеми атомами кристалла. Таким образом, можно считать, что в металле в узлах решетки находятся положительно заряженные ионы и они «погружены» в газ свободных электронов (рис.7). Эти электроны обеспечивают высокую электропроводность и, соответственно, низкое электросопротивление металлов.

Рисунок 7. Металлический кристалл.
Конечно, химические элементы и особенно химические соединения имеют и значительно более сложные атомные структуры. Например, натриевая соль NaCl имеет решетку, показанную на рис. 8, а соединение Nd2Fe14B, из которого в настоящий момент изготавливают постоянные магниты, используемые в компьютерах, мобильных телефонах, автомобилях, имеет ёще более сложную решетку, содержащую 68 атомов в элементарной ячейке (рис.9).
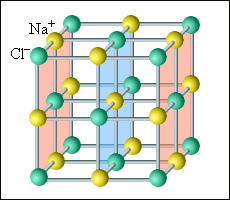
| Рисунок 8. Кристаллическая структура NaCl |
Кристаллические тела могут быть монокристаллами, т.е.состоять лишь из одного кристалла, и поликристаллами. Монокристаллы характеризуются анизотропией свойств. Это объясняется тем, что вдоль разных направлений в кристалле расположение атомов и расстояния между ними различны. Поликристаллические тела состоят из многих сросшихся между собой кристалликов, которые называются кристаллитами или зернами. Большие монокристаллы редко встречаются в природе и технике. Чаще всего кристаллические твердые тела, в том числе и те, которые получаются искусственно, являются поликристаллами.

| Рисунок 9. Структура соединения Nd2Fe14B. Тетрагональная решетка, содержащая 68 атомов в элементарной ячейке. |
В свою очередь, в поликристаллах зерна могут иметь хаотическую ориентацию и тогда говорят, что поликристаллические тела изотропны, т. е. их свойства одинаковы во всех направлениях. Однако зерна поликристалла могут иметь и какую-то преимущественную ориентацию (текстуру) и тогда материал становится анизотропным. Атомную структуру, также как и ориентацию зерен в поликристалле, а также многие другие особенности структуры изучают с помощью дифракционных и микроскопических методов, которые в течение многих лет развиваются на кафедре физического материаловедения НИТУ МИСиС.
Дата добавления: 2015-02-07; просмотров: 2374;
