Олефиновые и ароматические углеводороды
Можно получить молекулу, в которой есть два атома углерода и только четыре атома водорода. На первый взгляд, при этом нарушаются правила валентности, которые Вы изучали предыдущие пять минут. Но химическое соединение этилен С2Н4 построено так, что атомы
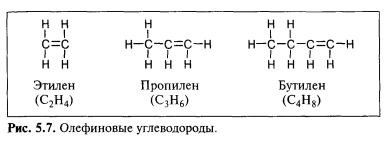
углерода связаны двойной связью, и это компенсирует недостаток водородных атомов (рис. 5.7). двойная связь, удерживающая вместе два атома углерода, не прочнее, чем одинарная связь, а слабее. Можно себе представить, что две связи занимают место, где могла быть одна связь. Поэтому соединение оказывается химически неустойчивым, может довольно легко реагировать с другими веществами и при этом превращаться в новое соединение, в котором уже нет двойной связи. По этой причине этилен очень часто используют для синтеза более сложных химических соединений. Например, если прицепить друг к другу много молекул этилена, получится полиэтилен.
Принципиальная характеристика олефинов — это то, что в них на два атома водорода меньше, чем в соответствующем насыщенном парафине (то есть в парафине,содержащем полный комплект водородных атомов), и,значит, их общая формула СnН2n .
Олефинов в природе не существует. Их нет в сырой нефти — они появляются, потому что их создают люди с помощью процесса крекинга, несколько вариантов которого мы рассмотрим в последующих главах. Другие олефины, представляющие интерес с точки зрения нефтепереработки, это пропилен (С3Н6) и бутилен (С4Н8). Как и этилен, эти соединения можно вводить в реакции с другими веществами, поэтому они пригодны в качестве сырья для ряда химических процессов и процессов нефтепереработки.
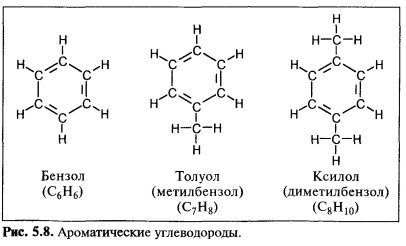
Ароматические углеводороды являются еще одним исключением из правил валентности. Рассмотрим циклическое соединение циклогексан. Каждый атом углерода связан с двумя другими атомами углерода и к нему прицеплено два атома водорода. Если убрать один из водородов от каждого углеродного атома, то правило валентности нарушится и, чтобы оно снова выполнялось, между углеродными атомами можно поместить некоторое количество двойных связей. Для этого требуется, чтобы двойная связь была у каждого второго атома углерода(рис. 5.8). Мы получили молекулу C6H8, бензол. Представление, что каждая вторая связь в бензольном кольце —двойная, является сильно упрощенным. Более реальное представление оперирует понятиями резонансных структур и перескакивающих связей.
Если удалить один из водородов из молекулы бензола,а на его место посадить группу СН3, получится углеводород состава С7Н8 , толуол (группа СН3 называется метильным радикалом, а группа С2Н5 — этильным радикалом. Названия радикалов похожи на названия соответствующих парафинов — метана и этана). Если два водорода в бензольном кольце заменить на два метальных радикала, то получится молекула состава C8H10, ксилол. Двойные связи в бензольном кольце достаточно неустойчивы и химически активны. Поэтому бензол широко используется как строительный блок для получения новых веществ в химической промышленности.
Понятие «ароматика» включает все соединения, в молекулах которых есть бензольное кольцо. Однако на практике этот термин часто используется только по отношению к бензолу, толуолу и ксилолам. Между прочим, название ароматика возникло из-за своеобразного сладковатого углеводородного запаха, присущего большинству этих соединений.
Вы могли заметить, что как только число атомов углерода становится больше шести, число их различных комбинаций в структуре возрастает лавинообразно. Поэтому индивидуальным соединениям уделяется очень мало внимания. Чтобы описать состав нефти или нефтепродукта, иногда указывают процентное содержание парафинов, нафтенов и ароматики; эти группы веществ обычно характеризуются соответствующими физическими свойствами (плотность, вязкость, температура кипения и т.д.).
Дата добавления: 2015-02-07; просмотров: 3678;
