Классификация поликонденсации (гомополиконденсация, гетерополиконденсация, линейная, трехмерная, циклополиконденсация, равновесная и неравновесная поликонденсации).
Процесс поликонденсации, в котором участвуют однородные мономеры, называется гомополиконденсацией. Например, реакция полиамидирования:
n H 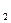 N - R - COOH →H[-HN - R - CO-]
N - R - COOH →H[-HN - R - CO-] 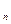 OH + n H
OH + n H 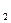 O.
O.
аминокислота полиамид
Процесс поликонденсации, в котором участвуют разнородные мономеры, называется гетерополиконденсацией. Например, реакция полиамидирования:
n H2N-R-NH 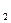 + n HOOC-R`-COOH → H[-HN- R-NH-CO-R`-CO-]
+ n HOOC-R`-COOH → H[-HN- R-NH-CO-R`-CO-] 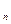 OH + (2n- 1) H2O
OH + (2n- 1) H2O
диамин дикарбоновая кислота полиамид
Реакция поликонденсации бифункциональных соединений, то есть бифункциональных мономеров, приводящая к образованию линейных полимеров, называется линейной поликонденсацией.
Поликонденсация мономеров, содержащих более двух функциональных групп, приводящих к образованию разветвленных или сетчатых полимеров, называется трехмерной поликонденсацией. Например, образование фенолформальдегидных, глифталевых смол. Двухступенчатая реакция, в которой образовавшийся на первой стадии продукт линейной поликонденсации, на второй стадии подвергается внутримолекулярной циклизации, называется циклополиконденсацией.
Поликонденсация в зависимости от значения константы равновесия (Кравн) подразделяется на равновесную (обратимую) и неравновесную (необратимую).
Константа равновесия равна отношению концентрации продуктов реакции к концентрации исходных реагентов.

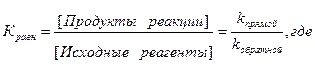 k- константа скорости реакции.
k- константа скорости реакции.
Если Кравн = 1 , то система находится в состоянии равновесия.
К необратимой поликонденсации относится поликонденсация с константой равновесия
Кравн >10 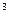 (например, синтез фенолформальдегидных смол сетчатого строения), а к обратимой относится поликонденсация с константой равновесия Кравн <10
(например, синтез фенолформальдегидных смол сетчатого строения), а к обратимой относится поликонденсация с константой равновесия Кравн <10 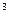 (обычно 0,1 или 10). Например, синтез полиамидов и полиэфиров.
(обычно 0,1 или 10). Например, синтез полиамидов и полиэфиров.
При неравновесной поликонденсации обычно образуются значительно более высокомолекулярные полимеры (с молекулярной массой ≥100000), чем при равновесной поликонденсации (молекулярная масса от 20000 до 70000). Обратимый характер реакции поликонденсации объясняется тем, что может протекать не только прямая реакция образования полимера, но и обратная реакция за счет взаимодействия полимера с выделяющимся низкомолекулярным соединением. Этим объясняется тот факт, что молекулярная масса полимера при поликонденсации растет не до бесконечности, а получается полимер с ограниченной молекулярной массой. Удаляя из сферы реакции выделяющиеся низкомолекулярные соединения, можно сместить равновесие в сторону образования продуктов реакции, и получить полимер с более высокой молекулярной массой.
По характеру функциональных групп, взаимодействующих между собой при поликонденсации, мономеры подразделяются на:
1) Мономеры с однородными функциональными группами.
Например, образование простых эфиров:
n НО- СН2-СН2-ОН → Н-[-О-СН2-СН2-]n-ОН + n Н2О
этиленгликоль полиэфир
1,2- этандиол
2) Мономеры, содержащие в молекуле разнородные функциональные группы.
Например, образование полиамидов:
n НООС- R – NН2 → НО- [-ОС- R- NН-]n-Н + n Н2О
аминокарбоновая кислота полиамид
Получение полигексаметиленадипамида (анида,найлона-6,6):
1. n Н2N-(CH2)6-NH2 + n HOOC-(CH2)4-COOH →
гексаметилендиамин адипиновая кислота
→ H-[-HN-(CH2)6-NH-OC-(CH2)4-CO-]n-OH + (2n-1) H2O
полигексаметиленадипамид (анид, найлон-6,6).
2. n Н2N-(CH2)6-NH2 + n ClOC-(CH2)4-COCl →
гексаметилендиамин дихлорангидрид адипиновой кислоты
→ H-[-HN-(CH2)6-NH-OC-(CH2)4-CO-]n-Cl + (2n-1) HCl
полигексаметиленадипамид (анид, найлон-6,6).
Получение поли-e-капроамида (капрона):
n H 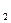 N –(СН2)5 - COOH →H[-HN – (СН2)5 - COO-]
N –(СН2)5 - COOH →H[-HN – (СН2)5 - COO-] 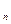 OH + n H
OH + n H 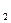 O
O
аминокапроновая кислота поли-e-капрамид (капрон)
Дата добавления: 2015-02-03; просмотров: 2256;
