Количественный и качественный состав микрофлоры кишечника в норме
| Названия микроорганизмов | Дети до 1 года | Дети старшего возраста | Взрослые |
| Бифидобактерии | 1010 – 1011 | 109 – 1010 | 108 – 1010 |
| Лактобактерии | 106 – 107 | 107 – 108 | 106 – 108 |
| Эшерихии | 106 – 107 | 107 – 108 | 106 – 108 |
| Бактероиды | 107 – 108 | 107 – 108 | 107 – 108 |
| Пептострептококки | 103 – 105 | 105 – 106 | 105 – 106 |
| Энтерококки | 105 – 107 | 105 – 108 | 105 – 108 |
| Сапрофитные стафилококки | ≤104 | ≤104 | ≤104 |
| Патогенные стафилококки | - | - | - |
| Клостридии | ≤103 | ≤105 | ≤105 |
| Кандида | ≤103 | ≤104 | ≤104 |
| Патогенные энтеробактерии | - | - | - |
Санитарно-микробиологическое исследование пищевых продуктов (разбор схемы). Бактериологический контроль качества стерилизации и дезинфекции.
1. а) При определении количества бактерий группы кишечных палочек навеску анализируемого продукта (1,0-0,001 г по СанПиН 2.3.2.1078-01), в которой не должно быть БГКП, смешивают с 9 частями жидкой питательной среды (чаще всего используют среду Кесслер, содержащую в своём составе генцианвиолет, угнетающий рост грамположительных бактерий). Из пробирок с забродившей средой (помутнение, наличие газа в поплавках) делают посевы на чашки со средой Эндо. Посевы выдерживают в термостате при температуре 37 °С в течение 18-24 ч. Из колоний, типичных для БГКП (красных, с металлическим блеском, розовых, бледно-розовых), готовят мазки и окрашивают их по Граму.
б) Методы обнаружения сальмонелл. Пробу мяса или мясного продукта дважды пропускают через мясорубку, перемешивают, взвешивают 25 г, затем помещают в стерильную банку смесителя с 225 см3 буферной пептонной водой и гомогенизируют. Далее в асептических условиях переносят содержимое смесительной банки в стерильную колбу вместимостью 500 см3. Колбу выдерживают в термостате при температуре (37±1) °С не менее 16 и не более 20 ч, после чего приступают к анализу.
Выявление сальмонелл проводится в четыре последовательных этапа: первичный (прямой) посев, обогащение, посев со среды обогащения и подтверждение.
Первичный посев производится путем посева взвеси исследуемого материала на плотные элективные среды. Эти среды выдерживают в термостате при температуре 37 °С и исследуют на присутствие колоний, которые являются типичными или подозрительными на сальмонеллы.
На элективных средах сальмонеллы растут, образуя характерные колонии:
- на фуксин-сульфитном агаре (агаре Эндо) сальмонеллы растут в виде круглых, бесцветных или слегка розоватых прозрачных, или полупрозрачных колоний;
- на эозин-метиленовом синем агаре (агаре Левина) сальмонеллы растут в виде прозрачных, бледных, нежно-розовых или розовато-фиолетовых колоний.
Обогащение проводят путем посева на жидкие селективные среды (среды Мюллера, Кауфмана и Киллиана, селенитовый Ф-бульона и хлористо-магниевая среды "М"). Эти среды выдерживают в термостате при температуре 37 °С. На селенитовом бульоне лучшей температурой для накопления сальмонелл является 43 °С.
В случае отсутствия роста бактерий сальмонелл при первичном (прямом) посеве на элективных средах, через 12-24 ч проводят высев на селективные среды со сред обогащения. Предварительно содержимое флаконов перед пересевом тщательно перемешивают и высевают штрихом петлей диаметром 2,5-3 мм на чашку с висмут-сульфитным агаром, бактоагаром Плоскирева или агаром Эндо. Посевы помещают в термостат на 18-24 ч при температуре 37 °С, а посевы на висмут-сульфитном агаре - на 48 ч.
На селективных средах сальмонеллы растут, образуя характерные колонии:
- на бактоагаре Плоскирева сальмонеллы растут в виде бесцветных колоний, но колонии более плотные и несколько меньшего размера, чем на среде Эндо;
- на висмут-сульфитном агаре сальмонеллы растут в виде черных или коричневых колоний с характерным металлическим блеском.
Далее проводят подтверждение - пересев подозрительных на сальмонеллы колоний и определение их биохимических и серологических характеристик. В соответствии с нормативами санитарно-биологических показателей для мяса и мясных продуктов содержание сальмонелл в 25 г исследованного продукта не допустимо.
в) Методы выявления и определения количества Staphylococcus aureus в колбасных изделиях и продуктах из мяса.
Сущность метода заключается в определении морфологии, характера роста на питательных средах и в способности отдельных стафилококков продуцировать лецитиназу и коагулировать цитратную плазму крови кролика под воздействием фермента коагулазы.
Методика проведения анализа заключается в следующем. Из разведения анализируемой взвеси продукта (1:10) проводят посевы на молочно-солевой агар, содержащий 65 г/дм3 хлористого натрия, для выявления пигмента или желточно-солевой агар, содержащий 65 г/дм3 хлористого натрия, для выявления лецитиназной активности. Взвесь наносят на поверхность агара в количестве 0,2 см3 и равномерно растирают по всей поверхности агаровой среды. Посевы термостатируют в течение 24 ч при температуре 37 °С и 24 ч выдерживают при комнатной температуре.
На поверхности питательной среды колонии стафилококка имеют вид плоских или слегка выпуклых блестящих колоний с ровным краем. При этом на молочно-солевом агаре лучше выявляется пигмент (эмалево-белый или золотистый), а на желточно-солевом агаре колонии стафилококков могут образовывать «радужный венчик», что является одним из признаков их патогенности.
Из подозрительных колоний готовят препараты, которые окрашивают по Граму. При наличии стафилококков в препарате обнаруживаются грамположительные мелкие кокки, располагающиеся неправильными гроздьями.
Для подтверждения признаков патогенности стафилококков ставят реакцию плазмокоагуляции. В прибор с 0,5 см3 цитратной плазмы крови кролика, разведенной физиологическим раствором в соотношении 1:4, вносят петлю чистой суточной культуры стафилококка и ставят в термостат при температуре 37 °С. Реакцию плазмокоагуляции учитывают через 3-4 ч (не встряхивая пробирку) и оставляют в термостате на сутки для окончательного учета через 24 ч.
Тест на коагулазу считают положительным, если культура показала, по крайней мере, 3+ - оценку коагулазной реакции, отмеченной на рисунке 1. Реакцию на 1+ или 2+ оценивают как промежуточную.
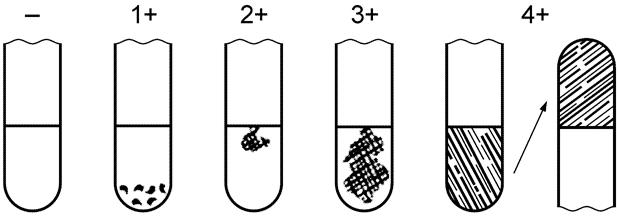
Рис. 1.Результаты коагулазного теста
- отрицательная оценка: не отмечено образования фибрина;
1+ положительная оценка: небольшие несформировавшиеся комочки;
2+ положительная оценка: небольшой сформировавшийся комок;
3+ положительная оценка: большой сформировавшийся комок;
4+ все содержимое пробирки скоагулировано и не меняет своего положения при переворачивании пробирки.
Для определения количества стафилококков учитывают колонии стафилококков, давшие положительную реакцию плазмокоагуляции.
Количество S. aureus в 1 см3 или 1 г продукта определяют исходя из количества коагулазоположительных стафилококков, принадлежность которых к S. aureus подтверждена по образованию ацетоина, определению ферментации в аэробных условиях мальтозы и, при необходимости, определению термостабильной нуклеазы и гемолитической активности. При расчете на 1 г продукта количество подсчитанных колоний умножают на степень разведения и делят на количество посевного материала.
2. Приготовить взвесь в физиологическом растворе кусочка пищевого продукта, зараженного сальмонеллами, и произвести посев взвеси на среду обогащения и на дифференциально-диагностическую среду Плоскирева или Эндо.
3. Приготовить препараты-мазки из культур сальмонелл и кишечной палочки, окрасить по Граму, промикроскопировать и сравнить морфологию бактерий во всех препаратах. Препараты зарисовать.

| 
|
| Salmonella enteritidis | Escherichia coli |
4. Методика посева смывов на общую бактериальную обсемененность.
Общую бактериальную обсемененность определяют для установления эффективности санитарной обработки посуды в посудомоечных машинах, а также при оценке новых моющих и дезинфицирующих средств. Для этого перед посевом в пробирку с тампоном (смыв) добавляют 5 мл 0,1% пептонной воды или изотонического раствора хлорида натрия. Тампон тщательно отмывают, после чего 1,0 мл смывной жидкости помещают в чашку Петри и заливают расплавленным МПА. Чашки помещают в термостат при 30 °C. Предварительный подсчет выросших колоний производят через 48 часов, окончательный - через 72 часа. Количество колоний, выросших на чашке, умножают на 10 для определения общего количества бактерий, содержащихся на поверхности исследуемого предмета.
5. Метод отпечатков на «Бактотест» со средой Эндо при санитарно-бактериологическом контроле на объектах питания.
Данный метод рекомендуется использовать для контроля эффективности санитарной обработки рабочих поверхностей, кухонного инвентаря, посуды, спецодежды и рук обслуживающего персонала.
«Бактотесты» представляют собой круглые ванночки площадью 10 см2 с крышками, выпускаемые стерильными, упакованными по 24 штуки в герметизированные пеналы и предназначенные для разового использования. Перед началом исследования необходимо приготовить среду Эндо в соответствии с наставлением по ее применению, открыть пенал с «Бактотестами», вынуть их из пенала и снять крышки; расположить «Бактотесты» на горизонтальной поверхности; прокипяченную и слегка остуженную среду Эндо разлить по 2 мл в каждую ванночку; после застывания и охлаждения среды Эндо ванночки закрыть крышками и упаковать в пеналы. Подготовленные к работе «Бактотесты» можно хранить при комнатной температуре в течение 4-х суток в сухом и защищенном от света месте.
Взятие отпечатков проводят готовыми (заправленными) «Бактотестами» путем легкого прижатия средой Эндо к обследуемой поверхности. При этом на один «Бактотест» берут 10 отпечатков (обследуемая площадь 100 см2) с поверхности больших предметов: разделочные доски, столы, весы, кастрюли, котлы, разделочные ножи, разливные ложки, тарелки, спецодежда обслуживающего персонала; один «Бактотест» используют для обследования трех мелких предметов: стаканы, чашки, столовые и чайные ложки, вилки, столовые ножи; при обследовании рук обслуживающего персонала на один «Бактотест» делают отпечатки со всех пальцев. Использованные «Бактотесты» маркируют восковым карандашом и упаковывают в пенал, закрыв крышками. После взятия отпечатков проводят инкубацию «Бактотестов» со средой Эндо в термостате при 37 °С в течение 18-24 часов. Выросшие колонии, подозрительные на бактерии группы кишечной палочки по внешнему виду и по морфологии мазков, окрашенных по Граму, высевают на среду Гисса с глюкозой в пробирки с поплавками с последующей инкубацией в термостате при 37 °С в течение 18-24 часов. Заключение о наличии микробов группы кишечной палочки на обследованных объектах делается на основании образования кислоты и газа в пробирках со средой Гисса.
Дата добавления: 2015-03-20; просмотров: 1446;
