ОСНОВНЫЕ ТЕОРИИ ВОСПАЛЕНИЯ
Как патологический процесс, лежащий в основе большинства заболеваний человека, воспаление является центральной проблемой патологии на протяжении всей истории учения о болезни. Формирование представлений о сущности воспаления издавна было тесно связано с развитием взглядов на природу болезни.
В экспериментальном периоде патологии на ранних его этапах доминировали теории воспаления Р. Вирхова (1858) иЮ. Конгейма (1885). Согласно клеточной(аттракционной, нутритив-ной) теории Р. Вирхова воспаление заключается в нарушении жизнедеятельности клеточных элементов в ответ на раздражение, развитии дистрофических изменений, состоящих в появлении в клетках белковых зерен и глыбок, притяжении (аттракции) питательного (нутритивного) материала из жидкой части крови, возникновении вследствие этого мутного набухания цитоплазмы, характерного для воспаления.
По сосудистойтеории Ю. Конгейма воспаление характеризуется расстройствами крово-
Глава 9 / ВОСПАЛЕНИЕ

|
обращения, приводящими к экссудации и эмиграции и обусловливающими последующие клеточные (дистрофические) изменения. Однако, как впоследствии было установлено, воспаление характеризуется одновременным развитием и тесной взаимосвязью сосудистых и тканевых явлений. Ю. Конгеймом впервые детально описана вся совокупность изменений сосудистого тонуса и кровотока с экссудацией и эмиграцией. Особенно большой вклад в изуче-
тельных явлении по мере усложнения воспалительного процесса, позволили И. И. Мечникову показать значение воспаления как защитно-приспособительной реакции всего организма. И. И. Мечников впервые установил связь воспаления с иммунитетом, в механизмах которого фагоцитоз также играет существенную роль.
В первой половине нынешнего столетия учение о воспалении стало развиваться в связи с возникновением
| ние воспаления внес И. И. Мечни- ии „ П845 19161 биофизических и биохимических ме- |
| Лауреат Нобелевской премии 1908 г. |
ков (1892). Он положил начало сравнительной патологии воспаления, теории клеточного и гуморального иммунитета, учению о фагоцитозе и сформулировал биологическую(фагоцитарную) теорию воспаления. Согласно ей основным и центральным звеном воспалительного процесса является поглощение фагоцитами инородных частиц, в том числе бактерий.
Проанализировав воспалительную реакцию у различных видов животных, стоящих на разных ступенях эволюционного развития, И. И. Мечников показал ее усложнение в филогенезе. На ранних этапах филогенеза (у простейших одноклеточных организмов) защита от чужеродного материала осуществляется путем фагоцитоза. При этом и у простейших организмов возникают некоторые явления альтерации. У многоклеточных организмов, не имеющих сосудистой системы, воспаление проявляется скоплением вокруг места повреждения фагоцитирующих амебоидных клеток (амебоцитов). У высших беспозвоночных воспаление выражается скоплением в месте повреждения кровяных клеток -лимфогематоцитов. Несмотря на наличие у них кровеносной системы (открытого типа), сосудистые реакции, характерные для позвоночных, не возникают. Вместе с тем уже на этом этапе эволюционного развития обнаруживаются явления пролиферации. У позвоночных животных и человека воспалительная реакция значительно усложняется за счет сосудистых явлений с экссудацией и эмиграцией, участия нервной системы.
Результаты сравнительно-патологических исследований, свидетельствующие о вовлечении все более сложных новых защитных и приспособи-
тодов. Результаты разносторонних физико-химических исследований воспалительного очага позволили Г. Шаде (1923) выдвинуть физико-химическую,или молекулярно-патологическую, гипотезу воспаления, согласно которой ведущим в патогенезе этого процесса является местное нарушение обмена веществ, приводящее к развитию ацидоза и повышению осмотического давления в ткани, лежащих, в свою очередь, в основе расстройств кровообращения и клеточных явлений при воспалении. Однако вскоре было показано, что физико-химические изменения, характерные для очага воспаления, обнаруживаются в ходе уже развившейся воспалительной реакции и, следовательно, не могут быть пусковым механизмом сосудистых и клеточных явлений [Альперн Д. Е., 1927]. При некоторых видах воспаления (аллергическое) ацидоз не развивается либо выражен слабо [Адо А. Д., 1935].
На основании результатов широких патохи-мических исследований В. Менкин (1938) пришел к выводу о ведущей роли биохимическихсдвигов в патогенезе воспаления. Он предложил ряд специфических для воспаления веществ, опосредующих различные воспалительные феномены, - некрозин, экссудин, лейкотоксин, пи-рексин и др. Как установлено с тех пор, такую роль действительно выполняют физиологически активные вещества - медиаторы воспаления, многие из которых в настоящее время идентифицированы и достаточно изучены. Однако свести весь патогенез воспаления только к разрозненным эффектам отдельных медиаторов было бы неправильным.
С начала нынешнего столетия, когда было установлено участие нервной системы в патоге-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
незе воспаления, возникли гипотезы, отдающие первостепенную роль нервному фактору - рефлекторным механизмам, нарушению трофической функции нервной системы. Так, по вазомоторной (нервно-сосудистой) теории Г. Риккера (1924) первичным в возникновении воспаления является расстройство функции сосудодвигатель-ных нервов. В зависимости от степени их раздражения и, следовательно, развивающейся сосудистой реакции складывается такое соотношение между тканью и кровью, которое ведет к возникновению воспалительной гиперемии и стаза и, соответственно, обусловливает интенсивность и характер нарушений обмена веществ. Однако вся совокупность воспалительных явлений не может быть объяснена только реакцией сосудов микроциркуляторного русла.
Д. Е. Альперн (1959) особое внимание уделял вопросу о единстве местного и общего в воспалении, о роли реактивности организма в развитии этого процесса. Он подчеркивал сущность воспаления как общей реакции организма на действие вредного агента. Им обоснована нервно-рефлекторнаясхема патогенеза воспаления, согласно которой различные сосудисто-тканевые реакции регулируются нервной и гуморальной (главным образом гипофизарно-надпочечнико-вой) системами.
9.2. ЭТИОЛОГИЯ ВОСПАЛЕНИЯ
Причиной воспаления может быть любой фактор, способный вызвать тканевое повреждение. Различают флогогены внешние и внутренние.Чаще встречается воспаление, вызванное экзогенными агентами. В свою очередь, внешние флогогены по своей природе могут быть биологическими (чаще всего инфекционными - бактерии, риккетсии, вирусы, грибки, животные-паразиты), физическими (механическая, термическая, лучевая энергия), химическими (кислоты, щелочи, боевые отравляющие вещества, скипидар, кротоновое и горчичное масла и т. д.). Внутренними причинами воспаления чаще всего являются очаг некроза ткани, гематома, образовавшиеся камни, отложение солей, иммунные комплексы и др. Как правило, легко проследить связь между возникновением эндогенной причины воспаления и действием на организм экзогенных факторов.
Ввиду того, что наиболее частой причиной
Глава 9 / ВОСПАЛЕНИЕ
14 Зак»№ 532
воспаления являются инфекционные агенты, его делят по этиологии на инфекционное(септическое) и неинфекционное(асептическое).
В эксперименте, как правило, используются модели асептического воспаления, вызванного химическими агентами. Традиционными являются раздражающие флогогены, приводящие к развитию острого гнойного воспаления: скипидар, кротоновое масло, ляпис, ксилол, формалин и т. д. Применяются и индифферентные в химическом отношении вещества, например каолин. Для воспроизведения асептического воспаления с преобладанием экссудативных явлений прибегают к декстрану. В последние годы наиболее часто из асептических агентов используется карагинан - сульфатированный гликоза-миногликан, выделенный из ирландского мха Chondrus.
Для того чтобы избежать дальнейшего присутствия флогогена в очаге воспаления, можно избрать модели термического или лучевого (ультрафиолетовые лучи, ионизирующая радиация) воспаления.
Нередко применяется гиперергическое воспаление по типу немедленных или замедленных аллергических реакций. Это воспаление представляет интерес в связи с бурным его течением, частыми явлениями некроза, что обусловлено повышенной реактивностью сенсибилизированного организма.
В патофизиологических исследованиях к моделям инфекционного воспаления прибегают сравнительно редко. Это связано со сложностями моделирования такого воспаления, обусловленными более глубоким взаимодействием микроорганизмов с иммунной системой в процессе его возникновения и течения. В настоящее время из инфекционных возбудителей преимущественно используются кишечная палочка, стафилококки, синегнойная палочка, поскольку именно они являются наиболее частыми причинами гнойно-воспалительных заболеваний и инфекционных осложнений у человека. Близкими к инфекционному воспалению являются такие модели, как, например, каловый перитонит.
Для изучения сосудистых явлений в очаге воспаления наиболее удобным объектом является брыжейка лягушки (опыт Ю. Конгейма), ухо кролика (метод прозрачной камеры - Е.Л. Кларк и Е.Р. Кларк), защечный мешок хомяка, раздуваемый воздухом (Г. Селье); для исследования
клеточной динамики очага воспаления целесообразно использовать метод «кожного окна» (Дж. Рибак) или такие модели, как подкожный «воздушный мешок» (Г. Селье), перитонит, плеврит, когда легко можно собрать экссудат.
9.3. ПАТОГЕНЕЗ ВОСПАЛЕНИЯ
Патогенез воспаления представляет собой сложное сочетание нервных, гуморальных и эф-фекторных механизмов, лежащих в основе большого числа воспалительных феноменов, составляющих, в свою очередь, явления альтерации, расстройств микроциркуляции с экссудацией и эмиграцией и пролиферации (рис. 54).
9.3.1. Роль повреждения ткани в развитии воспаления
Альтерация(alteratio от лат. alterare - изменять), или дистрофия, - повреждение ткани, нарушение в ней питания (трофики) и обмена веществ, ее структуры и функции. Различают первичную и вторичную альтерацию. Первичная альтерация является результатом повреждающего воздействия самого воспалительного агента, поэтому ее выраженность при прочих равных
условиях (реактивность организма, локализация) зависит от свойств флогогена. Строго говоря, первичная альтерация не является компонентом воспаления, так как воспаление есть реакция на повреждение, вызванное флогогеном, т. е. на первичную альтерацию. В то же время практически первичные и вторичные альтеративные явления трудно отделимы друг от друга.
Вторичнаяальтерация является следствием воздействия на соединительную ткань, микрососуды и кровь высвободившихся внеклеточно лизосомальных ферментов и активных метаболитов кислорода. Их источником служат активированные иммигрировавшие и циркулирующие фагоциты, отчасти - резидентные клетки. При воспалении у животных с предварительно вызванной лейкопенией альтерация выражена слабо. Определенную роль в альтерации может играть также литический комплекс С5Ь-С9, образующийся при активации комплемента плазмы и тканевой жидкости.
Таким образом, вторичная альтерация непосредственно не зависит от воспалительного агента, для ее развития нет необходимости в дальнейшем присутствии флогогена в очаге. Она является реакцией организма на уже вызванное вредным началом повреждение. Это неотъемле-
патогенеза воспаления
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
мая часть воспалительного процесса. Более того, это достаточно целесообразный и необходимый компонент воспаления как защитно-приспособительной реакции. Дополнительное встречное повреждение направлено на скорейшее отграничение (локализацию) флогогена и (или) поврежденной под его воздействием ткани от всего организма. Ценой повреждения достигаются и другие важные защитные явления: более выраженный микробицидный и литический эффект лизо-сомальных ферментов и активных метаболитов кислорода, поскольку он осуществляется не только в фагоцитах, но и внеклеточно; вовлечение других медиаторов воспаления и клеток, усиленная экссудация, эмиграция и фагоцитоз. В результате достигается более быстрое завершение воспалительного процесса. Понятно, что альтерация может быть целесообразной лишь в известных пределах. Так, например, при дисбалансе в системе лизосомальные протеиназы - их ингибиторы возникают избыточные проявления альтерации с преобладанием некроза.
Альтеративные явления при воспалении включают тканевой распад и усиленный обмен веществ («пожар обмена»), приводящие к ряду физико-химических изменений в воспалительной ткани - накоплению кислых продуктов (ацидоз, или Н+-гипериония), увеличению осмотического давления (осмотическая гипертензия, или гиперосмия), повышению коллоидно-осмотического, или онкотического, давления (гиперонкия).
В зависимости от силы повреждающего агента, интенсивности и локализации воспаления морфологические проявления альтерации широко варьируют: от едва заметных структурно-функциональных изменений до полной деструкции (некробиоз) и гибели (некроз) тканей и клеток. Наблюдаются мутное набухание цитоплазмы клеток, явления их белковой, жировой и других видов дистрофии. Резко повышается проницаемость мембран клеток и клеточных органелл. Изменения субклеточных структур касаются в первую очередь митохондрий, лизо-сом, рибосом, эндоплазматической сети. Митохондрии набухают или сморщиваются, кристы их разрушаются. Повышение проницаемости и повреждение мембран лизосом сопровождаются выходом разнообразных ферментов, играющих роль в разрушении субклеточных структур. Изменяются форма и величина цистерн эндоплаз-матического ретикулума, в цитоплазме появля-
Глава 9 / ВОСПАЛЕНИЕ
ются везикулы, концентрические структуры и др. Отмечаются краевое расположение хроматина, повреждение мембраны ядра. В строме наблюдаются мукоидное и фибриноидное набухание вплоть до фибриноидного некроза, растворение коллагеновых и эластических волокон.
Повышение обмена веществ при воспалении происходит преимущественно за счет углеводов. Первоначально усиливается как их окисление, так и гликолиз. В основе этого лежит активация соответствующих тканевых ферментов. Заметно увеличивается потребление кислорода воспаленной тканью. По мере накопления в очаге лейкоцитов, лизосомальные ферменты которых расщепляют углеводы преимущественно анаэробным путем, а также повреждения и снижения количества митохондрий в ходе альтерации явления окисления заметно ослабевают, а гликолиза - нарастают. Соответственно расщепление углеводов не всегда доходит до конечных продуктов - углекислого газа и воды. Дыхательный коэффициент снижается. В ткани накапливаются недоокисленные продукты углеводного обмена - молочная и трикарбоновые кислоты.
Кроме того, вследствие нарушения обмена жиров, белков и распада нуклеиновых кислот в очаге нарастает содержание жирных кислот, кетоновых тел, полипептидов, аминокислот, нук-леотидов (АТФ, адениловая кислота), нуклеози-дов (аденозин). В результате развивается ацидоз. Первоначально он компенсируется тканевыми буферными системами и ускоренным крово-и лимфотоком. По мере истощения буферных систем и замедления крово- и лимфотока ацидоз нарастает и становится некомпенсированным. Если в норме концентрация водородных ионов в ткани составляет 0,5 • 10 7 , т. е. рН равен 7,34, то при воспалении может быть соответственно 25 • 10 г и 5,6 и ниже (рис. 55). Чем острее протекает воспалительный процесс, тем более выражен ацидоз. Так, при остром гнойном воспалении рН составляет 6,5-5,39, а при хроническом - 7,1-6,6. Ацидоз имеет некоторое значение в развитии воспалительных феноменов, например в повышении проницаемости сосудов. Он создает благоприятные условия для реализации разрушительных эффектов лизосомальных ферментов, в частности гликозидаз, расщепляющих углеводные компоненты матрикса соединительной ткани.
Наряду с Н*-гиперионией, в очаге нарастает
содержание и других ионов - калия, натрия, кальция. Это обусловлено разрушением клеток и усиленной диссоциацией в кислой среде солей. Вследствие опережающего повышения уровня внеклеточного калия нарушается соотношение ионов калия и кальция (дизиония).Одновременно нарастает молекулярная концентрация, поскольку в процессе тканевого распада и усиленного обмена веществ происходит расщепление крупных молекул до множества мелких. Вследствие повышения ионной и молекулярной концентрации развивается гиперосмия. Так, если в норме депрессия межклеточной жидкости составляет - 0,62°, т. е. осмотическое давление равно 8 атм, то при гнойном воспалении - соответственно - 0,80° и 19 атм.
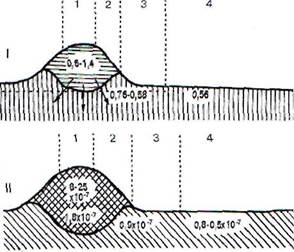
Рис. 55. Схематическое изображение разреза через воспалительный отек кожи: I - изменения осмотического давления (Д*С) в разных зонах очага воспаления: 1 - центр воспаления; 2 - зона полнокровия; 3 - зона явного отека; 4 - зона латентного отека.
II - изменения концентрации ионов водорода: 1 - центр гнойного воспаления; 2 - зона воспалительного инфильтрата; 3 - зона периферического отека; 4 - зона перехода к нормальному состоянию (по Шаде)
В результате физико-химических изменений воспаленной ткани, расщепления белков до полипептидов и аминокислот с увеличением концентрации последних происходит увеличение дисперсности коллоидов, их способности притягивать и задерживать воду. Развивается гипер-онкия. Изменения осмотического и онкотичес-кого давления являются важным фактором экссудации и, соответственно, воспалительного отека.
9.3.2. Медиаторы воспаления
В ходе первичной и вторичной альтерации высвобождаются большие количества разнообразных медиаторови модуляторов воспаления(табл. 34). Под медиаторами (посредниками) воспаления понимают биологически активные вещества, ответственные за возникновение или поддержание тех или иных воспалительных явлений, например повышенной сосудистой проницаемости, эмиграции и т. д. Это те же вещества, которые в условиях нормальной жизнедеятельности организма, образуясь в различных органах и тканях в физиологических концентрациях, ответственны за регуляцию функций на клеточном, тканевом уровне. При воспалении, высвобождаясь (вследствие активации клеток и жидких сред) в больших количествах, они приобретают новое качество - медиаторов воспаления. Практически все медиаторы являются и модуляторами воспаления, т. е. способны усиливать или ослаблять выраженность воспалительных явлений. Это обусловлено комплексностью их влияния и взаимодействием их как с клетками-продуцентами этих веществ, так и между собой. Соответственно эффект медиатора может быть добавочным (аддитивным), потенцирующим (синергистическим) и ослабляющим (антагонистическим), а взаимодействие медиаторов возможно на уровне их синтеза, секреции или эффектов. Медиаторное звено является основным в патогенезе воспаления. Оно координирует взаимодействие множества клеток - эффекторов воспаления, смену клеточных фаз в очаге воспаления. Соответственно патогенез воспаления можно представить как цепь множественных межклеточных взаимодействий, регулируемых медиаторами - модуляторами воспаления.
Все известные медиаторы воспаления по происхождению можно разделить на гуморальные(образующиеся в жидких средах - плазме крови и тканевой жидкости) и клеточные.К первым относятся производные комплемента, кинины и факторы свертывающей системы крови, ко вторым - вазоактивные амины, производные ара-хидоновой кислоты (эйкозаноиды), лизосомаль-ные факторы, цитокины (монокины), лимфоки-ны, активные метаболиты кислорода, нейропеп-тиды. В то время как все гуморальные медиаторы являются предсуществующими, т. е. имеются в виде предшественников до активации последних, среди клеточных медиаторов можно
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
Таблица 34 Медиаторы воспаления
| Происхождение | Основные группы | Основные медиаторы | Основные источники | Основные эффекты |
| 1. Гуморальные' | Производные комплемента | С5Ь-С9 С5а des Arg С5а СЗа | Плазма Тканевая жидкость | Тканевая деструкция (С5Ь-С9) Активация лейкоцитов Повышение проницаемости сосудов (С5а, СЗа) Дегрануляция тучных клеток (С5а, СЗа) Спазм гладкой мускулатуры (СЗа) |
| Кинины | Брадикинин Каллидин | Плазма Тканевая жидкость | Вазодилятация Повышение проницаемости сосудов Спазм гладкой мускулатуры Угнетение гранулоцитов Стимуляция лимфоцитов и фибробластов Боль | |
| Факторы свертывающей системы крови | Фибринопептиды Продукты деградации фибрина | Плазма | Активация лейкоцитов Усиление фагоцитоза | |
| II.Клеточные ТПредсуще-ствующие | Вазоактивные амины | Гистамин | Базофилы Тучные клетки Тромбоциты | Вазодилятация Повышение проницаемости сосудов Спазм гладкой мускулатуры |
| Серотонин | Тромбоциты | Зуд Угнетение гранулоцитов Стимуляция моноцитов-макрофагов и фибробластов | ||
| Лизосомаль-ные факторы | Протеиназы | Гранулоциты Моноциты -макрофаги | Тканевая деструкция Усиление эмиграции и фагоцитоза Стимуляция моноцитов-макрофагов и фибробластов Пролиферация и активация лимфоцитов | |
| Неферментные катионные белки | Гранулоциты | Микробицидность Повышение проницаемости сосудов Дегрануляция тучных клеток Адгезия и эмиграция лейкоцитов | ||
| Нейропептиды | Вещество Р Кальцитонин-генродственный пептид Нейрокинин А | С-волокна афферентных нейронов | Вазодилятация Повышение проницаемости сосудов Дегрануляция тучных клеток Спазм гладкой мускулатуры | |
| Нейромедиато-ры | Ацетилхолин | Холинергичес-кие нейроны | Вазодилятация Спазм гладкой мускулатуры Стимуляция лейкоцитов | |
| 2. Вновь образующиеся | Производные арахидоновой кислоты (эй-козаноиды) | Простагландины | Моноциты -макрофаги Гранулоциты Тромбоциты | Активация лейкоцитов Вазодилятация Боль |
| Тромбоксаны | Моноциты-макрофаги Гранулоциты Тромбоциты | Агрегация тромбоцитов Спазм гладкой мускулатуры Активация гранулоцитов | ||
| Лейкотриены Гидроокси-и гидропероксиэй- козатетраеновые кислоты Липоксины | Моноциты-макрофаги Гранулоциты Тромбоциты | Активация лейкоцитов Повышение проницаемости сосудов (LTC4,D4,E4) Вазодилятация Спазм гладкой мускулатуры (LTC4, D4, E4, липоксины) |
' Все предсуществующие.
Глава 9 / ВОСПАЛЕНИЕ 213
Продолжение табл. 34
| Происхождение | Основные группы | Основные медиаторы | Основные источники | Основные эффекты |
| Фосфолипиды | Фактор, активирующий тромбоциты | Гранулоциты Тучные клетки Моноциты-макрофаги | Спазм гладкой мускулатуры Вазодилятация Повышение проницаемости сосудов Активация лейкоцитов Агрегация тромбоцитов | |
| Монокины | Интерлейкин-1 Фактор некроза опухоли | Моноциты-макрофаги | Активация лейкоцитов и других клеток Пролиферация и активация лимфоцитов Усиление фагоцитоза Стимуляция пролиферации и активации фибробластов Стимуляция тканевой деструкции | |
| Лимфокины | Фактор, активирующий макрофаги Фактор, угнетающий макрофаги Интерлейкин-2 | Т-лимфоциты | Активация и угнетение макрофагов Стимуляция гранулоцитов и лимфоцитов Активация естественных киллеров | |
| Активные формы кислорода | Супероксид-анион Гидроксил-анион Пергидроксил-анион Синглетный кислород Перекись водорода Гипохлорид | Гранулоциты Моноциты-макрофаги | Тканевая деструкция Активация гранулоцитов Стимуляция фагоцитоза Угнетение моноцитов | |
| Другие малые молекулы | Окись азота | Моноциты-макрофаги Гранулоциты | Тканевая деструкция Активация гранулоцитов |
выделить как предсуществующие (депонированные в клетках в неактивном состоянии) - вазо-активные амины, лизосомальные факторы, ней-ропептиды, так и вновь образующиеся (т. е. продуцируемые клетками при стимуляции) - эйко-заноиды, цитокины, лимфокины, активные метаболиты кислорода.

|
| Фракции комплемента |
| Гистамим |
| Секреция протеаз и прочих медиаторов воспаления |
| Нарушение проницаемости капилляров |
|
| Миграция клеток-эффекторов в очаг воспаления |
 Тучные клетки СЗа,С5а
Тучные клетки СЗа,С5а
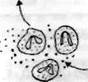
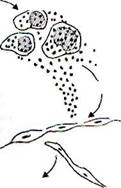
Рис. 56. Связь комплемента с тучными клетками в очаге острого воспаления
Из гуморальных медиаторов воспаления наиболее важными являются производные комплемента. Среди почти 20 различных белков, образующихся при активации комплемента, непосредственное отношение к воспалению имеют его фрагменты С5а, СЗа, СЬ и комплекс С5Ь-С9. При этом С5а и в меньшей степени СЗа являются медиаторами острого воспаления. СЗЬ опсонизи-рует патогенный агент и, соответственно, способствует иммунной адгезии и фагоцитозу. Комплекс С5Ь-С9 ответствен за лизис микроорганизмов и патологически измененных клеток. Источником комплемента служат плазма крови и в меньшей мере тканевая жидкость. Усиленная поставка плазменного комплемента в ткань является одним из важных назначений экссудации. Образующийся из С5а в плазме и тканевой жидкости под влиянием карбоксипептидазы N С5а des Arg и СЗа повышают проницаемость посткапиллярных венул. При этом С5а и СЗа, будучи анафилатоксинами (т. е. либераторами гис-тамина из тучных клеток), повышают проницаемость как прямо, так и опосредованно через гистамин (рис. 56). Эффект С5а des Arg не свя-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
зан с гистамином, но является нейтрофилзави-симым, т.е. осуществляется за счет факторов проницаемости, высвобождаемых из полиморфноя-церных гранулоцитов, - лизосомальных ферментов и неферментных катионных белков, активных метаболитов кислорода. Кроме того, С5а и С5а des Arg привлекают нейтрофилы. В отличие от них СЗа практически не обладает хемотакси-ческими свойствами. Активные компоненты комплемента высвобождают не только гистамин, но и интерлейкин-1, простагландины, лейкот-риены, фактор, активирующий тромбоциты, и синергистически взаимодействуют с простаглан-динами и веществом Р.
Кинины- вазоактивные пептиды, образующиеся из кининогенов (а2-глобулинов) под влиянием калликреинов в плазме (нона-пептид брадикинин) и в тканевой жидкости (декапеп-тид лизилбрадикинин, или каллидин). Пусковым фактором активации калликреин-кинино-вой системы является активация при повреждении ткани фактора Хагемана (XII фактор свертывания крови), превращающего прекалликре-ины в калликреины. Кинины опосредуют расширение артериол и повышение проницаемости венул путем контракции эндотелиальных клеток. Они сокращают гладкую мускулатуру вен и повышают внутрикапиллярное и венозное давление. Кинины угнетают эмиграцию нейтрофи-
лов, модулируют распределение макрофагов, стимулируют миграцию и митогенез Т-лимфоцитов и секрецию лимфокинов. Они также усиливают пролиферацию фибробластов и синтез коллагена и, следовательно, могут иметь значение в ре-паративных явлениях в патогенезе хронического воспаления. Один из наиболее значимых эффектов кининов - активация рефлексов путем раздражения окончаний чувствительных нервов, что обусловливает возникновение воспалительной боли. Кинины вызывают или усиливают высвобождение гистамина из тучных клеток, синтез простагландинов многими типами клеток, поэтому некоторые из их основных эффектов -вазодилятация, сокращение гладкой мускулатуры, боль - связывают с высвобождением других медиаторов, особенно простагландинов.
Активация фактора Хагемана запускает не только процесс кининообразования, но и свертывания крови и фибринолиза. При этом образуются такие медиаторы, как фибринопептиды и продукты деградации фибрина, которые являются мощными хематтрактантами. Кроме того, фибринолиз и образование тромбов в сосудах очага имеют существенное значение как в патологических, так и в защитных явлениях воспаления.
Из клеточных медиаторов первостепенный интерес вызывают эйкозаноиды(рис. 57), по-
Глава 9 / ВОСПАЛЕНИЕ
скольку скорее всего именно они являются центральным медиаторным звеном воспалительной реакции. В пользу этого свидетельствуют продолжительное поддержание продукции эйкоза-ноидов в очаге, их тесная связь с ключевым событием воспалительного процесса - лейкоцитарной инфильтрацией, мощный противовоспалительный эффект ингибиторов их синтеза. Основную роль в продукции эйкозаноидов в очаге воспаления играют лейкоциты, особенно моноциты и макрофаги, хотя они образуются почти всеми типами ядерных клеток при стимуляции последних. Преобладающими эйкозаноидами в очаге воспаления почти всегда оказываются про-стагландин (ПГ) Е2, лейкотриен (ЛТ) В4 и 5-гид-роксиэйкозатетраеновая кислота (5-ГЭТЕ). Образуются также, хотя и в меньшем количестве, тромбоксан (Ткс) А2, nrF2a, IirD2, простацик-лин (ПГ12), ЛТС,, ЛТБ4, ЛТЕ4, другие ТЭТЕ.
Главными эффектами эйкозаноидов при воспалении являются влияния на лейкоциты. ПГ, Ткс и особенно ЛТ как мощные хематтрактанты играют, таким образом, важную роль в механизмах самоподдержания лейкоцитарной инфильтрации. ПГ сами не повышают сосудистую проницаемость, но, будучи сильными вазодилятатора-ми, усиливают гиперемию и, следовательно, экссудацию. ЛТС4, JTTD4, ЛТЕ4 повышают проницаемость сосудов путем прямой контракции эн-дотелиальных клеток, а ЛТВ4 - как нейтрофил-зависимый медиатор. ПГ и ЛТ имеют значение в генезе воспалительной боли. При этом ПГЕ2, не обладая прямой болевой активностью, повышает чувствительность рецепторов афферентных болевых нервных окончаний к брадикинину и гистамину. ПГЕ2 является сильным жароповы-шающим агентом, и лихорадка при воспалении может быть отчасти обусловлена его высвобождением. ПГ играют ключевую роль в модуляции воспалительного процесса, осуществляя двунаправленную регуляцию экссудации, эмиграции и дегрануляции лейкоцитов, фагоцитоза. Так, например, ПГЕ способны потенцировать развитие отека, вызванного гистамином или бради-кинином, а ПГГ2а, напротив, ослаблять. Аналогичные отношения между ПГЕ и ПГР2а распространяются также на эмиграцию лейкоцитов.
Особо широкий спектр взаимодействий с другими медиаторами воспаления характерен для ЛТ. Они синергистически взаимодействуют в отношении бронхоспазма с гистамином, ацетил-
холином, ПГ и Ткс, стимулируют высвобождение ПГ и Ткс. Модуляторная функция эйкозаноидов осуществляется через изменения соотношения циклических нуклеотидов в клетках.
Источниками гистамина являются базофилы и тучные клетки. Серотонин(нейромедиатор) у человека, кроме незначительного количества в тучных клетках, содержится также в тромбоцитах и энтерохромаффинных клетках. Благодаря быстрому высвобождению при дегрануляции тучных клеток, способности изменять просвет микрососудов и вызывать непосредственную контракцию эндотелиальных клеток венул гис-тамин и серотонин считаются основными медиаторами первоначальных микроциркулятор-ных нарушений в очаге острого воспаления и немедленной фазы повышения проницаемости сосудов. Гистамин играет дуалистическую роль как в отношении сосудов, так и клеток. ЧерезН2-рецепторы он расширяет артериолы, а через Hj-рецепторы суживает венулы и, таким образом, повышает внутрикапиллярное давление. Через Н, -рецепторы гистамин стимулирует, а через Нг-рецепторы угнетает эмиграцию и дегрануляции) лейкоцитов. При обычном течении воспаления гистамин действует преимущественно через Н2-рецепторы на нейтрофилах, ограничивая их функциональную активность, и через Н,-рецепторы на моноцитах, стимулируя их. Таким образом, наряду с провоспалительными сосудистыми эффектами, он оказывает противовоспалительное действие. Серотонин также стимулирует моноциты в очаге воспаления. Гистамин осуществляет двунаправленную регуляцию пролиферации, дифференцировки и функциональной активности фибробластов и, следовательно, может иметь значение в репаративных явлениях. Модуляторные эффекты гистамина также опосредуются циклическими нуклеотидами.
Что касается взаимодействий биогенных аминов в очаге воспаления, то известно, что гистамин через Н,-рецепторы может запускать или усиливать синтез простагландинов, а через Н2-рецепторы - угнетать. Взаимодействуя как между собой, так и с брадикинином, нуклеотидами и нуклеозидами, веществом Р, биогенные амины повышают проницаемость сосудов. Сосудорасширяющее действие гистамина усиливается в комплексе с ацетилхолином, серотони-ном, брадикинином.
Основным источником лизосомальных фер-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
ментовв очаге воспаления являются фагоциты - гранулоциты и моноциты-макрофаги. Несмотря на огромную важность фагоцитоза в патогенезе воспаления, фагоциты являются прежде всего подвижными носителями медиаторов - модуляторов, секретируемых внеклеточно. Высвобождение лизосомального содержимого осуществляется в ходе их хемотаксической стимуляции, миграции, фагоцитоза, повреждения, гибели. Главными компонентами лизосом у человека являются нейтральные протеиназы - эластаза, катеп-син G и коллагеназы, содержащиеся в первичных, азурофильных, гранулах нейтрофилов. В процессах противомикробной защиты, в том числе при воспалении, протеиназы относятся к факторам «второй очереди» после кислородзависи-мых (миелопероксидаза - перекись водорода) и таких кислороднезависимых механизмов, как лактоферрин и лизоцим. Они обеспечивают главным образом лизис уже убитых микроорганизмов. Основные же эффекты протеиназ - медиация и модуляция воспалительных явлений, в том числе повреждения собственных тканей. Меди-аторный и модуляторный эффекты протеиназ осуществляются в отношении сосудистой проницаемости, эмиграции, фагоцитоза.
Повышение проницаемости сосудов под влиянием лизосомальных ферментов происходит за счет лизиса субэндотелиального матрикса, истончения и фрагментации эндотелиальных клеток и сопровождается геморрагией и тромбозом. Образуя или расщепляя важнейшие хемотакси-ческие вещества, лизосомальные ферменты являются модуляторами лейкоцитарной инфильтрации. Лизосомальные ферменты, в зависимости от концентрации, могут и сами усиливать или угнетать миграцию нейтрофилов. В отношении фагоцитоза нейтральные протеиназы также обладают рядом эффектов. В частности, эластаза может образовывать опсонин СЗЬ, который является также важным для адгезии частиц к поверхности нейтрофила. Следовательно, нейт-рофил сам обеспечивает себе механизм усиления фагоцитоза. Как катепсин G, так и эластаза повышают сродство Fc-рецептора мембраны нейтрофила к комплексам иммуноглобулинов и, соответственно, усиливают эффективность поглощения частиц.
Благодаря способности лизосомальных ферментов активировать системы комплемента, кал-ликреин-кининовую, свертывания и фибриноли-
Глава 9 / ВОСПАЛЕНИЕ
за, высвобождать цитокины и лимфокины воспаление развертывается и самоподдерживается в течение длительного времени.
Важнейшим свойством неферментных кати-онных белков,содержащихся как в азурофильных, так и в специфических гранулах нейтрофилов, является их высокая микробицидность. В этом отношении они находятся в синергисти-ческом взаимодействии с системой миелопероксидаза - перекись водорода. Катионные белки адсорбируются на отрицательно заряженной мембране бактериальной клетки путем электростатического взаимодействия. В результате этого нарушаются проницаемость и структура оболочки и наступает гибель микроорганизма, что является предпосылкой для последующего эффективного лизиса его лизосомальными протеина-зами. Высвободившиеся катионные белки опосредуют повышение проницаемости сосудов (главным образом путем индукции дегрануляции тучных клеток и высвобождения гистамина), адгезию и эмиграцию лейкоцитов.
Главным источником цитокинов (монокинов)при воспалении являются стимулированные моноциты и макрофаги. Кроме того, эти полипептиды продуцируются нейтрофилами, лимфоцитами, эндотелиальными и другими клетками. Наиболее изученными из цитокинов являются интерлейкин-1 (ИЛ-1) и фактор некроза опухоли (ФНО). Цитокины повышают сосудистую проницаемость (нейтрофилзависимым путем), адгезию и эмиграцию лейкоцитов. Наряду с провоспали-тельными свойствами, цитокины могут иметь значение и в непосредственной защите организма, стимулируя нейтрофилы и моноциты к умерщвлению, поглощению и перевариванию внедрившихся микроорганизмов, а также усиливая фагоцитоз путем опсонизации патогенного агента. Стимулируя раневое очищение, пролиферацию и дифференцировку клеток, цитокины усиливают репаративные процессы. Наряду с этим они могут опосредовать тканевую деструкцию (деградацию хрящевого матрикса и резорбцию кости) и, таким образом, играть роль впатогенезе заболеваний соединительной ткани, вчастности ревматоидного артрита. Действие цитокинов вызывает также ряд метаболических эффектов, лежащих в основе общих проявлений воспаления - лихорадки, сонливости, анорексии, изменения обмена веществ, стимуляции гепато-цитов к усиленному синтезу белков острой фазы,
активации системы крови и т. д. Цитокины взаимодействуют между собой, с простагландияа-ми, нейропептидами и другими медиаторами.
К медиаторам воспаления (цитокинам) относится также ряд лимфокинов - полипептидов, продуцируемых стимулированными лимфоцитами. Наиболее изученными из лимфокинов, модулирующих воспалительный ответ, являются фактор, угнетающий макрофаги, макрофагак-тивирующий фактор, интерлейкин-2. Лимфоки-ны координируют взаимодействие нейтрофилов, макрофагов и лимфоцитов, регулируя таким образом воспалительную реакцию в целом.
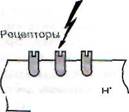
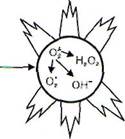
Активные метаболиты кислорода, прежде всего свободные радикалы - супероксидный анион радикал 02', гидроксильный радикал НО', пергидроксил Н02", вследствие наличия на их внешней орбите одного или нескольких непарных электронов обладают повышенной реактивностью с другими молекулами и, следовательно, значительным деструктивным потенциалом, который имеет значение в патогенезе воспаления (рис. 58).
|
|
| Мембрана |
| j Оксидаза | \ / * ®* НАДФ-Н НАДФ НСТ |
| Пентозофосфатный шунт |
| Рис. 58. Индукция активных форм кислорода при активации оксидазной системы клеточной мембраны |
Источником свободных радикалов, а также других кислородпроизводных медиаторов и модуляторов воспаления - перекиси водорода (Н202), синглетного кислорода (02'), гипохлорита (НОС1) - служат: дыхательный взрыв фагоцитов при их стимуляции, каскад арахидоновой кислоты в процессе образования эйкозаноидов, ферментные процессы в эндоплазматическом ретикулуме и пероксизомах, митохондриях, цитозоле, а также самоокисление малых молекул, таких как гидрохиноны, лейкофлавины, катехоламины и ДР-
Роль активных метаболитов кислорода в воспалении состоит, с одной стороны, в повышении бактерицидной способности фагоцитов, а с другой - в их медиаторной и модуляторной функциях. Медиаторная роль активных метаболитов кислорода обусловлена их способностью вызывать перекисное окисление липидов, окисление белков, углеводов, повреждение нуклеиновых кислот. Указанные молекулярные изменения лежат в основе вызываемых активными метаболитами кислорода явлений, характерных для воспаления, - повышения проницаемости сосудов (вследствие повреждения эндотелиальных клеток), стимуляции фагоцитов. Модуляторная роль активных метаболитов кислорода может заключаться в усилении как воспалительных явлений (путем индукции высвобождения ферментов и взаимодействия с ними в повреждении ткани), так и противовоспалительных эффектов (за счет инактивации лизосомальных гидролаз и других медиаторов воспаления). Большое значение имеют активные метаболиты кислорода в поддержании хронического воспаления.
К медиаторам и модуляторам воспаления относят также нейропептиды - вещества, высвобождаемые С-волокнами в результате активации воспалительным агентом полимодальных ноци-цепторов, играющих важную роль в возникновении аксон-рефлексов в конечных разветвлениях первичных афферентных (чувствительных) нейронов. Наиболее изученными являются вещество Р, кальцитонин-генсвязанный пептид, нейрокинин А. Нейропептиды повышают проницаемость сосудов, и эта их способность во многом опосредована медиаторами, происходящими из тучных клеток. Между немиелинными нервами и тучными клетками имеются мембранные контакты, которые обеспечивают сообщение центральной нервной системы с очагом воспаления. Нейропептиды синергистически взаимодействуют в повышении проницаемости сосудов как между собой, так и с гистамином, брадикини-ном, С5а, фактором, активирующим тромбоциты, лейкотриеном В4; антагонистически - с АТФ и аденозином. Они оказывают также потенцирующее воздействие на привлечение и цитоток-сическую функцию нейтрофилов, усиливают адгезию нейтрофилов к эндотелию венул. Кроме того, нейропептиды повышают чувствительность ноцицепторов к действию различных медиаторов, в частности простагландина Б2 и простацик-
Часть II. ТИПОВЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ
лина, участвуя, таким образом, в воссоздании воспалительной боли.
Кроме вышеперечисленных веществ, к медиаторам воспаления относятся также ацетилхо-лин и катехоламины,высвобождающиеся при возбуждении холин- и адренергических структур. Ацетилхолин вызывает расширение сосудов и играет роль в аксон-рефлекторном механизме артериальной гиперемии при воспалении. Норадреналин и адреналин тормозят рост сосудистой проницаемости, выступая главным образом как модуляторы воспаления.
9.3.3. Расстройства кровообращения и микроциркуляции в воспаленной ткани
Расстройства микроциркуляции.Сосудистые явления развиваются вслед за воздействием воспалительного агента, поскольку первоначальные из них являются по своей природе рефлекторными. Они хорошо прослеживаются под микроскопом в классическом опыте Ю. Конгейма на брыжейке лягушки и включают ряд стадий:
1. Кратковременный спазм артериол, сопровождающийся побледнени-ем ткани. Является результатом рефлекторного возбуждения вазоконстрикторов от воздействия воспалительного агента. Длится от нескольких десятков секунд до нескольких минут, так что его не всегда удается отметить.
2. Артериальная гиперемия, обусловленная расширением артериол, механизм которого, с одной стороны, связан с аксон-рефлекторным возбуждением вазодилятаторов, а с другой - с непосредственными сосудорасширяющими эффектами медиаторов воспаления: ней-ропептидов, ацетилхолина, гистамина, брадики-нина, простагландинов и др. Артериальная гиперемия лежит в основе двух основных внешних местных признаков воспаления - покраснения и повышения температуры ткани. Кроме того, в воссоздании жара имеет значение повышенная теплопродукция в очаге из-за усиленного обмена веществ.
3. Венозная гиперемия. Она может
развиться уже через несколько минут после воз
действия воспалительного агента, однако харак
теризуется значительной продолжительностью -
сопровождает весь ход воспалительного процес
са. Одновременно, поскольку при ее участии осу-
ществляются основные воспалительные явления, она считается истинной воспалительной гиперемией.
В механизме венозной гиперемии различают три группы факторов:
а) нарушения реологических свойств крови и
собственно ее циркуляции. Сюда относятся по
вышение вязкости крови вследствие ее сгуще
ния, обусловленного экссудацией, потери альбу
минов, увеличения содержания глобулинов, из
менения коллоидного состояния белков; усиле
ние сопротивления кровотоку в результате кра
евого стояния лейкоцитов, набухания и агрега
ции эритроцитов; тромбообразование вследствие
активации свертывающей системы крови; нару
шение характера кровотока - замедление тока
крови в осевой зоне, уменьшение краевой плаз
матической зоны;
б) изменения сосудистой стенки, которые
включают потерю сосудистого тонуса вследствие
паралича нервно-мышечного аппарата сосудов;
снижение эластичности сосудистой стенки; на
бухание эндотелия и повышение его адгезивнос-
ти, в результате чего просвет сосудов сужается,
создаются условия для прилипания лейкоцитов
к эндотелию;
в) тканевые изменения, состоящие в сдавле-
нии венул и лимфатических сосудов отечной,
инфильтрированной тканью; снижении упруго
сти соединительной ткани.
Следуетзаметить, что многие из вышеперечисленных факторов являются, с одной стороны, непосредственными причинами, а с другой - одновременно следствиями развивающейся венозной гиперемии.
Воспалительная гиперемия отличается от других видов гиперемии (вызываемой, например, механическим фактором) значительным ослаблением или даже извращением реакции сосудов воспаленной ткани на действие сосудосуживающих агентов (адреналин, кофеин) и на раздражение симпатических нервов. Это явление может быть связано с «десенсибилизацией», или тахифилаксией, сосудов, т.е. сниженной или качественно измененной их чувствительностью к действию вазоконстрикторных стимулов, обусловленной блокадой рецепторов. Другие отличия воспалительной гиперемии связаны с более выраженным кровенаполнением воспаленного участка органа или ткани,- расширением и увеличением количества функционирующих капилля-
Глава 9 / ВОСПАЛЕНИЕ
ров, интенсивностью микроциркуляции, отставанием линейной скорости кровотока и др., что позволяет рассматривать воспалительную гиперемию как специальный вид нарушений микроциркуляции (А. Д. Адо, Г. И. Мчедлишвили).
4. С т а з. Он может развиться в некоторых разветвлениях сосудов воспаленной ткани. Распространенный стаз характерен для острого, быстро развивающегося, например гиперергичес-кого, воспаления. Как правило, нарушение кровотока при воспалительном стазе является преходящим, однако при возникновении повреждений сосудистой стенки и тромбов во многих микрососудах стаз становится необратимым.
Дата добавления: 2015-03-19; просмотров: 3206;
