КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ФЕРМЕНТОВ. Современные классификация и номенклатура ферментов разработаны Комиссией по ферментам Международного биохимического союза и утверждены на V Международном
Современные классификация и номенклатура ферментов разработаны Комиссией по ферментам Международного биохимического союза и утверждены на V Международном биохимическом конгрессе в 1961 г. в Москве.
В основу классификации легли 3 принципа:
1. Химическая природа фермента.
2. Химическая природа субстрата, на который действует фермент.
3. Тип катализируемой реакции.
Ферменты делят на шесть классов.
1. Оксидоредуктазы- ферменты, катализирующие реакции окисления—восстановления:
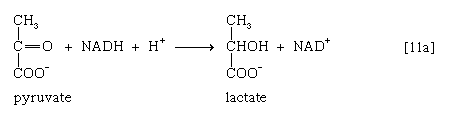
пируват лактат
- аэробные дегидрогеназы, или оксидазы, катализируют перенос протонов (электронов) непосредственно на кислород;
- анаэробные дегидрогеназы ускоряют перенос протонов (электронов) на промежуточный субстрат, но не на кислород.
Наиболее распространены оксидоредуктазы, содержащие в качестве активной группы никотинамидадениндинуклеотид,или НАД+. Кроме НАД+ пиридинферменты содержат в качестве кофермента никотинамидадениндинуклеотидфосфат(НАДФ+). Коферментами оксидоредуктаз являются также флавопротеины (ФП) - флавинмононуклеотид, ФМН, и флавинадениндинуклеотид, ФАД.
2. Трансферазы - ферменты, катализирующие реакции межмолекулярного переноса различных атомов, групп атомов и радикалов.
Фосфотрансферазы-перенос остатка фосфорной кислоты. Фосфорные эфиры органических соединений обладают повышенной химической активностью. Донором фосфатных остатков в большинстве случаев является АТФ.
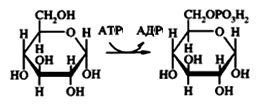
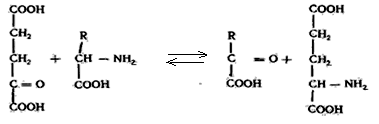
Аминотрансферазыускоряют реакцию переноса аминогруппы от аминокислоты на a-кетокислоту.
Протеинкиназыускоряют перенос остатка фосфата с АТФ на белки,изменяя их биологическую активность.
Гликозилтрансферазыускоряют реакции переноса гликозильных остатков.
Ацилтрансферазыкатализируют перенос ацилов (остатков карбоновых кислот).
3. Гидролазыкатализируют расщепление внутримолекулярных связей органических веществ при участии молекулы воды.
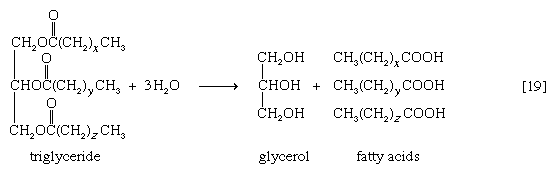
Эстеразыкатализируют гидролиз сложных эфиров спиртов с органическими и неорганическими кислотами. Например, липазаускоряет гидролиз триацилглицеринов (жиров):
Фосфатазыкатализируют гидролиз фосфорных эфиров:
глюкозо-6-фосфат + Н2О®глюкоза + Н3РО4
Гликозидазыкатализируют гидролиз гликозидов. Из гликозидаз, действующих на полисахариды, наиболее известны амилазы.
Пептидгидролазыускоряют гидролиз пептидных связей в белках и пептидах.
4. Лиазы- ферменты, катализирующие разрыв связей С—О, С—С, С—N и других, а также обратимые реакции отщепления различных групп от субстратов негидролитическим путем. Эти реакции сопровождаются образованием двойной связи и выделением таких простейших продуктов, как СО2, H2O, NH3 и т. д..
Углерод-углерод-лиазы – декарбоксилазы:
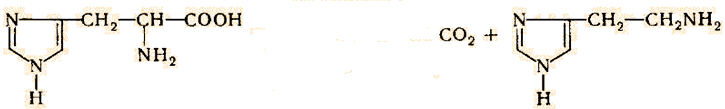
5. Изомеразы- ферменты, катализирующие взаимопревращения структурных, оптических и геометрических изомеров. Мутаротазаускоряет реакцию превращения α-D-глюкопиранозы в β-D-глюкопиранозу:

6. Лигазы (синтетазы) - ферменты, катализирующие синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ либо других веществ.
Одной из важнейших карбоксилаз является пируваткарбоксилаза:
СН3-СО-СООН + СО2 ® НООС-СН2-СО-ООН
Международная комиссия подготовила Классификацию ферментов (КФ).Код каждого фермента содержит четыре цифры, разделенные точками. Первая цифра указывает номер класса, вторая означает подкласс и характеризует вид субстрата. Например, у трансфераз указывает на природу переносимой группы, у гидролаз - на тип гидролизуемой связи. 3 цифра – уточняет природу участвующих в реакции соединений или групп. Четвертая цифра – номер фермента в данном подподклассе.
Пепсин – пептид-пептидогидролаза; КФ 3.4.4.1.
Дата добавления: 2015-03-19; просмотров: 1306;
