Получение альдегидов и кетонов.
1. Окисление спиртов. Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот:
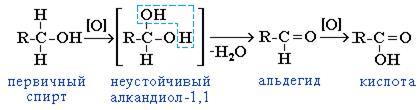
При окислении вторичных спиртов образуются кетоны:
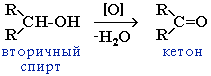
2. Гидратация алкинов (реакция Кучерова). Присоединение воды к ацетилену в присутствии солей ртути (II) приводит к образованию ацетальдегида:
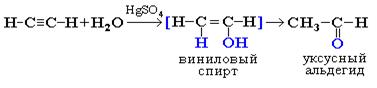
Кетоны получают при гидратации других гомологов ацетилена:
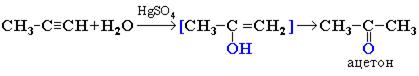
3. Окисление алкенов (катализаторы - хлориды Pd и Cu):
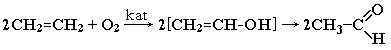
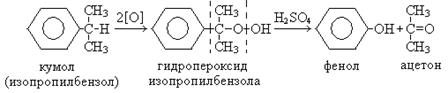
4. Кумольный способ получения ацетона и фенола (Кружалов, Сергеев, Немцов):
5. Реакция оксосинтеза:
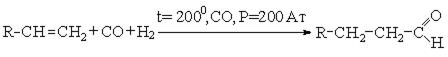
6. Восстановление хлорангидридов карбоновых кислот:
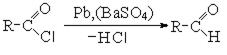
7. Карбонильные соединения являются промежуточными продуктами окисления углеводородов до кислот.
Химические свойства альдегидов и кетонов.Электронная структура карбонильной группы определяет реакционную способность альдегидов и кетонов. Атом углерода карбонильной группы находится в состоянии sp2-гибридизации. Валентный угол между δ- связями 1200. Неспаренный р- электрон углерода перекрывается с р- электроном кислорода и образует π- связь, которая располагается перпендикулярно плоскости молекулы альдегида. Электронная плотность π- связи смещена к кислороду. Исходя из этого, типичными реакциями альдегидов и кетонов являются:
─ реакции нуклеофильного замещения (AdN);
─ реакции окисления;
─ реакции с участием атомов водорода в α- положении в карбонильной группе.
Реакции нуклеофильного присоединения.Реакции нуклеофильного присоединения протекают через стадию образования промежуточного комплекса, который характеризуется изменением типа гибридизации исходного альдегида. Молекула принимает тип гибридизации, который будет в конечных продуктах реакции. Механизм реакции имеет вид:
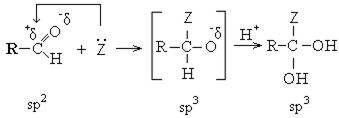
1. Взаимодействие с синильной кислотой:
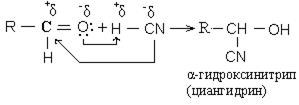
Кетоны в реакции AdN вступают труднее, чем альдегиды. Это связано с пространственными препятствиями алкильных радикалов кетонов при образовании промежуточной структуры.
2. Присоединение гидросульфита натрия:
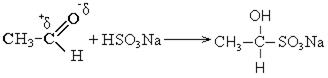
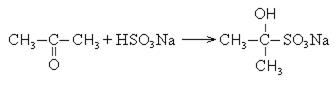
С гидросульфитом натрия вступают во взаимодействие только метилкетоны.
Реакции карбонильных соединений с гидросульфитом натрия используются для очистки продуктов от карбонильных соединений.
3. Взаимодействие с аммиаком:
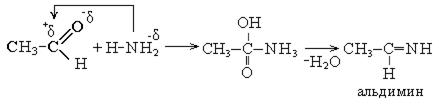
Взаимодействие кетонов с аммиаком происходит иначе:
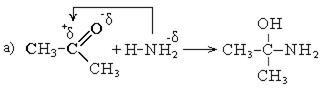
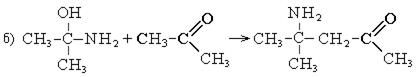
4. Взаимодействие с гидроксиламином. При взаимодействии карбонильных соединений с гидроксиламином образуются оксимы:
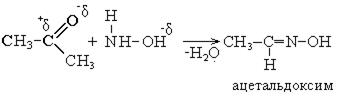
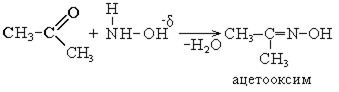
Эта реакция используется для количественного определения карбонильных соединений в реакционных смесях, различных продуктах. При этом используется солянокислый гидроксиламин (NH2-OH•HCl).
5. Взаимодействие альдегидов с гидразином:
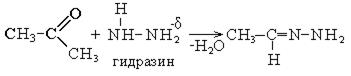
Аналогично взаимодействуют кетоны.
6. Взаимодействие с фенилгидрозином:
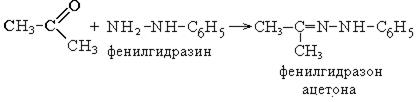
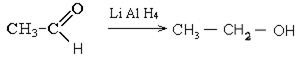
7. Реакции гидрирования. При восстановлении альдегидов образуются первичные спирты. При восстановлении кетонов образуются вторичные спирты. При восстановлении кетонов водородом в момент выделения возможно образование пинаконов.
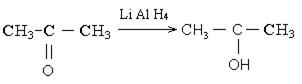
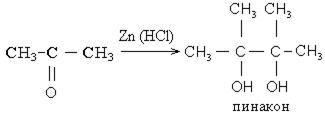
8. Взаимодействие альдегидов со спиртами:
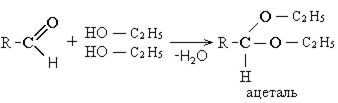
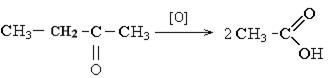
Реакции окисления. Окисление карбонильных соединений протекает в мягких условиях. Альдегиды окисляются до карбоновых кислот. Кетоны окисляются до смеси кислот с разрывом углеводородной цепочки:
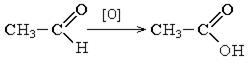
Реакции серебряного зеркала:
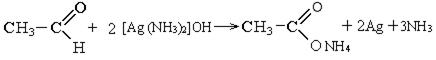
Реакции с участием α- водородных атомов. В альдегидах и кетонах атомы водорода в α- положении к углероду карбонильной группы очень подвижны и способны диссоциировать по типу кислоты.
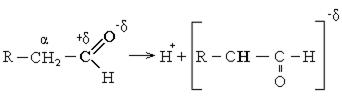
Подвижность протонов в α- положении обусловлена акцепторным влиянием кислорода, снижающим электронную плотность на углероде в α- положении.
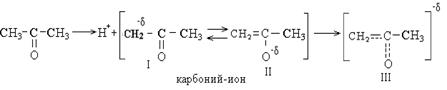
Структура ІІІ энергетически стабильна, так как стабилизирована резонансом. Структура ІІІ является гибридом двух структур: І и ІІ.
1. Реакция бромирования:
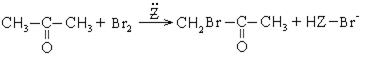
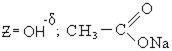
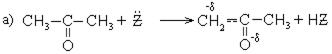
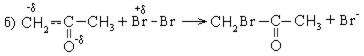
Дата добавления: 2015-03-19; просмотров: 3443;
