Принцип методу. При титруванні заліза (II) ванадатом амонію NH4VO3 у розчині проходить окиснювально-відновний процес:
При титруванні заліза (II) ванадатом амонію NH4VO3 у розчині проходить окиснювально-відновний процес:
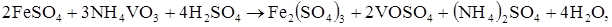
який в іонному вигляді можна записати:
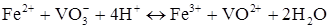 (хімічна реакція).
(хімічна реакція).
В електродній реакції бере участь визначувана речовина, що здатна окиснюватися на Pt мікроаноді при накладенні зовнішньої ЕРС=1 В (нас. к.е.):
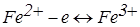 (електродний процес).
(електродний процес).
При зануренні електродів у досліджуваний розчин за рахунок окиснювання заліза (II) у ланцюзі фіксується високий дифузійний струм, величина якого пропорційна концентрації Fe2+ (рис. 7.20). При титруванні кількість заліза (II) зменшується. Знижується і величина дифузійного струму (ділянка АВ, рис. 21). За точкою еквівалентності (ТЕ) значення струму (Iост.) мінімально і постійно (ділянка ВС).
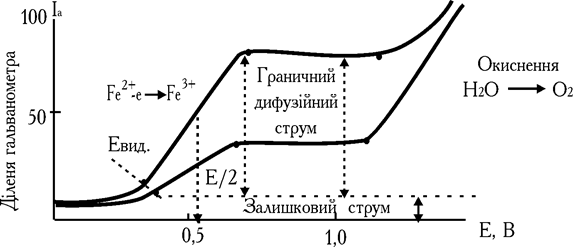
Рис. 7.20. Вольтамперні криві Fe2+ різної концентрації
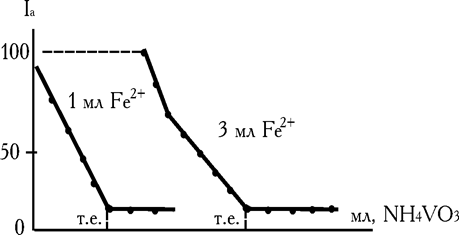
Рис. 7.21. Крива амперометричного титрування заліза (II) – NH4VO3
Необхідні прилади, реактиви і посуд
1. Амперометрична установка будь-якого типу.
2. Платиновий обертовий електрод
3. Насичений каломельний електрод.
4. Мірний циліндр місткістю 50 мл.
5. Мікробюретка 2–5 мл.
6. Стаканчик для титрування місткість 50 мл.
7. Розчин H2SO4.
8. Розчин NH4VO3, 0,01М.
9. Аналізований розчин солі Мору або сульфату заліза (II).
Дата добавления: 2015-03-19; просмотров: 800;
