Хлорфторвуглеводні і озон
Найбільш поширеними в даний час в атмосфері хлорфторвуглеводнями (ХФВ) є Фреон–11 (CFCl3) і Фреон–12 (CF2Cl2). Їх широке надходження в атмосферу почалося з 1970-х років завдяки їх використанню для аерозолів і як холодоагенти.
Під дією УФ ХФВ фотодисоціюють з утворенням атомарного хлору:
CFCl3 + hv = CFCl2 +·Cl,
CF2Cl2 + hv = CF2Cl +·Cl.
Атоми хлору, як сказано вище, стають каталізаторами розкладання озону:
O3 + ·Cl = O2 +·ClO,
ClO· + ·O = O2 +·Cl
за сумарним рівнянням реакції:
O3 + ·O = 2O2.
Як правило, реакція протікає з участю ще і «третіх речовин»:
2Cl· + 2O3 = 2ClO·+ 2O2
2ClO· + M = Cl2O2 +·M,
Cl2O2 + hv = ClO2 +·Cl,
ClO2 +·M = Cl·+ O2 + M
Тобто, сумарна реакція виглядатиме як:
2O3 = 3O2.
Згідно даним Всесвітньої Метеорологічної Організації швидкість зниження загального змісту озону в середніх широтах складає 4–5 % за 10 років. Головною причиною цього є дія антропогенних викидів сполук хлору і брому.
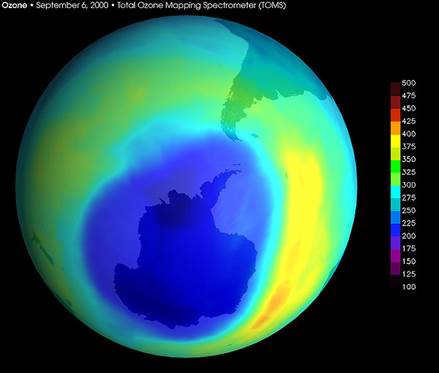
Зображення антарктичної озонової діри, вересень 2000.
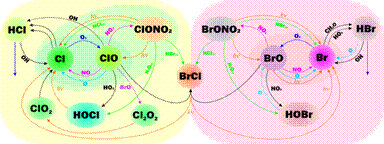
Схема реакції галогенів в стратосфері, що включає реакції галогенів з озоном
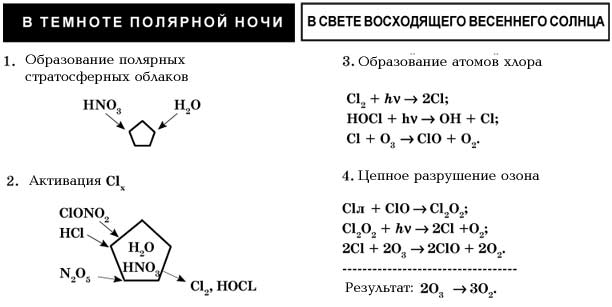

Озоновий шар в атмосфері
Дата добавления: 2014-12-17; просмотров: 1674;
