Атомно-кристаллическое строение металлов
Все элементы таблицы Менделеева делятся на металлы (К, Na, Cu, Ag и др.) и неметаллы (S, Р, С, О, N, Н и др.). Металлы обладают следующими свойствами:
· высокой тепло- и электропроводностью;
· с ростом температуры электросопротивление металлов растёт;
· высокой термоэлектронной эмиссией, то есть металлы при нагреве легко испускают электроны;
· наличием металлического блеска;
· высокой пластичностью - их можно ковать.
У металлов в отличие от аморфных тел атомы расположены в строго определенной последовательности, образуя кристаллическую решетку.
У металлов чаще всего встречаются следующие кристаллические решетки: кубическая, гексагональная, тетрагональная.
Кубическая решеткабывает объемно центрированная и гранецентрированная.
Объемно центрированная кубическая решетка (ОЦК) (рис. 1.1). Такую решетку имеет железо до 910о С, а также Сr, Мо, W, Nb и другие металлы.
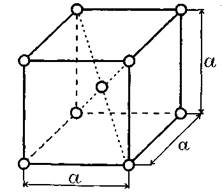
Рис.1.1. Объёмно центрированная решетка
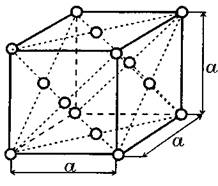
Рис. 1.2. Гранецентрированная кубическая решетка
Период- это расстояние между двумя параллельными атомными плоскостями в элементарной ячейке. Измеряется в нанометрах. 1 нм = 10А =10-9 см. Для Fе период решетки равен 2,86 А. Он характеризует объем этой ячейки.
Гранецентрированная кубическая решетка (ГЦК) (рис. 1.2). Такую решетку имеет железо выше 910о С, а также Al, Cu, Ni и другие металлы. Период а - это ребро куба.
Гексагональная решёткаимеет два периода решетки: а ≠с (рис. 1.3). Такую решетку имеют кадмий, цинк, графит и магний
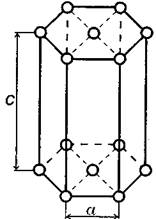
Рис. 1.3. Гексагональная решетка
Тетрагональная решетка (закаленная сталь; Mn; In) (рис. 1.4) c≠a. Она может быть объемно центрированной или гранецентрированной.
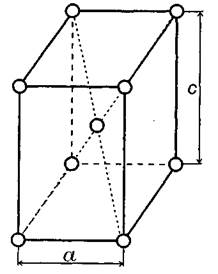
Рис. 1.4. Тетрагональная объёмно центрированная решетка
Дата добавления: 2014-12-01; просмотров: 1854;
