Основность
Наличие неподеленной пары электронов у атома азота, которые могут быть представлены на образование связи с протоном, обеспечивает ароматическим аминам основные свойства
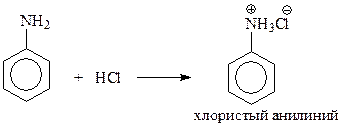
Интерес представляет сопоставление основности алифатических и ароматических аминов. Как уже было показано при изучении алифатических аминов, об основности аминов удобно судить по константе основности Кв
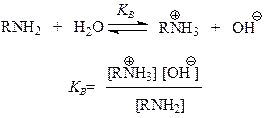
Сравним основности анилина, метиламина и аммиака
Кв
Аммиак 1,7.10-5
Метиламин 4,4.10-4
Анилин 7,1.10-10
Из этих данных видно, что появление электронодонорной метильной группы повышает электронную плотность у атома азота и приводит к усилению основности метиламина по сравнению с аммиаком. В то же время фенильная группа более чем в 105 раз ослабляет основность анилина по сравнению с аммиаком.
Уменьшение основности анилина по сравнению с алифатическими аминами и аммиаком может быть объяснено сопряжением неподеленной пары электронов азота с секстетом электронов бензольного кольца
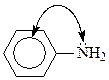
Это снижает способность неподеленной пары электронов присоединять протон. Еще более эта тенденция сказывается у ароматических аминов, которые содержат в бензольном кольце электроноакцепторные заместители
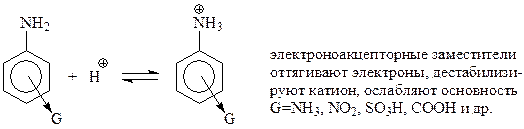
Так, м-нитроанилин как основание в 90 раз слабее, чем анилин.
Как и можно было ожидать, электронодонорные заместители в бензольном кольце усиливают основность ароматических аминов
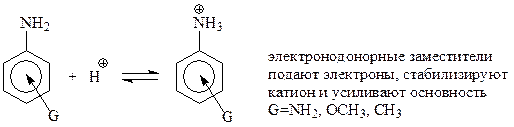
Жирноароматические амины под влиянием алкильной группы проявляют бóльшую основность, чем анилин и амины с электроноакцепторными группами в кольце.
17.2.2. Реакция с азотистой кислотой.Особый интерес к реакции аминов с азотистой кислотой вызван тем, что она позволяет различить первичные, вторичные и третичные амины. Кроме того, в случае участия в реакции первичных аминов получаются, имеющие большое препаративное значение, соли диазония
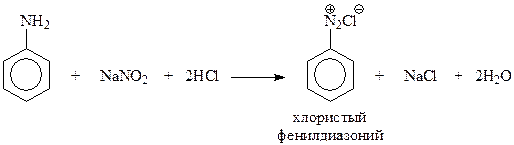
Поскольку азотистая кислота неустойчива, ее обычно получают из ее соли и более сильной минеральной кислоты по ходу опыта
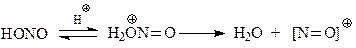
Азотистая кислота в кислой среде диссоциирует с образованием нитрозокатиона, который и реагирует с амином.
С вторичными жирно-ароматическими аминами азотистая кислота реагирует с образованием п-нитрозоаминов
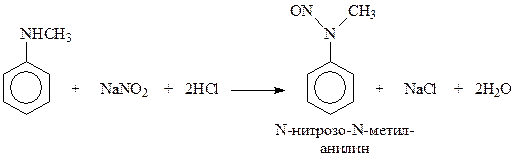
Такие соединения в кислой среде перегруппировываются таким образом, что нитрозогруппа перемещается в п-положение бензольного кольца
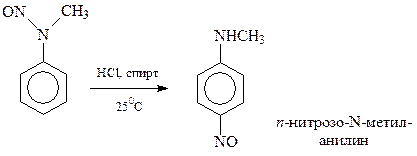
Реакция третичных аминов с азотистой кислотой представляют собой частный случай электрофильного замещения. При этом слабый электрофил –
нитрозогруппа - вступает в бензольное кольцо в п-положение. А если оно занято – в о-положение
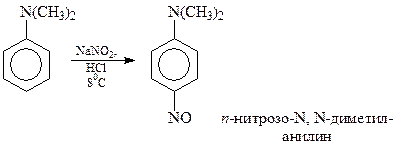
Восстановлением нитрозогруппа трансформируется в аминогруппу, а окислением – в нитрогруппу
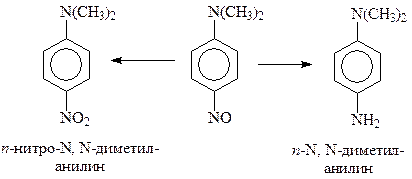
Несмотря на различный результат реакции азотистой кислоты с первичными, вторичными и третичными аминами, все они идут по одной схеме – ион нитрония атакует в молекуле амина место с наибольшей электронной плотностью и замещает протон. В случае первичных и вторичных аминов – это атом азота, у третичных аминов – активированное аминогруппой п-положение бензольного кольца.
17.2.3. Окисление.Появление аминогруппы в бензольном кольце делает его крайне уязвимым к действию окислителей. Действительно, анилин легко окисляется при хранении под действием кислорода воздуха.
При окислении анилина различными окислителями получается множество соединений: азобензол, азоксибензол, нитробензол, хинон и др.
Предполагается, что в процессе окисления первоначально образуется нестабильный свободный радикал, который далее окисляется как с участием азота, так и бензольного кольца
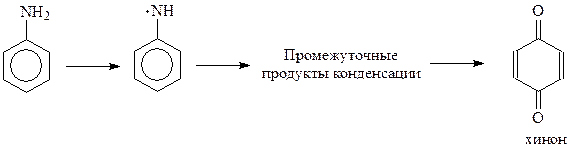
Дата добавления: 2014-12-24; просмотров: 3909;
