Генетический контроль экспрессии генов
Что понимают под генетическим контролем экспрессии или регуляции действия генов? Это понятие означает, что экспрессия гена или набора генов может избирательно увеличиваться или уменьшаться (индуцироваться или репрессироваться) селективно. Регулирующее действие осуществляют белки, которые могут вмешиваться в транскрипцию. На экспрессию оказывает влияние изменение уровня АТФ, но это соединение не является результатом.
Сведения о регуляторных механизмах экспрессии генов по большей части получены в результате изучения образцов контроля активности генов, распространяемых на последовательность реакции в биосинтезе микроорганизмами белков, на гены фага лямбда, 5 S-гены Xenopus, гены, обеспечивающие скрещивание дрожжей, и гены, вовлеченные в контроль развития эукариотов. Сравнение механизмов, контролирующих действие генов у разных организмов, показывают чрезвычайное разнообразие в этих механизмах. В этом убеждает рассмотрение наиболее изученных систем. В применении к бактериям известно два механизма, один из которых контролирует активность ферментов, тогда как второй — синтез ферментов (синтез специфических белков). Сущность контроля (регуляции) активности ферментов иллюстрируется примером биосинтеза изолейцина, ранним предшественником которого является треонин и превращение которого в изолейцин осуществляется в результате пяти последовательных реакций с участием ферментов. Если к культуре бактерий, обладающих самостоятельной способностью синтезировать аминокислоты, в том числе изолейцин, прибавить изолейцин, то это приводит к прекращению клетками синтеза данной аминокислоты. Ростовые потребности клеток в это время обеспечиваются лишь экзогенным изолейцином. Механизм этого явления заключается в ингибировании (подавлении) активности фермента, катализирующего превращение треонина в последующий предшественник изолейцина. Синтез восстанавливается лишь тогда, когда экзогенный изолейцин истощается в среде.
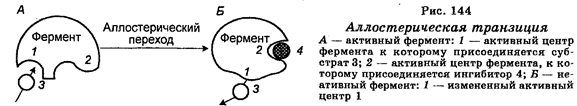
Уникальность этого явления связана с тем, что ингибитор (конечный продукт) и нормальный субстрат имеют различную структуру и не конкурируют за один и тот же сайт связывания на ферменте. Можно сказать, что фермент несет два сайта связывания, один из которых специфичен для субстрата, другой — для ингибитора. Нормально субстрат прикрепляется к активному сайту фермента. Однако если к этому специфическому сайту прикрепляется ингибитор, то наступает структурное превращение (транзиция) в ферменте, вследствие чего нормальный субстрат больше не прикрепляется, что блокирует активность фермента, катализирующего конец биосинтеза либо одну из его стадий. Это явление получило название аллостерической транзиции (рис. 144).
В основе аллостерического взаимодействия лежит любое измерение в активности фермента, вызываемое избирательным связыванием на втором сайте фермента, причем этот сайт не перекрывает сайта на ферменте для связывания субстрата. Фермент, по существу, становится химическим трансдуктором, позволяющим взаимодействие между двумя молекулами — ингибитором и субстратом, которое другим способом исключено. Определенные ферменты чувствительны к активированию при соединении их с эф- фекторной молекулой, отличной от каталитического субстрата. Кроме того, определенные ферменты чувствительны к активированию одним метаболитом и подавлению другим. Поскольку возможны мутации, которые могут поражать один ингибиторный сайт, не затрагивая другого, фенотипически они проявляются в резистентности клеток к ингибированию конечным продуктом и в выработке ими больших количеств конечного продукта. Таким образом, аллостерическая транзиция обеспечивает исключительно гибкую систему регуляции активности ферментов.
Синтез ферментов регулируется с помощью индукции и репрессии ферментов, заключающихся в стимуляции или подавлении синтеза специфических ферментов как ответной реакции на добавление в среду компонента, повышающего концентрацию эффектора в клетке.
Примером индукции ферментов является случай с ферментами бактерий, обеспечивающих утилизацию лактозы. Бактерии приобретают способность сбраживать лактозу после некоторого культивирования в присутствии этого углевода. Это определяется синтезом ими b-галактозидазы, которая расщепляет лактозу на глюкозу и галактозу, а также b-галактозидпермеазы и b-галактозидтранс-цетилазы, обеспечивающих проникновение субстрата в клетку и ацетилирование некоторых токсических галактозидов в направлении их детоксификации (соответственно). Следовательно, лактоза индуцирует синтез ферментов, причем этот синтез является координированным .
Примером репрессии ферментов может служить синтез трипто-фана, который образуется из антраниловой кислоты с участием ант-ранилатсинтетазы. Если бактерии посеять в среду, в которой в качестве источника азота и углерода содержатся NH4Cl и глюкоза, соответственно, то они очень хорошо растут и самостоятельно синтезируют триптофан (как и другие аминокислоты). Но если в среду добавить экзогенный триптофан, то бактерии перестают синтезировать эту аминокислоту. Важно заметить, что добавление триптофана останавливает синтез всех ферментов, участвующих в его биосинтезе. Таким образом, конечный продукт подавляет весь биосинтез.
Опираясь на данные об индукции и репрессии белков, французские ученые Ф. Жакоб и Ж. Моно (1961) сформулировали модель генетического контроля синтеза белков, компонентами которой являются гены структуры, регуляции и операторные гены, а также цитоплазматический репрессор. По этой модели молекулярная структура белков определяется генами структуры, первичным продуктом которых является мРНК. Синтез мРНК может быть начат лишь на определенном пункте цепи ДНК (операторе), от которого может зависеть и транскрипция нескольких сцепленных структурных генов. Группа генов, транскрипционная активность которых координируется одиночным оператором, представляет собой опе-рон, являющийся единицей первичной транскрипции и единицей координированной экспрессии генов. Таким образом, бактериальные опероны транскрибируются в полицистронные мРНК. Существуют также гены-регуляторы. Под контролем того или иного гена-регулятора продуцируется цитоплазматический фактор-репрессор, который обладает реверсивной способностью связываться со специфическим оператором. Благодаря этому связыванию комбинация репрессора и оператора блокирует начало транскрипции всего оперона (формирование мРНК), контролируемой оператором и, следовательно, предотвращает синтез белков, управляемый структурными генами, принадлежащими оперону.
Репрессор обладает свойством специфически связываться (реагировать) с малыми молекулами (эффекторами). В случае индуцированных ферментных систем репрессор связывается с оператором и блокирует транскрипцию олерона. Присутствие эффектора (индуктора) связывает (инактивирует) репрессор, и это приводит к тому, что происходит транскрипция и трансляция генов оперона. Другими словами, репрессор, соединенный с эффектором, теряет родство к оператору и не связывается с ним, а это сопровождается активацией оперона. В случае репрессибельных ферментов репрессор сам по себе является неактивным, т. е. не имеет родства к оператору и не блокирует транскрипцию оперона. Он активируется лишь в результате комбинации (соединения) с конечным продуктом в биосинтезе, в результате чего блокирует транскрипцию оперона. Следовательно, транскрипция оперона происходит в отсутствие эффектора (конечного продукта), тогда как присутствие эффектора сопровождается ингибированием оперона.
Регуляторные механизмы в случае индуцибельных и репрессибельных систем имеют негативный характер, т. к. подавляют синтез специфических белков. Регуляторный механизм оперирует на генетическом уровне, контролируя частоту синтеза мРНК. Опероны классифицируют на катаболизирующие (индуцибельные) и синтезирующие (репрессибельные).
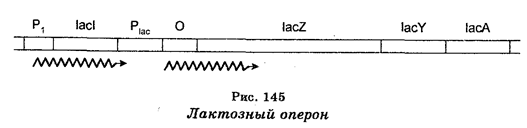
Примером катаболизирующих оперонов является лактозный оперон (рис. 145), в состав которого входят структурные гены z, у и a, кодирующие b-галактозидазу, b-пермеазу и b-трансацетилазу, соответственно, ген-регулятор lac 1, кодирующий синтез репрессоpa (белок мм. 37 200, состоящий из четырех идентичных единиц, содержащих по 377 аминокислотных остатков), промоторы P2 и Р1, к которым присоединяется РНК-полимераза, и ген-оператор (О), управляющий функционированием структурных генов.
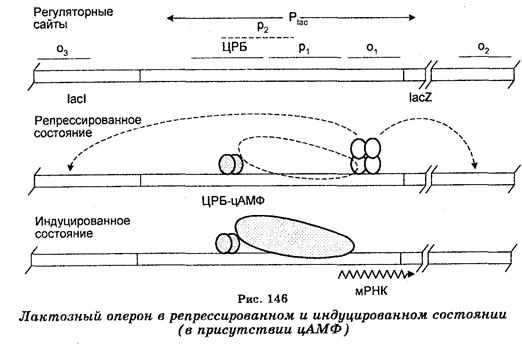
Механизм регуляции лактозного оперона заключается в том, что в отсутствие индуктора (лактозы) репрессор активен, т. е. продукт гена lac 1 связан с оператором O1 в соединении с двумя другими операторами (О2 и О3) и это блокирует транскрипцию полигенной мРНК, т. е. предупреждает движение РНК-полимеразы с промотора. Операторы О2 и О3, которых часто называют псевдооператорами, повышают связывание репрессора с оператором О1. Промотор P1 частично перекрывается вторым промотором P2, который в нормальных условиях не имеет существенного значения. РНК-полимераза может подходить к обоим промоторам, но основным все же является промотор Р1, поскольку движение РНК-полимеразы к промотору P2 ингибируется белком CRP, который при этом стимулирует транскрипцию с промотора P1. При наличии в среде индуктора репрессор теряет активность, т. е. связывается с индуктором, вследствие чего оператор становится свободным (деблокируется), и в результате движения РНК-полимеразы происходит транскрипция мРНК. При наличии в среде лактозы синтез ферментов увеличивается в 1000 раз. Инициация транскрипций требует наличия циклического АМФ и белка сгр. Следовательно, лактозный оперон контролируется негативно путем контроля частоты синтеза мРНК (рис. 146).
Однако возможна и позитивная регуляция лактозного оперона. Если вслед за индуктором в среду, где выращены бактерии,прибавить глюкозу, то наступает катаболитная репрессия (3-галак-тозидазы, сопровождающаяся снижением уровня цАМФ. Если же в культуру прибавить экзогенный цАМФ, то катаболитическая репрессия снимается и лактозный оперон будет функционировать нормально. Таким образом, цАМФ является позитивным регулятором (регуляция происходит в присутствии индуктора).
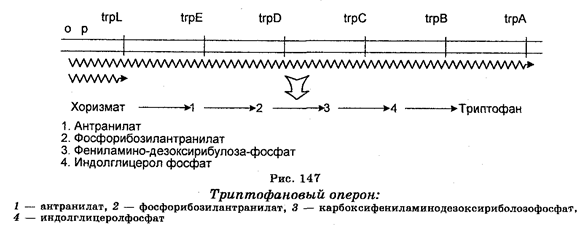
Примером биосинтезирующего оперона является триптофановый оперон, который состоит из 5 генов trpE, D, С, В и А, кодирующих ферменты, участвующие в биосинтезе триптофана (рис. 147). Первая химическая реакция, характерная для синтеза триптофана (как и для тирозина и фенилаланина), заключается в конденсации (накоплении) эритрозы-4-Ф и фосфоенолпирувата, необходимых для образования З-дезокси-арабино-гептулозоната-7-Ф (ДДГФ), катализируемого ДАГФ-синтетазой. Образующийся продукт (хоризмат) с помощью ферментов превращается в триптофан. Экспрессия этого оперона находится под негативным контролем репрессора, являющегося продуктом гена trp R. Репрессия конечным продуктом (трип-тофаном) заключается в том, что неактивный в свободном состоянии репрессор не мешает переходу РНК-полимеразы к промотору, т. е. не мешает транскрипции мРНК. Репрессор становится активным в результате связывания с конечным продуктом (триптофаном). Когда комплекс репрессор + триптофан связывает оператор, то это предупреждает преход РНК-полимеразы к промоторам, т. е. подавляет синтез мРНК. Более тонкий механизм заключается в том, что продукт гена trp R (репрессор) ингибирует синтез одной из ДАГФ-синтетаз, в частности, синтетазу АгоН, путем ингибирования ее мРНК, а следовательно, ингибирует и мРНК всего гистидинового оперона.
То, что существуют различные пути регуляции генов, подтверждается данными о регуляции оперона ara BAD, который ответственен за метаболизм арабинозы, встречающейся обычно в стенках клеток растений, а у микроорганизмов — являющейся одним из источников углерода и энергии. Арабиноза попадает в организм животных или человека с растительной пищей, где она метаболи-зируется микроорганизмами. Однако прежде она должна поступить в бактерии. Это поступление арабинозы в бактериальные клетки, т. е. транспорт арабинозы обеспечивается двумя независимыми системами, представляющими собой продукты генов ara Е и ara FG (рис. 148).
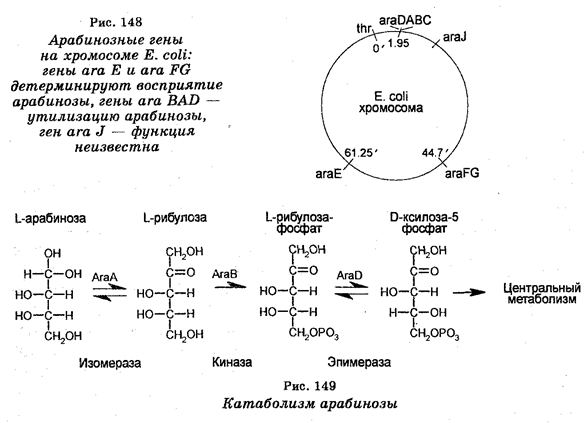
Система ara Е обладает низким родством к арабинозе, поэтому она используется лишь при очень высоких концентрациях этого углевода, тогда как система ara FG, обладающая высоким родством к арабинозе, используется при очень низких концентрациях углевода (порядка 10-7 М).
Гены, кодирующие ферменты, которые необходимы для катаболизма арабинозы, показаны на рис. 149. Катаболизм арабинозы начинается с того, что она вначале конвертируется синтезируемая под контролем гена ara А арабинозной изомеразой в L-рибулозу. Затем рибулоза фосфорилируется рибулозокиназой, являющейся продуктом гена ara В в L-рибулозу-б-фосфат. В свою очередь рибулозо-фосфат конвертируется в П-ксилозу-б-фосфат с помощью рибулозо-фосфатэпимеразы, являющейся продуктом гена ara D. Важно отметить, что гены транспортной системы, а также дополнительный арабинозоиндуцируемый ген и гены метаболизма арабинозы локализованы в разных районах хромосомной карты Е. coil. Все эти наборы генов регулируются позитивно арабинозой.
Репрессия метаболических и транспортных генов в ага-опероне осуществляется продуктом (белком) гена ara С. Этот белок является позитивным регулятором. В то же время белок гена ага С может и репрессировать экспрессию этих генов. Таким образом, этот белок существует в двух состояниях — индуцирующем и репрессирующем, индуцируя или репрессируя инициацию транскрипции (начало синтеза мРНК) арабинозного оперона. Индуцирующим свойством белок ага С обладает в присутствии арабинозы, позитивно действуя на один сайт, репрессирующим — в отсутствие этого углевода, действуя негативно на другой сайт (рис. 150).
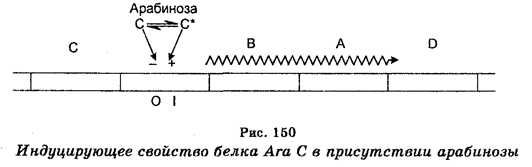
Индукция арабинозного оперона происходит в присутствии цАМФ и белка CRP, являющегося рецептором для цАМФ. Главная роль этого белка заключается в позволении индукции арабинозного оперона только в отсутствие глюкозы. Это получило название катаболитной репрессии.
Опероноподобная организация генетического контроля действия генов показана у фага лямбда, вируса иммунодефицита человека и многих других микроорганизмов.
Считают, что в геноме эукариотических клеток содержится 10 000-50 000 генов-регуляторов. Регулирующие белки, синтезируемые под контролем этих генов, связываются со специфическими последовательностями ДНК вблизи регулируемых генов.
Для некоторых организмов — эукариотов (например, дрожжей) также характерна опероновая организация функционально связанных генов.
Рассмотрение вопроса о регуляции действия генов у организмов на более высокой ступени эволюционной лестницы показывает, что здесь отмечается еще большее усложнение и разнообразие в контроле. Изучение генов, контролирующих синтез 5S-PHK у южноафриканской жабы Xenopus показало, что в овоцитах гены, кодирующие 5S-PHK, экспрессируются лишь в период развития овоци-тов, тогда как ядерные гены соматических клеток, кодирующие синтез 5S-PHK, экспрессируются как в овоцитах, так и в клетках эмбрионов. Установлено также, что синтез 5S-PHK стимулируется белковыми факторами TFA, TFB и TFC. Два последних фактора используются также в транскрипции других генов.
В случае большинства эукариотов считают, что у них нет опе-роноподобной организации генетического контроля действия генов, т. е. эукариотические гены регулируются индивидуально, транс-крибируясь в моноцистронные мРНК, либо эукариотические гены регулируются частично полицистронно, частично моноцистронно. В пользу второго предположения свидетельствуют данные об обнаружении у нематоды С. elegans генов, организованных в опероны. У организма этого вида процессинг полицистронной мРНК в моно-цистронную мРНК происходит до трансляции.
Считают, что генетический контроль синтеза белков у прокари-отов и у эукариотов осуществляется как на уровне транскрипции (частота синтеза мРНК, процессинг мРНК, транспорт мРНК из ядра, стабильность мРНК), так и на уровне трансляции (частота трансляций, регуляции синтеза белковых факторов, ответственных за инициацию, элонгацию и терминацию полипептидной цепи). Считают также, что у эукариотов в генетической регуляции имеет значение структура хроматина, которая блокирует доступ специфических активирующих белков (активаторов) к промоторам. В клетках эукариотов установлен специфический комплекс, который обеспечивает АТФ-зависимое разрушение нуклеосом, позволяя при этом активаторам связываться с нуклеосомным стержнем, что ведет к транскрипции. С другой стороны, установлено, что синтез некоторых ферментов интенсифицируется под влиянием стероид-ных гормонов. Контроль может осуществляться и после трансляции (контроль протеолиза).
Вопросы для обсуждения
1. Что вы понимаете под действием генов и каковы продукты действия генов? Назовите первичные и вторичные продукты действия генов.
2. Дайте определение экспрессивности и пенетрантности генов. Приведите примеры этих свойств генов.
3. Что закодировано в молекулах ДНК?
4. Каковы структура и свойства генетического кода?
б. Что позволяет считать генетический код универсальным?
6. Что вы знаете о разных типах РНК и о тРНК?
7. В состав бактериальной рибосомы диаметром 23 нм входит 35% белка. Сколько белковых молекул м. м. 17 300 может содержаться в ри-босоме, если предположить, что на долю белков приходится 36% объема рибосомы?
8. Что вы знаете о митохондриальном генетическом коде?
9. В чем заключаются различия между ядерным и митохондриаль-ным генетическими кодами?
10. Каково происхождение генетического кода?
11. Один из сегментов молекулы мРНК имеет последовательность УГААГЦГГАУУЦГЦ. В результате мутации шестой слева Ц оказался замененным на У. Как это скажется на полипептиде?
12. Какова разница между индукцией и репрессией ферментов?
13. В чем заключается концепция оперона и каково ее значение в понимании механизмов действия генов?
14. На каких уровнях реализации генетической информации осуществляется генетический контроль экспрессии генов?
15. Чем определяются трудности в изучении генетической регуляции действия генов у эукариот?
16. Сколько типов РНК участвует в биосинтезе белков и что известно о нуклеотидном составе, химических и физических свойствах РНК каждого типа?
17. В научной литературе имеются данные о том, что 7-метил-гуано-зин-б'-монофосфат ингибирует синтез белков в бесклеточной системе, происходящей из ретикулоцитов. Известно также, что на 5'-конце многих молекул мРНК эукариотических клеток имеется 7-метилгуанозин. Известно также, что если удалить эту группу из мРНК (химическим путем) вируса везикулярного стоматита, то это не предотвращает трансляцию в бесклеточной ретикулоцитной системе. Можете ли вы объяснить значение этих данных?
18. Какое влияние оказывает на регуляцию триптофанового оперона увеличение длины РНК-полимеразы?
Литература
Дубинин Н. П. Генетика. Кишинев: Штиинца. 1985. 533 стр.
Пехов А. П. Биология и общая генетика. М.: РУДН, 1993. 439 стр.
Schleif R. Genetics and Molecular Biology. The Johns Hopkins Univesity Press. 1993. 698 pp.
Дата добавления: 2014-12-20; просмотров: 2312;
