Обмен метгемоглобина
В течение суток до 3% гемоглобина может спонтанно окисляться в метгемоглобин:
Hb (Fe2+) ® Met Hb (Fe3+) +e-
Восстановление метгемоглобина до гемоглобина осуществляет метгемоглобинредуктазная система. Она состоит из цитохрома b5 и цитохром b5 редуктазы (флавопротеин), донором водорода служит НАДН2, образующийся в гликолизе.
1). Цитохром b5 восстанавливает Fe3+ метгемоглобина в Fe2+ гемоглобина:
MetHb(Fe3+) + цитb5 восст → Hb(Fe2+) + цит b5 окисл
2). Окисленный Цитохром b5 восстанавливается цитохром b5 редуктазой:
цит b5 окисл + НАДН2 → цитb5 восст + НАД+
Восстановление метгемоглобина может осуществляться также неферментативным путём, например, за счёт витамина В12, аскорбиновой кислоты или глутатиона.
У здорового человека концентрация метгемоглобина в крови не превышает 1%.
Генетический дефект ферментов гликолиза и метгемоглобинредуктазной системы приводит к накоплению метгемоглобина и увеличению образования активных форм кислорода. Активные формы кислорода вызывают образование дисульфидных мостиков между протомерами метгемоглобина, что приводит к их агрегации с образованием телец Хайнца. Последние способствуют разрушению эритроцитов при попадании их в мелкие капилляры. Накопление метгемоглобина в крови из-за нарушения транспорта кислорода ведет к гипоксии.
Строение гема
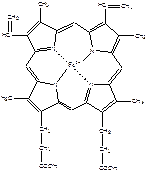
| Гем - это порфирин, в центре которого находиться Fe2+. Fe2+ включается в молекулу порфирина с помощью 2 ковалентных и 2 координационных связей. В зависимости от заместителей различают несколько типов порфиринов: протопорфирины, этиопорфирины, мезопорфирины и копропорфирины. В основе порфиринов находится порфин, который представляет собой конденсированную систему из 4 пирролов, соединенных между собой метиленовыми мостиками (-СН=). Молекула гема имеет плоское строение. При окислении железа, гем превращается в гематин (Fe3+). |
Использование гема
Гем является простатической группой многих белков: гемоглобина, миоглобина, цитохромов митохондриальной ЦПЭ, цитохрома Р450, ферментов каталазы, пероксидазы, цитохромоксидазы, триптофанпироллазы. Наибольшее количество гема содержат эритроциты, заполненные гемоглобином, мышечные клетки, имеющие миоглобин, и клетки печени, содержащие цитохром Р450.
Гемы разных белков могут содержать разные типы порфиринов. В геме гемоглобина находится протопорфирин IX, в состав цитохромоксидазы входит формилпорфирин и т.д.
Синтез гема
Гем синтезируется во всех тканях, но с наибольшей скоростью в костном мозге и печени. В костном мозге гем необходим для синтеза гемоглобина, в гепатоцитах — для образования цитохрома Р450.
1). Аминолевулинат-синтаза, пиридоксальзависимый фермент, в матриксе митохондрий катализирует образование 5-аминолевулиновой кислоты (5-АЛК) из глицина и суцинил-КоА. Суцинил-КоА поступает из ЦТК. Реакцию ингибирует и репрессирует гем. В ретикулоцитах реакцию индуцирует железо (через железосвязывающий белок и железочувствительный элемент (IRE)). Дефицит пиридоксальфосфата снижает активность аминолевулинатсинтазы. Стероидные гормоны и некоторые лекарства (барбитураты, диклофенак, сульфаниламиды), инсектициды, канцерогенные вещества являются индукторами аминолевулинатсинтазы. Это связано с возрастанием потребления гема системой цитохрома Р450, который участвует в метаболизме этих соединений в печени.
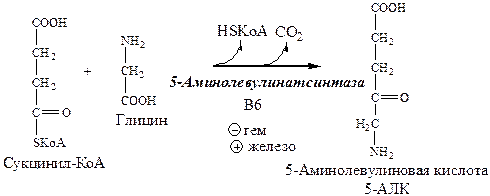
Из митохондрий 5-аминолевулиновая кислота поступает в цитоплазму.
2). Порфобилиноген-синтаза (Аминолевулинатдегидратаза) цитоплазматический Zn-содержащий фермент, соединяет 2 молекулы 5-аминолевулиновой кислоты в молекулу порфобилиногена. Реакцию ингибирует гем и ионы свинца. Поэтому, при отравлении свинцом в крови и моче повышается концентрация 5-АЛК.
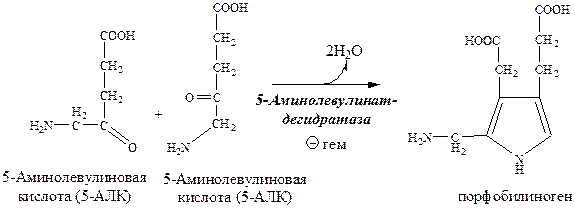
3). Порфобилиногендезаминаза в цитоплазме дезаминирует (-4NH4+) 4 молекулы порфобилиногена в молекулу гидроксиметилбилана.
4). Уропорфириноген III косинтаза в цитоплазме дегидрирует гидроксиметилбилан в молекулу уропорфириногена III. Гидроксиметилбилан может также неферментативно превращаться в уропорфириноген I, который декарбоксилируется в копропорфириноген I.
5). Уропорфириногендекарбоксилаза декарбоксилирует (-4СО2) в цитоплазме уропорфириноген III до копропорфириногена III. Из цитоплазмы копропорфириноген III опять поступает в митохондрии.
6). Копропорфриноген III оксидаза в митохондриях декарбоксилирует (+ О2, -2СО2) копропорфириноген III в протопорфириноген IX.
7. Протопорфириногеноксидаза в митохондриях окисляет (-6Н+) протопорфириноген IX в протопорфирин IX.
8). Феррохелатаза в митохондриях встраивает Fe2+ в молекулу протопорфирина IX с образованием гема. Источником железа для синтеза гема служит ферритин.
Дата добавления: 2017-09-19; просмотров: 829;
