Дегидрогалогенирование
ОБРАЗОВАНИЕ ДВОЙНОЙ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
Один из величайших химиков-синтетиков Роберт Вудворд сказал: «В органическом синтезе можно найти и вызов, и дерзание приключения, и озарение и вдохновение искусства. Легко представить себе, насколько более скучным стало бы занятие органической химией, если эти стимулы утратили свое значение.
По современным представлениям, изложенным в книге В.А. Смита и др. «Органический синтез. Наука и искусство», органический синтез – это суть оператор (алгоритм, последовательность операций) с помощью которого можно производить строго определенные преобразования молекулярной структуры исходного соединения. При этом можно проводить аналогию между сборкой механической конструкции и построением молекулы. Во всех случаях используются какие-то детали «конструкционные блоки», из которых создается объект, будь-то: здание, машина или молекула.
Конструкционные блоки в органическом синтезе называются синтоны. По определению данному в книгах Марча (4-х томник «Органическая химия» 1988) синтон определяется как структурная единица молекулы , которая может быть введена или создана в результате известной или возможной синтетической операции.
Одним из наиболее распространенных синтонов является двойная углерод-углеродная связь. Двойная углерод-углеродная связь построена из атомов углерода в состоянии sp2-гибридизации. В соответствие с типами органических реакции, связанных с изменением субстрата может быть два пути получения двойной связи: это присоединение, при котором степень гибридизации повышается при этом sp переходит в sp2, а также элиминирование, при котором степень гибридизации понижается sp3 переходит в sp2.
Наиболее широкое распространение получили методы, основанные на элиминировании. Причем не просто элиминировании, а β- или 1,2-элиминировании.
Элиминирование
Общие положения
Определение: Элиминирование – это реакция, в ходе которой от субстрата отщепляется молекула (вода, галогеноводород, производное толуолсульфокислоты) или частица ().
Существует несколько видов элиминирования: α-элиминирование, β-элимирование, γ-и δ-элиминирование, орто-элиминирование.
α-Элиминирование приводит к образованию карбенов. γ-и δ-Элиминирования приводят к образованию малых циклов. Общий способ получения циклоалканов с сохранением числа углеродных атомов. орто-Элиминирование наблюдается при нуклеофильном замещении в ароматическом ядре, протекающим по ариновому механизму. Например, получение смеси пара- и мета-крезолов по реакции пара-бромтолуола с едким натром.
Самое распространенное β-элимирование. Реакции β-элимирование протекают как два последовательных или одновременных ухода различной природы:
1. Катионоидный отрыв протона Н+, вызванного атакой основания и формирование карбаниона, а затем анионоидный отрыв аниона галогена Х-;
2. Анионоидный отрыв аниона галогена Х- или молекулы (вода) и формирование карбокатиона, за которым следует отрыв протона Н+ .
3. Одновременный катионоидный и анионоидный отрыв.
При β-элимировании можно получить: двойные углерод-углеродные связи, тройные углерод-углеродные связи, двойные связи углерод-гетероатом, тройные связи углерод-гетероатом, двойную связь между двумя гетероатомами. Для β-элимирования действуют две классификации. Это, во-первых, элиминирование с участием функциональных производных углеводородов и элиминирование для продуктов конденсации. Во-вторых, для элиминирования действуют два правила: Зайцева и Гофмана. По Зайцеву образуется наиболее алкилированный олефин. По Гофману наименее алкилированный.
Правило Зайцева реализуется в случае элиминирования с участием электроотрицательных групп, уходящих в форме анионов: Основные группы, уходящие в виде нуклеофильных частиц (нуклеофуги) представляют электроотрицательные группы, способные уходить в виде ионов – ионы галогенов, меркаптид-ион, алкоксид-ион, бисульфат-ион, тозилат-ион:
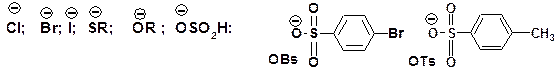
По Гофману протекает элиминирования с участием ониевых ионов, при этом уходящей группой является нейтральная молекула, кроме воды. Причем отщепление нейтральной молекулы происходит после отщепления протона. Ухолдящие группы присутствуют в молекуле субстрата в форме ониевых ионов – оксоний, аммоний фосфоний, сульфоний, диазоний:
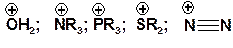
Уходят от молекулы субстрата в виде нейтральных молекул, героатомы которых обладают неподеленной электронной парой: вода, аммиак, фосфин, сульфид, азот. Объяснение образованию продукта по Гофману основано на том, что положительно заряженная группа, обладающая отрицательным индуктивным эффектом ослабляет β-связи и наиболее слабыми становятся те, которые рядом не имеют заместителей с положительным индуктивным эффектом.
Основные группы, уходящие в виде электрофильных частиц – это протон, ионы металлов, могут быть электроотрицательные элементы.
Стереохимия
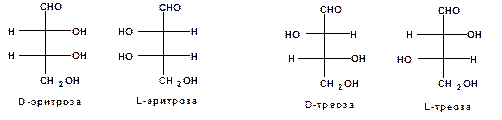
эритро-Изомер – это изомер, в котором все пары эквивалентных заместителей можно разместить так, что они будут находиться друг против друга. Другой изомер является трео-изомером. эритро-Изомер часто содержит два ассиметрических атома углерода, имеющие абсолютные конфигурации R и S, а трео-изомер – два атома углерода RR или SS.
Если при асиметрических атомах углерода находятся одинаковые заместители, то эритро-изомер становится совместимым со своим зеркальным изображением, а трео-изомер не может быть совмещен.
Не разделимый на оптические антиподы изомер называется мезо-изомером. Вторая форма представляет собой рацемат.
При синхронном элиминировании необходимо, чтобы р-орбитали атомов, у которых происходит элиминирование, были параллельны. Только в этом случае возможно образование π-связи. Различают два типа элиминирования: анти-элиминирование, при котором уходящие группы находятся в одной плоскости по разные стороны углерод-углеродной связи – антиперипланальны, и син- элиминирование, при котором уходящие группы находятся в одной плоскости по одну сторону углерод-углеродной связи – синперипланальны:
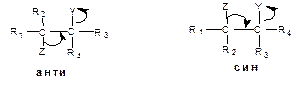
Эти процессы стереоспецифичны. Исходя из пары эритро- и трео-изомеров, получают либо цис-, либо транс-олефин в зависимости от типа элиминирования и от конфигурации исходного изомера:

Соотношение продуктов син- и анти- элиминирования зависит от природы уходящей группы и экспериментальных условий. В случае ониевых ионов преимущественно син-элиминирование.
Соотношение цис- и транс- изомера также зависит от природы переходного состояния. Если переходное состояние ближе к ионному, то растет доля цис-изомера. Т.е. присутствие легко уходящих групп и сильного основания способствуют образованию цис-олефина.
Влияние среды
Протонные растворители, обладающие высокой ионизирующей способностью ускоряют реакции Е1
В переходном состоянии Е2 заряд распределен между пятью атомами. В реакции замещения только по трем атомам. Следовательно, в реакции элиминирования большая степень локализации и соответственно меньшие величины зарядов на атомах. Поэтому при элиминировании целесообразно использовать растворители менее полярные, чем при замещении. Практически элиминирование проводят в спиртовой среде, а замещение в водной.
Апротонные высокополярные растворители способны нарушать правило Зайцева и приводить к значительному выходу наименее алкилированного олефина.
Дегидрогалогенирование
Дегидрогалогенирование – наиболее важный способ получения олефинов. Протекает тем легче, чем более склонен галоген к уходу в виде нуклеофильной частицы. Реакцию проводят в присутствии щелочей. КОН в спирте, алкоголятов щечных металлов, этоксид натрия (этилат натрия), трет-бутилат калия, а также аминов: анилин, пиридин, пространственно затрудненные амины:
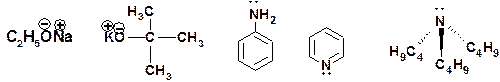
Правило Зайцева выполняется. Однако при использовании сильных и пространственно затрудненных оснований, например, 3-этилпентанолят калия, можно получить исключительно олефин с концевой двойной связью:
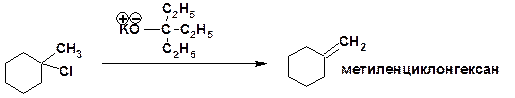
Дата добавления: 2017-08-01; просмотров: 1139;
