Физические свойства и строение.
Номенклатура.
В органической химии три номенклатуры. Но каждому названию должно соответствовать.
1. Тривиальная номенклатура – это система исторически сложившихся названий, но применяемых до настоящего времени. Эти названия даны в ранний период развития органической химии и не отражают строение молекул. Примерами тривиальных названий являются названия первых четырех членов гомологического ряда алканов.
2. Строение молекул учитывает рациональная номенклатура. За основу названия органического соединения принимается название первого члена гомологического ряда. Остальные соединения рассматриваются как его производные, в которых атомы водорода замещены на алкильные радикалы. Например:
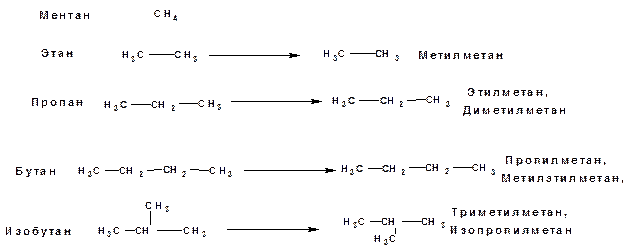
Алкильные радикалы перечисляются в порядке возрастания массы. Радикал нормального строения старше радикала изомерного строения. Если замещающих радикалов больше одного, то их количество обозначается префиксами ди- три- тетра- .
По мере роста количества соединений использование рациональной номенклатуры стало неудобным, и химики перешли к рассмотрению уже атома или группы атомов, а структуру, сформированную цепью углеродных атомов.
3. Рассмотрение наибольшей цепи проводится в систематической номенклатуре. Основы систематической номенклатуры были заложены на съезде химиков в 1892г в Женеве. Что дало основу для названия номенклатуры – женевская. Усовершенствована систематическая номенклатура была на съезде в 1930г в Льеже. Появилась Льежская номенклатура. Современный вариант систематической номенклатуры принят международным союзом по теоретической и прикладной химии (IUPAC) в 1957г. и усовершенствован в 1965г.
Для того чтобы назвать органическое соединение по систематической номенклатуре необходимо:
- выбрать самую длинную (главную) цепь;
- определиться со старшинством групп;
- пронумеровать главную цепь, придавая старшей группе наименьший из номеров локантов;
- перечислить префиксы;
- составить полное название соединения.
Примеры:
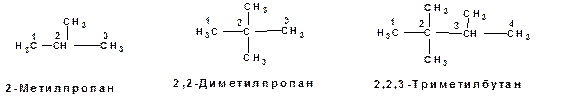
Способы получения.
Все способы получения делятся на промышленные и лабораторные.
Природные источники и промышленные способы получения алканов.
1. Предельные углеводороды с небольшим числом углеродных атомов (до 11) выделяют из природного газа или бензиновой фракции нефти. Основным способом переработки нефтяных фракций являются различные виды крекинга. Крекинг – это термическое разложение углеводородов и других составных частей нефти.
2. По методу Фишера-Тропша алканы можно получать каталитичеким гидрированием окиси и двуокиси углерода:
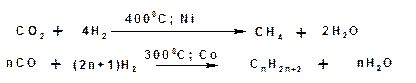
3. Каталитическая гидрогенизация угля. Получила название «ожижение» угля. Твердый каменный уголь в ходе этого процесса превращают в смесь алканов. Эта реакция лежит в основе производства синтетического бензина:
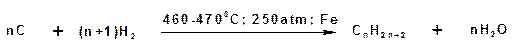
Лабораторные способы получения алканов.
1. Предельные углеводороды, начиная с пентана, наиболее часто получают в лабораторных условиях каталитическим гидрированием непредельных углеводородов с тем же числом углеродных атомов и таким же строением цепи:
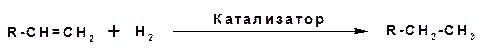
В качестве катализатора используют мелкодисперстные Рt, Pd, Ni. Процесс проводят при обычных температуре и давлении.
2. Предельные углеводороды в лабораторных условиях получают восстановлением галогенпроизводных действием цинка в водном растворе минеральной кислоты или уксусной кислоты:
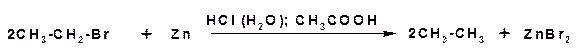
При использовании в качестве субстрата йодистых алкилов можно получить алкан восстановлением йодистоводородной кислоты:
 3. Синтез предельных углеводородов из соединений с меньшим числом углеродных атомов осуществляется действием натрия на галогенпроизводные – реакция Вюрца:
3. Синтез предельных углеводородов из соединений с меньшим числом углеродных атомов осуществляется действием натрия на галогенпроизводные – реакция Вюрца:
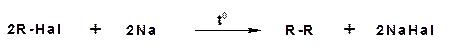
Особенностью синтеза Вюрца является то, что в случае использования в качестве исходных веществ различных галогеналкилов в результате реакции получается смесь трех углеводородов:
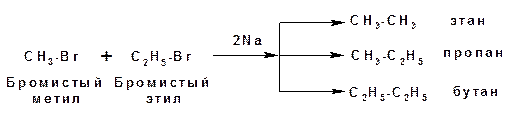
4. Общим способом получения углеводородов является декарбоксилирование карбоновых кислот:
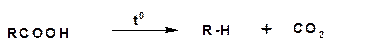
Насыщенные углеводороды в ряде случаев удобнее получать нагреванием натриевой соли карбоновой кислоты с избытком едкого натра:
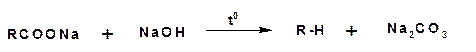
При нагревании натриевой соли карбоновой кислоты с едким натром получается углеводород с числом атомов углерода равным числу атомов углерода в радикале кислоты. Углеводород с удвоенным количеством атомов углерода получается при электролизе натриевой соли карбоновой кислоты:

Физические свойства и строение.
Дата добавления: 2017-08-01; просмотров: 340;
