В природных водах на их качество.
Для определения качесва воды производят физические, химические, бактериологические, биологические и технологические анализы в наиболее характерные периоды для данного водоисточника. Число и объем анализов качества воды зависит от ее назначения.
Т. 1.2. сл.3.
О качестве природной воды судят на основе ее полоного анализа. Правильность определения солевого состава может быть проверена по равенству суммы главных катионов сумме доминирующих анионов, выраженных в мг/л и пересчитанных в мг-экв/л.
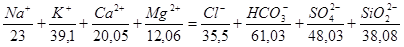

Температура воды подземных источников характеризуется постоянством 8 – 12 0С. Температура воды поверхностных источников меняется по сезонам. Оптимальная температура воды для хозяйствено питьевого водоснабжения 7 – 110С.
Прозрачность, мутность и взвешенные вещества характеризуют наличие в воде суспензированных частиц песка, глины, ила, планктона, водорослей, которые попадают в нее в результате эрозии берегов, с дождевыми и талыми водами. Мутность воды – понятие протовоположное прзрачности, определяют на мутномерах в мг/л путем сравнения образцов вод с имитантами из трепела, каолина или инфузорной земли. Мутность можно определить на ФЭК. По ГОСТ 2874–82 мутность питьевой воды не должна превышать 1,5 мг/л.
Содержание взвешенных частиц определяют путем фильтрования и взвешивания.


 На водоочистных комплексах часто определяют не мутность, а обратную ей величину– прозрачность (ГОСТ 3356–74 "по кресту" и шрифту). По кресту
На водоочистных комплексах часто определяют не мутность, а обратную ей величину– прозрачность (ГОСТ 3356–74 "по кресту" и шрифту). По кресту
– труба 3,5 м Æ 0,03 м – фарфоровый. Нижняя часть подсвечтвается
лампой 300 Вт. Нормой прозрачности питьевой воды является: по кресту – 300 см, по шрифту – 30 см.
Цветность воды обусловлена присутствием гумусовых и дубильных веществ. На окраску так же влияет присутствие железа, сточных вод.
В поверхностных водах с увеличением жесткости, а в гидрокарбонатных – щелочности цветность обычно уменьшается, в то время как мягкие воды с наибольшей щелочностью имебт высокую цветность.
Рис. 1,2. Сл. 4.
Цветность определяют на ФЭК, измеряя оптическую плотность воды.
Привкусы и запахи могут быть естественного (присутствие железа, марганца, H2S) и искусственного происхождения (сброс воды). По ГОСТ 3351–74 различают четыре основных вкуса воды: соленый, горький, сладкий, кислый. Многочисленные оттенки вкусовых ощущуний, складываемых из основных, называются привкусами.
Соленый NaCl; горький – MgSO4; кислый – CO2; щелочной – поташ, сода; вяжущий – CaSO4.
К запахам естественного происхождения относится: землистный, рыбный, гнилостный, сероводородный, ароматический, болотный, глинистный, тинистный. Искусственного происхождения – хлорный, камфорный, аптечный, фенольный.
Интенсивность и характер запахов и привкусов в воде определяется органолептически по 5 – большой шкале.
Т.1,3.сл.5.
Общий, сухой, прокаленный остаток – понятия, позволяющие судить о колличесиве солей и концентрации примесей. Общий или плотный остаток образует содержащие в воде в основном примеси неорганического происхождения (1100С – высушивание). Сухой или растворенный остаток – зарактеризуется содержанием сухих солей или нелетучих органических веществ. Он получается при выпаривании предварительно отфильтрованной воды. Прокаленный остаток – минеральные соли. В питьевой воде не превышает 1г/л.
Хлориды и сульфаты (мг-экв/л или мг/л) благодаря хорошей растворимости присутствуют во всех водах обычно виде натриевых, калиевых, кальциевых солей. Содержание сульфат-ионов в природных водах варьируется 60 – 100 мг/л.
Щелочность воды (мг-экв/л) определяется суммой содержащихся в воде гидроксильных ионов и анионов слабых кислот – угольной, органических. Различают бикарбонатную, карбонатною и гидратную щелочность, которые находят по номограммам. Их сумма обуславливает общую щелочность воды. В процессе обработки почвы могут возникнуть следующие компоненты щелочности.
Т.1.4. сл.6.
Жесткость природных вод вызывается присутствием хорошо растворимых солей ионов Ca2+ и Mg2+, жесткость воды не является вредной для здоровья человека, а скорее наоборот. Кальций способствуев выведению из организма кадмия, отрицательно ввлияющего на сердечно-сосудистую систему.
Железо и марганец присутствуют в водах в формах, зависящих от рН (Fe+2, Fe+3).
Активная реакция воды является показателем ее щелочности или кислотности. Колличесивенно она характеризуется концентрацией водородных ионов. На практике концентрация водородных ионов выражается показателем рН.
Активная концентрация природных вод обычно варьируется в пределах рН 6,5 – 8,5, что соответствует лимитам питьевой воды.
Растворимые в воде газы – O2, CO2, H2S, СН4, N2 имеют значение для оценки ее качества; так CO2, H2S обуславливают коррозионные свойства воды по отношению к металлам и бетонам. Углекислота содержится во всех природных водах от нескольких мг/л (поверхностные воды) до сотен мг/л (подземные воды).
В заввисимости от рН воды углекислота присутствует в ней в виде свободной углекислоты (растворимая CO2), полусвязанной углекислоты HCO3– (бикарбонат-ион) и связанной CO32– (карбонат-ион).
Гидробтонты – населяющие природные воды. Они подразделяются на:
– плангтон – обитатели, пребывающие в толще воды от дна до поверхности;
– бентос – обитатели, находящиеся на дне водоема;
– нейстон – организмы, населяющие поверхностную пленку воды;
– пагон – молуски, ракообразные.
Бактерии, вирусы по типу питания разделяет на три групы:
1) аутотрофные – энергию получают при фотосинтезе;
2) гетеротрофные (сапрофиты) – для питания используют готовые органические вещества;
3) паротрофные (паразиты).
На Т. 1.8. сл. 7. показаны сроки существования отдельных микробов.
Дата добавления: 2017-05-18; просмотров: 650;
