Массовый и объемный состав продуктов сгорания
При действительном количестве воздуха, подаваемом на горение (α 1), и полном сгорании углерода в состав дымовых газов входят: СО2, SO2, H2O, N2 и О2.
Двуокись углерода образуется в результате сгорания Ср, содержащегося в топливе. Исходя из реакции (5.3), масса СО2, получаемая от сгорания одного килограмма топлива, равна:

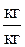
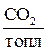 (5.14)
(5.14)
SО2 в продуктах сгорания получается от сгорания серы. Ее масса, согласно реакции (5.4), может быть определена как:
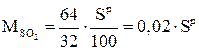
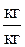
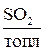 . (5.15)
. (5.15)
Водяные пары, входящие в продукты сгорания, имеют три источника: от сгорания водорода топлива; от испарения влаги, содержащейся в топливе; вносятся воздухом, подаваемым на горение.
Масса водяных паров, получившихся от сгорания водорода топлива, рассчитывается согласно уравнению (5.2), по формуле:
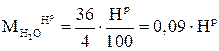
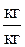
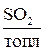 . (5.16)
. (5.16)
Количество водяных паров, поступивших в продукты сгорания от испарения влаги, содержащейся в самом топливе, будет равно:
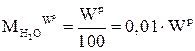
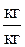
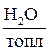 . (5.17)
. (5.17)
Наконец, масса водяных паров, вносимых с воздухом, может быть рассчитана как:

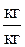
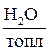 . (5.19)
. (5.19)
где 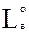 и
и 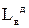 – теоретическое и действительное количество воздуха,
– теоретическое и действительное количество воздуха, 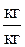
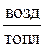 ;
;
d - влагосодержание абсолютно сухого воздуха, 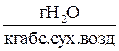 .
.
При практических расчетах влагосодержание абсолютно сухого воздуха может быть принято равным d = 0,1 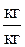
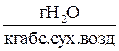 .
.
Таким образом, общее содержание водяных паров в продуктах сгорания будет равно:
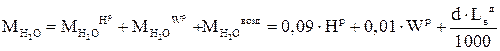
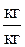
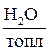 (5.20)
(5.20)
Источниками N2, входящего в состав продуктов сгорания, являются азот самого топлива и азот, вносимый с воздухом. Его общее количество может быть рассчитано по уравнению:
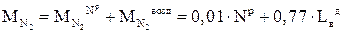
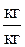
 , (5.21)
, (5.21)
где 0,77 – массовое содержание азота в воздухе, 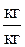
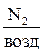 .
.
Последний компонент, входящий в состав дымовых газов, кислород, определяется по формуле:
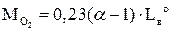
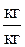
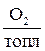 . (5.22)
. (5.22)
Дата добавления: 2017-04-20; просмотров: 1608;
