Другие кишечные гормоны
В 70-х годах было обнаружено, что многие известные гормоны желудочно-кишечного тракта, в частности гастрин и секретин, не оказывают влияния на аппетит. В отличие от них холецисгокинин вызывает сильное торможение пищевой активности. Первым, по-видимому, продемонстрировал специфическое влияние холецистокинина на потребление пищи X . Купманс с сотрудниками (Koopmans et al., 1972). В цикле исследований группы Дж. Смита (Smith et al., 1974) на крысах было показано, что холецистокиыин может вызывать торможение аппетита. Авторы, однако, оценивали этот эффект, скорее, как фармакологический, чем физиологический. У обезьян также обнаружено торможение потребления пиши после введения холецистокинина. У человека потребление пищи зависит от дозы введенного холецистокинина и от способа его введения. Так, внутривенное введение гормона в дозе 0.5 ед/кг приводит к торможению аппетита, а постепенное внутривенное введение в дозе 1 ед/кг, напротив, вызывает его стимуляцию (Stur-devant, Goetze, 1976). Прямое действие холецистокинина на центры питания и другие нервные центры показано в электрофизиологическом исследовании Н. Дафни и Е. Джекобсона (Dafny, Jacobson, 1975). Наконец, продемонстрировано, что после введения глюкагона возрастает электрическая активность центра сытости. (Более подробно эти вопросы освещены в монографии: Уголев, 1978.)
В 80-е годы интенсивная работа в этом направлении продолжалась. На человеке и животных было вновь продемонстрировано, что в передаче сигнала насыщения большую роль играют кишечные гормоны. Суммируя полученные за эти годы данные, можно ска-
зать, что экзогенный холецистокинин, в том числе его синтетический октапептид холецистокинин-8, вызывает снижение потребления пищи, которое зависит от дозы гормона и места его введения (периферического или центрального). При этом для развития эффекта насыщения необходим сульфатированный тирозин в 7-й позиции С-терминального конца цепи октапеп-тида холецистокинина. Показана также физиологическая специфичность холецистокинина: он ингибирует потребление пищи, но не воды (Smith, 1983; Gibbs, Smith, 1986, и др.).
В последние годы дискутируется вопрос о периферическом и центральном механизмах действия холецистокинина на аппетит. (Физиологический и фармакологический эффекты гормона дифференцировать достаточно трудно.)
Так как систематические инъекции холецистокинина приводят к резкому изменению пищевого поведения, то предполагается, что гормон должен прямо или опосредованно вызывать изменения функционального состояния мозговых структур. Считается, что основным путем передачи информации после введения экзогенного холецистокинина служат афферентные волокна абдоминальной вагусной системы, с рецепторами которой связывается гормон. Кроме того, гормон может связываться и с рецепторами пилорического сфинктера желудка.
Для объяснения эффекта эндогенного холецистокинина привлекается гипотеза, согласно которой освобождение этого гормона, вызывая чувство насыщения, определяет окончание акта еды, следствием чего является соответствующее поведение. По-видимому, эндогенный холецистокинин может прямо влиять на функции мозга, вызывая торможение аппетита. Принято, что основную роль в этом эффекте играют вентромедиальная и латеральная области гипоталамуса.
В последние годы продемонстрировано, что такие кишечные пептиды, как глюкагон, соматостатин и бомбезин, также вызывают торможение потребления пищи, но в меньшей мере, чем холецистокинин. В отличие от этих гормонов секретин, гастрин и ГИП не обладают таким эффектом.
Подробно история развития проблемы и ее современное состояние освещены з ряде детальных сводок (Smith, 1982, 1983, 1984; Gibbs, Smith, 1986, 1988; Murphy et al., 1988; Кассиль, 1990, и др.).
Наконец, к кишечным пептидным гормонам, ингибирующим потребление пищи, относится также сатиетин (обзор: Замбржицкий, 1989).
Следует отметить, что влияние на аппетит холе-цистокинина, глюкагона, энтерогастрона и других гормонов, по-видимому, является важной, но скорее дополнительной (а не основной) функцией. По крайней мере в некоторых случаях можно думать об их фармакологическом, а не физиологическом действии. Эти же факты давали возможность предполагать, что среди кишечных гормонов, возможно, существуют такие, которые обладают преимущественно нейротропным действием, и их аппетиттормозящие эффекты будут выражены более отчетливо, чем у известных гормонов. Действительно, нами было продемонстрировано, что арэнтерин влияет на потребление пищевых веществ более эффективно, чем холецистокинин и секретин. В частности, при внутрибрюшинном введении препарата арэнтерина в дозе 0.1 мг на 100 г. массы тела крысы наблюдается резкое торможение потребления раствора глюкозы (рис. 8.2). После введения заведомо большей дозы секретина (0.5 мг на 100 г массы тела) торможения аппетита не происходит. Введение холецистокинина также в дозе 0. 5 мг на 100 г массы тела вызывает сравнительно слабый и кратковременный эффект (рис. 8.3) (Уголев, 1978).
Итак, эндокринные клетки тонкой кишки, по-видимому, продуцируют более чем один фактор, способный понижать пищевую возбудимость. В одних случаях некоторые из этих факторов - хорошо известные гормоны, проявляющие новые стороны физиологической (или фармакологической) активности, в других случаях -это «новые» гормоны. К числу последних относится арэнтерин. Заслуживает внимания, что арэнтерин обладает большей продолжительностью действия, чем холецистокинин. В этом смысле арэнтерин вообще отличается от большинства кишечных гормонов, эффект которых непродолжителен. Это означает, что кишечная гормональная система способна не только к кратковременным, но и более продолжительным регуляторным эффектам.
Рассмотрим более обобщенно влияние желудочно-кишечных гормонов на потребление пищи. Следует различать два типа эффектов: 1) прямые (гипотала-мотропные) эффекты, в том числе арэнтерина и холецистокинина, на структуры гипоталамуса; 2) косвенные эффекты, которые, по-видимому, следует учитывать в комплексе реакций, связанных с нормальным насыщением. В частности, согласно дегидратационной теории регуляции аппетита, физиологическая дегидратация тканей, вызванная секрецией главных пищеварительных органов, служит одной из причин пони-
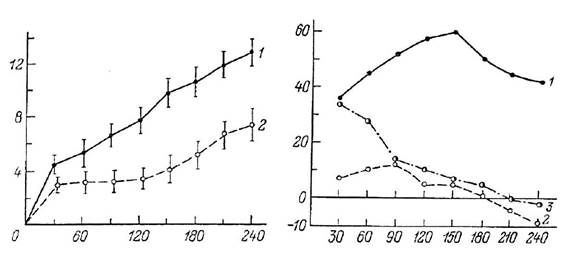
Рис. 8.2. Потребление глюкозы после внутрибрюшинного введения раствора Рингера и препарата ар-энтерина (по: Уголев, 1978).
По оси абсцисс - время после потребления глюкозы (мин); по оси ординат - количество выпитого 40%-ного раствора глюкозы (мл).
Дата добавления: 2016-03-22; просмотров: 690;
