VIII. ВИТАМИНЫ СТАЛИ
Восемьдесят лет тому назад русский ученый Н. И. Лунин поставил весьма интересный опыт. Его интересовали пищевые потребности живого организма. Подопытных животных, мышей он разделил на две группы. Одну стал кормить обыкновенным коровьим молоком, другую – молоком искусственным, то есть смесью всех тех веществ, которые входят в состав молока. Вещества эти Лунин тщательно очищал, чтобы данные опыта были как можно более точными.
Первая группа мышей жила и процветала, а во второй зверята начали болеть, слабеть и, наконец, умирать. Им не хватало какой‑то неуловимой малости, без которой они, однако, не могли существовать.
Позже физиологи установили, что этой «малостью» являются витамины. Они нужны организму в очень незначительных количествах. Если их нет, организм начинает слабеть и погибать. Но стоит добавить в пищу несколько неуловимых крупиц витаминов – и наливаются силой мускулы, загораются огнем жизни глаза, распрямляются полусогнутые спина и колени.
Влияние витаминов на живой организм подобно влиянию легирующих металлов на сталь.
Несколько процентов или даже десятых долей процента металла, который зачастую и сам‑то не обладает какими‑либо выдающимися свойствами, – и резко изменяется качество стали. Если это ванадий, сталь становится неутомимой, способной бессчетное количество раз ответить упругим противодействием на сгибающее ее постороннее усилие. Если это вольфрам, внезапно вырастает твердость стали. Марганец делает сталь неразрушимой, износостойкой. Никель сообщает ей чудесную способность сопротивляться коррозии, не ржаветь и т. д.
Примерно сто лет назад впервые начали вводить в сталь легирующие добавки, имея целью улучшить ее качество. С тех пор каких только примесей не испытали металлурги! Были среди них и такие, что понижали качество металла. Но постепенно определился и круг металлов, которые вводятся в сталь в тех или иных случаях, и пропорции этих добавок. Возникло огромное количество марок легированных сталей, обладающих широчайшим диапазоном разнообразнейших свойств.
Многие металлы свою службу человеку начали именно в качестве присадок к стали. Только потом, и в значительной степени благодаря этому применению, ближе знакомились с ними люди и находили им новые– по силам и способностям – применения. Такой, например, была судьба вольфрама – самого прочного и самого тугоплавкого металла.
Другие, честно работая на главный металл сегодняшнего дня, вместе с тем предъявляют свое право на самостоятельную роль в технике и промышленности. Таков путь по жизни соперника железа – титана.
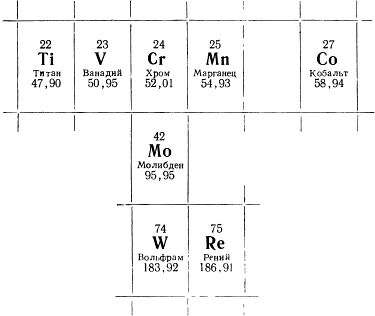
Наиболее часто применяющиеся в легированных сталях металлы в периодической системе элементов тесной группой расположились вокруг железа. В их круг входят медь, никель, кобальт – металлы, занимающие следующие за железом клетки в системе элементов. К ним относятся и марганец, хром, ванадий, титан – жильцы предшествующих железу клеток. Нельзя обойти в этом списке молибден и вольфрам, но и эти элементы тесно примыкают к основной группе. Они, правда, обитают на других «этажах» периодической системы элементов.
Рассказу о витаминах стали и посвящена эта глава книги
Горный гном
Этот металл занимает в периодической таблице элементов клетку между железом и никелем. Современное его название – кобальт. Соединения его применялись человеком еще за тысячи лет до того, как впервые этот металл удалось получить в чистом виде.
Еще в Древнем Египте и Китае соединения кобальта применялись для окраски стекол и глазурей в необыкновенно красивый и устойчивый синий цвет. Но получить чистый кобальт из руд его – а они были известны давно – обычными методами древней и средневековой металлургии не удавалось. И эти руды, внешне похожие на руды других металлов, но не дающие металла, германские мастера назвали – кобольд. Это было имя злого горного гнома. Когда в 1735 году шведскому химику Брандту удалось выделить новый чистый металл, он и назвал его по имени злого горного гнома.
В XVIII и XIX веках кобальт почти не находил себе применения, только древнее применение для окраски стекла и керамики введением окислов кобальта не было забыто. Зато XX век нашел множество применений непокорному горному гному.
Впрочем, внешность кобальта отнюдь не соответствует злому названию, которым его наградили незадачливые средневековые металлурги. В чистом виде кобальт – это приятного белого цвета, с легким красноватым оттенком металл, ковкий и тягучий. Плавится он почти при той же температуре, что и чистое железо, – при 1490 градусах, кипит при 3185 градусах.
При обычной температуре на воздухе кобальт почти не окисляется. Только при нагреве до 300 градусов начинает он покрываться легкой пленкой окисла. Но порошкообразный кобальт (его можно получить восстановлением окислов кобальта водородом) при 250 градусах уже самовоспламеняется на воздухе.
Интересным свойством кобальта является его способность растворять в себе водород. Кусок твердого кобальта может растворить в себе до 35 объемов водорода, а порошкообразный кобальт – даже до 100 объемов.
Соединения кобальта встречаются во многих медных, никелевых и марганцевых рудах. Кобальт получают из шлаков, штейнов или огарков после переработки этих руд в качестве побочного продукта. Обычно кобальт выщелачивают из этих отходов подкисленной водой. Дальнейшее отделение кобальта от сопутствующих металлов – сложный и хлопотливый процесс.
Производство кобальта растет, хотя и не так быстро, как некоторых других металлов. Если в 1900 году во всем мире было получено всего 354 тонны этого металла, то в 1947 году мировое производство кобальта составило (без СССР) 6200 тонн.
Сплавы кобальта обладают разнообразными удивительными свойствами. Это и определяет их применение.
Сплав 35 процентов кобальта с 50 процентами железа и рядом других добавок обладает максимальной из всех известных материалов намагничиваемостью.
Сплав кобальта с платиной после соответствующей термообработки имеет огромную коэрцитивную силу – его очень трудно размагнитить.
Известны и другие сплавы кобальта, обладающие особенными магнитными свойствами и идущие для изготовления постоянных магнитов и деталей электрооборудования. Широко известные магнико и альнико – это тоже представители семейства кобальтовых сплавов.
Другая важная группа этого семейства – жаропрочные и жароупорные сплавы. Представителем их может служить распространенный сплав виталлий. В его состав входят 65 процентов кобальта, 28 процентов хрома, 6 процентов молибдена, кроме того, доли процента углерода, железа и никеля. Этот сплав может длительно работать при температуре до 800 градусов, а при несколько более низких напряжениях – и при 900 градусах.
Из этого сплава изготавливают лопатки турбокомпрессоров и газовых турбин, детали реактивных двигателей и паровых котлов высоких параметров. Инженеры с удовольствием применяют этот сплав, и, если бы не высокая цена кобальта, он нашел бы еще более широкое распространение.
Жаропрочные сплавы кобальта применяются и в качестве связующих добавок при изготовлении твердых сплавов методом порошковой металлургии.
В качестве легирующей добавки кобальт входит в состав ряда сталей. Однако для того, чтобы проявилось облагораживающее влияние кобальта, его содержание в металле должно быть достаточно большим, обычно в пределах 5–10 процентов, но нередко и до 20 процентов. Это очень ограничивает применение кобальтовых сталей. И все же применяются быстрорежущие стали, содержащие до 10 процентов кобальта. Известны и магнитные стали, и жаропрочные стали, содержащие кобальт. Но еще шире используются соединения кобальта.
Прекрасные голубые и фиолетовые краски, применяющиеся для росписи фарфора, глазурей, эмалей, прекрасно растворяющиеся в стекле, – это соединения кобальта. Фиолетовые, желтые, зеленые краски, применяемые в разных производствах, – это тоже дети кобальта.
Хлористый кобальт обладает редким свойством изменять свой цвет под влиянием температуры и влажности. Так называемые симпатические чернила – это и есть раствор хлористого кобальта. Напишите им слово, дайте чернилам высохнуть, и на бумаге не останется и следа написанного. Но подержите листок над огнем, и ярко‑синие буквы выступят на нем.
Покрасьте хлористым кобальтом льняную рубашку – в сухую погоду она будет голубой. Но стоит сгуститься тучам, пройти дождю, и хотя на нее не упадет ни одна капля, она станет розовой.
Соли кобальта применяются в качестве катализаторов некоторых химических реакций. Находят они себе применение и в медицине и в фотографии.
Интересны кобальтовые удобрения. Их внесение в почву не повышает урожая, но количество кобальта в растениях, выросших на земле, в которую внесены эти удобрения, резко возрастает. А ведь при недостатке кобальта в пище резко падает продуктивность сельскохозяйственных животных – коров, овец, коз. Впрочем, иногда солями кобальта непосредственно «удобряют» пищу животных.
Но, конечно, еще не все свои свойства раскрыл кобальт людям. И множество его применений просто еще ждет своих открывателей.
Дата добавления: 2016-01-29; просмотров: 2210;
