Электрокардиограмма 4 страница
К этим симптомам вскоре присоединяется одышка, возникающая, как правило, при физической нагрузке. В покое ощущение нехватки воздуха выражено слабо. Как было сказано выше, причиной возникновения одышки являются не столько застойные явления в легких, которые в целом не характерны для констриктивного перикардита, сколько снижение объема крови, поступающей в легочную артерию, что приводит к изменению перфузионно-вентиляционных соотношений в легких и нарушению газового состава крови. По понятным причинам эти явления усугубляются на фоне физической нагрузки, что связано, главным образом, с развивающейся тахикардией, выраженным укорочением диастолы и критическим уменьшением диастолического наполнения желудочков и сердечного выброса.
Характерно, что в отличие от сердечной недостаточности, одышка при констриктивном перикардите, как правило, не нарастает в горизонтальном положении больного, т.е. отсутствуют признаки ортопноэ. Важно отметить, что приступы сердечной астмы и отек легких практически не встречаются при констриктивном перикардите.
Повышение венозного давления и связанный с этим застой крови в венозном русле большого круга кровообращения сопровождаются жалобами на увеличение живота в объеме (асцит), чувство тяжести в правом подреберье (гепатомегалия). Позже появляются отеки на ногах. Диспепсические явления (анорексия и др.), а также снижение массы тела объясняются, прежде всего, нарушением функции печени.
Осмотр и исследование органов брюшной полости и легких
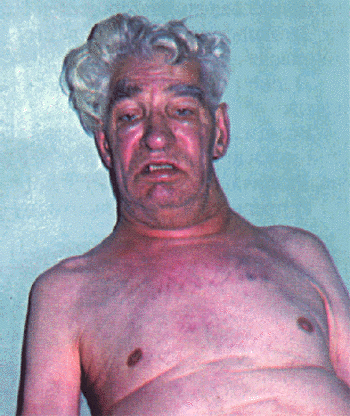
В далеко зашедших случаях заболевания обращают на себя внимание выраженное похудание больного и цианоз. При значительном сдавлении устья верхней полой вены лицо становится одутловатым, шея выглядит утолщенной, отечной, кожа лица и шеи приобретает выраженную цианотическую окраску, вены шеи набухшие. Отек и цианоз распространяются на голову и плечи (рис. 12.21, см. цветную вклейку). Такой симптомокомплекс, получивший название “воротник Стокса”, свидетельствует о существенном нарушении кровотока по верхней полой вене и встречается не только при констриктивном перикардите, но и при других заболеваниях, сопровождающихся сдавлением вены, например, при раке легкого или опухоли средостения и т.п.
|
| Рис. 12.21. Внешний вид больного с механическим препятствием кровотоку в верхней полой вене ("воротник Стокса") |
Несмотря на одышку, усиливающуюся при физической нагрузке, больные обычно занимают горизонтальное положение в постели, лежат низко, без подголовника, хотя при этом резко усиливаются цианоз и одутловатость лица. Это отличает больных с констриктивным перикардитом от пациентов с бивентрикулярной недостаточностью, которые, как известно, стремятся занять вертикальное положение (ортопноэ).
Самый характерный и постоянный внешний признак констриктивного перикардита, выявляемый при объективном исследовании, — это выраженный асцит и гепатомегалия, являющиеся следствием надпеченочной портальной гипертензии. Последняя развивается не только в результате повышения ЦВД, но и вследствие сдавления печеночных вен у места их прохождения через париетальный листок сердечной сумки. Печень увеличена значительно, особенно ее левая доля. Печень плотная, болезненная при пальпации. К другим проявлениям портальной гипертензии относятся развитие венозных коллатералей (портокавальных анастомозов) на передней брюшной стенке и спленомегалия.
Следует подчеркнуть, что асцит и выраженная гепатомегалия обычно предшествуют появлению отеков на ногах, что также является очень характерным признаком констриктивного перикардита. Часто именно эти два симптома (асцит и гепатомегалия) преобладают в клинической картине заболевания, напоминая клинические проявления цирроза печени (“псевдоцирроз” Пика).
Так же как и при тампонаде сердца, несмотря на значительные гемодинамические нарушения и наличие одышки, признаков застойных явлений в легких у больных констриктивным перикардитом выявить, как правило, не удается.
Исследование сердца и сосудов
Важными признаками констриктивного перикардита являются расширение и набухание шейных вен,сохраняющиеся даже после интенсивной терапии диуретиками. При этом, в отличие от случаев тампонады сердца, хорошо заметна пульсация вен,в частности, их диастолический коллапс (симптом Фридрейха), что отражает характерную для констриктивного перикардита форму кривой давления в ПП и югулярных венах, в частности, очень крутую и глубокую волну Y (“Y–коллапс”), механизм возникновения которой был описан выше (см. рис. 12.19).
Констриктивный перикардит, пожалуй, единственное заболевание, при котором ЦВД достигает столь высоких значений (200–300 см. вод. ст.). Причем венозное давление и, соответственно, набухание шейных вен заметно увеличиваются на вдохе (симптом Куссмауля). Известно, что во время вдоха развивается отрицательное внутриплевральное давление, что приводит к увеличению притока крови к правому сердцу. В норме это сопровождается некоторым спадением вен, поскольку кровь более интенсивно заполняет ПП и ПЖ, обладающие нормальной сократимостью и диастолическим тонусом. При констриктивном перикардите объем диастолического наполнения строго лимитирован перикардиальным рубцом, окружающим сердце. Поэтому усиление венозного притока крови к крупным венам не сопровождается более активным расслаблением камер сердца, и венозное давление еще больше возрастает на вдохе.
При пальпации сердца верхушечный толчок, как правило, обнаружить не удается, отсутствует и эпигастральная пульсация. При глубоком вдохе иногда может определяться необычное систолическое западение или втяжение нижней части грудины и межреберных промежутков. Этот феномен указывает на наличие спаек между наружным листком перикарда и передней стенкой грудной клетки и диафрагмой.
Границы сердца в большинстве случаев не расширены. Интересно, что при перемене положения тела (например, при повороте больного на левый бок), границы сердца не смещаются, поскольку неподвижный рубцовый панцирь, в который заключено сердце, фиксирован к средостению.
При аускультации I и II тоны глухие. Часто определяется трехчленный ритм (ритм галопа), образованный дополнительным патологическим III тоном, который определяется в самом начале диастолы (см. рис. 12.19, а и 12.20, а). Это так называемый “перикард-тон” или “тон броска”. Он возникает в результате внезапной остановки диастолического потока крови из предсердий в желудочки, обусловленной наличием рубцово измененного и ригидного перикарда. Перикард-тон обычно отличается большой интенсивностью.
Систолическое и пульсовое АД обычно понижены. В отличие от тампонады сердца, парадоксальный пульс при констриктивном перикардите встречается достаточно редко (не более чем в 20–25% случаев).
Электрокардиограмма
На ЭКГ в типичных случаях выявляется триада признаков:
- низкий вольтаж комплекса QRS;
- отрицательные и двухфазные зубцы Т во всех стандартных и грудных отведениях;
- расширенный высокий зубец Р или фибрилляция предсердий.
Мерцательная аритмия встречается у 1/3 больных констриктивным перикардитом. Если имеется вовлечение в патологический процесс миокарда желудочков или АВ-борозды, на ЭКГ могут появляться признаки внутрижелудочковых или атриовентрикулярных блокад.
Рентгенологическое исследование
При рентгенологическом исследовании обычно обнаруживается ряд важных диагностических признаков:
- относительно маленькое или нормальное сердце (точнее, желудочки) при одновременном увеличении размеров предсердий;
- отсутствие “талии” сердца и дифференциации дуг в связи с характерным выпрямлением контуров сердца;
- неровность контуров сердца в связи с наличием многочисленных сращений перикарда;
- обызвествление перикарда, обнаруживаемое примерно у 1/3 больных констриктивным перикардитом.
Катетеризация
На кривой давления в ПП определяются отрицательная Х-волна и особенно глубокая и крутая отрицательная Y–волна (“Y–коллапс”), отражающая быстрое, но кратковременное движение крови из предсердий в желудочки в самую раннюю фазу диастолы. Одновременно на кривой давления в желудочке определяется феномен “диастолического заполнения и плато”,т.е. кривая давления имеет вид квадратного корня (см. рис. 12.20, а).
Важным признаком является повышение давления в ПП и выравнивание диастолического давления в ПП, ПЖ, легочной артерии, а также давления заклинивания легочной артерии (ДЗЛА). Обычно разница между величинами диастолического давления в этих камерах сердца не превышает 5 мм рт. ст. Характерно, что при констриктивном перикардите среднее давление в ПП не снижается на вдохе.
При изучении систолической функции ЛЖ обращает на себя внимание снижение величины УО при сохраненной ФВ. Сердечный выброс (МО) обычно нормальный за счет высокой частоты сердечных сокращений (ЧСС).
Югулярная флебограмма
В отличие от больных с тампонадой сердца, при констриктивном перикардите на югулярной флебограмме выявляется глубокая отрицательная Y–волна (“Y–коллапс”), отражающая быстрое, но кратковременное наполнение ПЖ во время фазы быстрого наполнения желудочка (см. рис. 12.19, а), механизм которого описан выше.
Эхокардиографическое исследование
Эхокардиографическое исследование позволяет не только выявить морфологические изменения перикарда, характерные для констриктивного перикардита, но и количественно оценить гемодинамические изменения, обусловленные сдавлением сердца. В типичных случаях у больных констриктивным перикардитом при эхокардиографическом исследовании выявляются следующие признаки:
1. Утолщение, значительное уплотнение и сращение листков перикарда. Эхонегативное пространство между листками заполнено негомогенной слоистой массой, менее эхоплотной, чем сам перикард. Эта слоистая масса как бы склеивает оба листка перикарда (адгезия), поэтому во время сердечного цикла наблюдается одинаковое параллельное переднезаднее движение листков перикарда и эпикарда.
2. Отсутствие движения миокарда ЛЖ после короткого раннего диастолического наполнения. Этот признак соответствует глубокой Y–волне на югулярной флебограмме или кривой давления в ПП.
3. Нормальные или уменьшенные размеры желудочков и умеренная дилатация предсердий.
4. Недостаточное коллабирование нижней полой вены (менее 50%) после глубокого вдоха, свидетельствующее о высоком венозном давлении.
| 12.4. Лечение перикардитов |

|
Выбор наиболее адекватного способа лечения острого перикардита зависит от клинико-морфологической формы заболевания и его этиологии.
Острый сухой (фибринозный) перикардит
Впервые выявленный острый перикардит требует госпитализации больного и ограничения физической активности. Необходимо регулярно контролировать уровни артериального и венозного давлений и ЧСС. Показаны также повторные эхокардиографические исследования с целью своевременной диагностики формирования выпота в полости перикарда.
В большинстве случаев ограничиваются назначением нестероидных противовоспалительных лекарственных средств (НПВС):
- диклофенак (вольтарен) — 100–200 мг в сутки;
- индометацин — 25–50 мг каждые 6–8 ч;
- ибупрофен — 400–800 мг;
- мовалис — 7,5–15 мг 2 раза в сутки.
Глюкокортикоиды целесообразно назначать только в следующих клинических ситуациях:
- при интенсивном болевом синдроме, не поддающемся лечению НПВС;
- при тяжелом течении диффузных заболеваний соединительной ткани (системная красная волчанка, ревматоидный артрит, полимиозит и др.), осложненных острым перикардитом;
- при аллергическом лекарственном перикардите;
- при аутоиммунных острых перикардитах.
Суточные дозы и длительность приема глюкокортикоидов подбираются в зависимости от этиологии и характера перикардита и основного заболевания. При интенсивном болевом синдроме, например, глюкокортикоиды назначают в суточной дозе 40–60 мг в течение 5–7 дней с последующим снижением дозы и отменой препарата (подробнее о тактике лечения глюкокортикоидами — см. последующие главы руководства).
При вирусном (идиопатическом) перикардите рекомендуют воздерживаться от применения глюкокортикоидов (M. Freed, J.D. Band).
Антибиотики при сухом (фибринозном) перикардите назначают только в тех случаях, когда воспаление сердечной сорочки возникает на фоне явной бактериальной инфекции — сепсиса, инфекционного эндокардита, пневмонии, наличия гнойного очага и т.д. В зависимости от установленного или предполагаемого возбудителя этих патологических процессов назначают антибиотики пенициллинового ряда (оксациллин, ампициллин, аугментин и др.), цефалоспорины, современные макролиды (сумамед и др.), фторхинолоновые производные (ципрофлоксацин, офлоксацин и др.). Основные принципы и тактика лечения антибиотиками подробно изложены в последующих главах руководства.
При туберкулезном перикардите назначают комбинированную противотуберкулезную терапию, например, изониазид, рифампицин, пиразинамид и другие в сочетании с глюкокортикоидами. В этих случаях специфическое лечение назначается и проводится под контролем фтизиатра.
В остальных случаях от применения антибиотиков следует воздержаться в связи с возможными побочными, в том числе аллергическими, реакциями, способными только осложнить течение перикардита.
Острый экссудативный перикардит без тампонады сердца
Тактика лечения острых выпотных перикардитов без сдавления сердца в основном та же, что и сухих перикардитов различного генеза. При этом требуется особенно строгий и регулярный контроль (в том числе и эхокардиографический) за основными гемодинамическими показателями (АД, ЦВД, ЧСС, УИ, СИ, и т.д.), объемом экссудата и признаками, указывающими на развитие тампонады сердца.
Лечение включает обычно назначение постельного режима и НПВС. Антибиотики используют, как правило, при экссудативных перикардитах, развившихся на фоне бактериальной инфекции или при гнойных перикардитах.
Возможно также назначение глюкокортикоидов, в большинстве случаев способствующих более быстрому рассасыванию выпота, особенно в случаях аллергических, аутоиммунных перикардитов и перикардитов, развившихся на фоне диффузных заболеваний соединительной ткани.
При установленном или предполагаемом гнойном перикардите, помимо парентерального введения антибиотиков, показана пункция перикарда (см. выше), максимальное удаление гнойного экссудата, промывание полости перикарда раствором фурациллина или антибиотиков и повторное введение антибиотиков через катетер.
Пункция перикарда показана также при затягивающемся рассасывании экссудата (более двух недель лечения) и необходимости уточнения его природы и характера (например, для выявления специфической туберкулезной, грибковой, опухолевой и другой этиологии заболевания). В этих случаях результаты пункции помогают выбрать более адекватную тактику ведения больных.
Тампонада сердца
Тампонада сердца, развившаяся в результате выпотного перикардита, как правило, требует проведения неотложного перикардиоцентеза. Предварительно для стабилизации гемодинамики внутривенно капельно вводят 300–500 мл плазмы, коллоидных растворов или 0,9% раствора натрия хлорида, а также инотропные средства (дигоксин, добутамин). Это позволяет восстановить уровень системного АД и ударный объем и подготовить больного к проведению перикардиоцентеза.
Констриктивный перикардит
Единственным радикальным способом лечения констриктивного перикардита является субтотальная перикардэктомия — резекция перикарда. При этом сердце освобождается от сдавливающей капсулы, вначале в области левого, а затем — правого желудочка. Обратная последовательность приводит, как правило, к развитию отека легких.
Во время подготовки к операции назначают диуретики, ограничивают потребление соли, обеспечивают соблюдение постельного режима. С осторожностью назначают сердечные гликозиды, которые уменьшают риск развития сердечной недостаточности после проведения операции, следствием которой является значительное и внезапное увеличение преднагрузки на правый и левый желудочки.
В большинстве случаев (около 90%) в течение 3–4 месяцев после операции наступает улучшение состояния больных, хотя операционная летальность достигает 10%. После операции необходимо тщательное наблюдение за больным, перенесшим операцию перикардэктомии, и при необходимости — лечение диуретиками, ингибиторами АПФ и, с осторожностью, сердечными гликозидами. При туберкулезном или гнойном констриктивном перикардите после операции показано длительное лечение антибиотиками или противотуберкулезными препаратами.
 Запомните
1. Основные принципы лечения больных с острым (сухим или экссудативным) перикардитом формулируются следующим образом: Запомните
1. Основные принципы лечения больных с острым (сухим или экссудативным) перикардитом формулируются следующим образом:
| ||
| 12.5. Прогноз | ||

| ||
В большинстве случаев прогноз сухого (фибринозного) перикардита вполне благоприятный. На фоне адекватно назначенной терапии происходит быстрое уменьшение признаков воспаления. У части больных перикардит характеризуется затяжным или рецидивирующим течением. Наконец, примерно в 1/4 случаев возможна трансформация сухого (фибринозного) перикардита в выпотной (экссудативный) и даже (редко) в констриктивный (сдавливающий) перикардит.
При остром экссудативном перикардите в большинстве случаев выздоровление наступает через 2–6 недель. Тампонада сердца развивается примерно у 15% больных с острым перикардитом, а исход в констриктивный перикардит наблюдается у 10% больных. Еще в 10–20% случаев происходит рецидивирование перикардита. Нередко прогноз определяется характером, тяжестью и адекватностью терапии основного заболевания, осложнившегося перикардитом (ревматические болезни, туберкулез, опухоли, уремия и т.д.).
Отдаленный прогноз констриктивного перикардитазависит от эффективности оперативного вмешательства (перикардэктомии). В большинстве случаев успешно проведенная операция обеспечивает высокую выживаемость и качество жизни больных. При отсутствии оперативного лечения прогноз неблагоприятный.
| Глава 13. Хроническое легочное сердце |

|
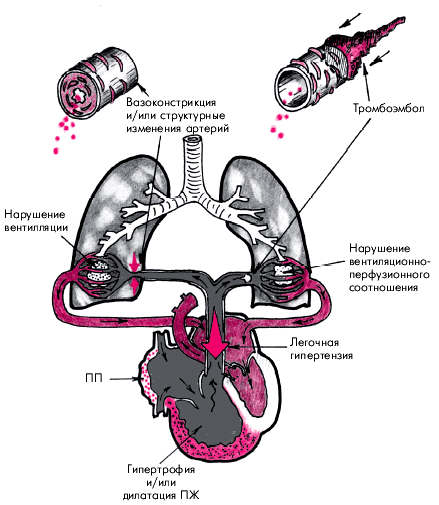
Легочным сердцем (ЛС) называют вторичное увеличение ПЖ (его гипертрофию и/или дилатацию), которое обусловлено легочной артериальной гипертензией, развившейся в результате заболеваний, нарушающих функцию легких, т.е. ведущих к развитию дыхательной недостаточности (рис. 13.1). Легочное сердце развивается не только вследствие заболеваний паренхимы легких, воздухоносных путей или сосудов легких, но и в результате поражения скелета и нервно-мышечного аппарата грудной клетки, а также нарушений центральной регуляции дыхания (E.H. Амосова). Следует помнить, что к понятию “легочное сердце” не относится увеличение ПЖ, вызванное нарушениями функции и структуры легких, которые обусловлены первичным поражением левых отделов сердца (например, стенозом левого атриовентрикулярного отверстия, постинфарктным кардиосклерозом и т.д.) или врожденными пороками сердца.
|
| Рис. 13.1. Схема изменений ПЖ и ПП при хроническом легочном сердце, обусловленном нарушением альвеолярной вентиляции и вентиляционно-перфузионных соотношений. Объяснение в тексте |
Сведения об истинной распространенности ЛС весьма противоречивы, поскольку диагностика этого патологического синдрома затруднена, особенно в тех случаях, когда отсутствуют признаки правожелудочковой недостаточности. По некоторым сведениям, на долю ЛС приходится примерно 5–10% всех случаев сердечно-сосудистых заболеваний у взрослых. Однако есть основания считать, что ЛС относится к более распространенной патологии, особенно среди мужчин в возрасте старше 50 лет, и по частоте занимает 3-е место после ИБС и АГ (А.Р. Fishman).
| 13.1. Этиология |

|
В табл. 13.1 представлены наиболее частые причины легочного сердца. Различают острое и хроническое ЛС.
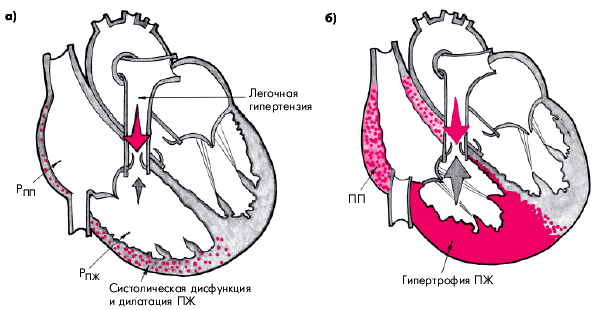
Острое легочное сердце развивается в течение нескольких часов или дней в результате внезапного и значительного повышения давления в легочной артерии и практически во всех случаях сопровождается острой правожелудочковой недостаточностью (без предшествующей гипертрофии ПЖ) (рис. 13.2, а). Наиболее частой причиной острого ЛС является тромбоэмболия ветвей легочной артерии (подробнее — см. главу 14).
Хроническое легочное сердце характеризуется постепенным и медленным (в течение нескольких лет) формированием легочной артериальной гипертензии и развитием гипертрофии ПЖ (компенсированное хроническое ЛС) (рис. 13.2, б). В дальнейшем по мере повышения давления в легочной артерии развивается систолическая дисфункция ПЖ и появляются признаки правожелудочковой недостаточности (декомпенсированное хроническое ЛС).
Существует множество причин, ведущих к формированию хронического ЛС (см. табл. 13.1). Чаще всего это различные бронхолегочные заболевания, протекающие с выраженным нарушением структуры легочной ткани и/или альвеолярной гипоксией (хронический обструктивный бронхит, бронхоэктазы, фиброз легочной ткани, обусловленный хроническими патологическими процессами в легочной паренхиме и др.).
|
| Рис. 13.2. Схематическое изображение морфологических изменений при остром (а) и хроническом (б) легочном сердце |
Таблица 13.1
Основные причины легочного сердца
| Варианты легочного сердца | Основные причины легочного сердца | |
| Острое ЛС | 1. Тромбоэмболия ветвей легочной артерии 2. Клапанный пневмоторакс 3. Массивные плевриты 4. Астматический статус | |
| Хроническое ЛС | 1. Заболевания паренхимы легких · Пневмосклерозы · Фиброз легких вследствие туберкулеза · Фиброз легких вследствие пневмокониозов · Фиброзирующий альвеолит · Хронические пневмониты и фиброз легких при диффузных заболеваниях соединительной ткани · Врожденные заболевания паренхимы легких (муковисцидоз, поликистоз, гипоплазия легких и др.) · Гранулематозные заболевания с поражением легких (саркоидоз и др.) · Состояние после резекции легких | |
| 2. Заболевания воздухоносных путей · Хронический обструктивный бронхит · Бронхоэктазы · Бронхиальная астма · Хроническая обструктивная эмфизема легких · Стеноз трахеи · Синдром обструктивного ночного апноэ · Врожденные аномалии ротоглотки | ||
| 3. Поражение легочного сосудистого русла · Рецидивирующие тромбоэмболии и тромбозы мелких ветвей легочной артерии · Васкулиты при диффузных заболеваниях соединительной ткани (узелковый периартериит и др.) · Первичная легочная гипертензия | ||
| 4. Торакодиафрагмальные заболевания · Кифосколиоз · Нейро-мышечные заболевания (полиомиелит, миастения, миопатии и мышечные дистрофии) · Обширные плевральные спайки (шварты) и фиброторакс | ||
| 5. Нарушения функции дыхательного центра · Идиопатическая альвеолярная гиповентиляция · Синдром ночного апноэ центрального происхождения · Длительное пребывание в высокогорной местности · Ожирение (синдром Пиквика) | ||
Частыми причинами хронического ЛС, по-видимому, являются рецидивирующие тромбоэмболии мелких ветвей легочной артерии, клинические проявления которых в некоторых случаях могут быть очень скудными.
Наконец, хроническое ЛС может явиться следствием выраженных деформаций грудной клетки (например, кифосколиоза) или даже нарушений центральной регуляции дыхания (синдром ночного апноэ).
 Запомните
1. Тромбоэмболия крупных ветвей легочной артерии является основной причиной быстрого (в течение нескольких часов или дней) развития острого легочного сердца, которое проявляется, в первую очередь, клиническими признаками острой правожелудочковой недостаточности.
2. Основными причинами хронического легочного сердца являются: Запомните
1. Тромбоэмболия крупных ветвей легочной артерии является основной причиной быстрого (в течение нескольких часов или дней) развития острого легочного сердца, которое проявляется, в первую очередь, клиническими признаками острой правожелудочковой недостаточности.
2. Основными причинами хронического легочного сердца являются:
|
13.2. Патогенез
| 13.2.1. Механизмы легочной артериальной гипертензии |

|
В основе развития хронического ЛС лежит постепенное формирование легочной артериальной гипертензии, обусловленной несколькими патогенетическими механизмами. Хотя значение каждого из них различно в зависимости от этиологии легочной гипертензии, все же главным звеном ее патогенеза в большинстве случаев является альвеолярная гипоксия, возникающая в условиях нарастающей неравномерности альвеолярной вентиляции.
1. Гипоксическая легочная вазоконстрикция. В нормально функционирующем легком существует достаточно сложный механизм регуляции местного кровотока, зависящего в первую очередь от парциального давления кислорода в альвеолярном воздухе. Этот механизм известен под названием рефлекса Эйлера–Лильестранда. Если в физиологических условиях в относительно небольшом участке легкого происходит снижение парциального давления кислорода в альвеолярном воздухе, то в этом же участке рефлекторно возникает местная вазоконстрикция, которая приводит к адекватному ограничению кровотока (рис. 13.3, б). В результате местный легочный кровоток как бы приспосабливается к интенсивности легочной вентиляции, и нарушений вентиляционно-перфузионных соотношений не происходит.
Если альвеолярная гиповентиляция выражена в большей степени и распространяется на обширные участки легочной ткани (например, при выраженном фиброзе легких или обструктивных заболеваниях легких и т.д.), развивается генерализованное повышение тонуса легочных артериол, ведущее к повышению общего легочного сосудистого сопротивления и легочной гипертензии (рис. 13.3, в).
Механизм гипоксической легочной вазоконстрикции до конца не ясен. Вероятно, он реализуется при участии САС, а также вазоконстрикторных эндотелиальных факторов. Эндотелины и ангиотензин II прямо стимулируют сокращение гладкой мускулатуры сосудистой стенки, тогда как снижение синтеза простагландина PGI2, эндотелиального расслабляющего фактора (NO) еще больше усиливает эти вазоконстрикторные влияния.
Дата добавления: 2016-01-20; просмотров: 2611;
