Хімічна енергія поверхневого шару
Надлишкова поверхнева енергія визначає також хімічну активність поверхні твердого тіла. Тому поверхня твердих тіл при нормальних умовах ніколи не буває чистою; вона завжди покрита різноманітними поверхневими плівками: продуктами корозії, адсорбованими газовими і водяними плівками, адсорбованими вуглеводнями. Більшість металів активно вступають у реакцію з окислювачами, що містяться в атмосфері, у першу чергу з киснем і сіркою. При цьому швидкість окислювання сильно залежить від умов у який знаходиться метал. Відомо, що в сухому чистому повітрі залізо не іржавіє століттями. Приклад тому - знаменита залізна колона в Індії, що не іржавіє з моменту свого створення ( 310 р. н.е.) завдяки низькій вологості і відсутності промислових забруднень. У той же час в атмосфері сучасного міста залізо іржавіє дуже швидко.
Одержати чисту поверхню твердого тіла надзвичайно складно. Так, навіть у вакуумі при тиску 10-6 мм. рт. ст. поверхня твердого тіла покривається моношаром адсорбованого газу приблизно за 1 с. При тиску 10-10 мм. рт. ст. цей час складає усього декілька годин, а при атмосферному тиску – соті частки секунди.
Оксидні плівки утворені на поверхні металу можуть мати захисну дію. Після того, як на металах утвориться плівка деякої товщини, подальший ріст її практично припиняється. Так відбувається, якщо оксид займає більший обсяг, чим об’єм металу, з якого він утворився. У цьому випадку плівка, що утвориться, - щільна, в ній формуються напруження стиску. З ростом товщини такої плівки дифузія іонів металу на поверхню або атомів кисню усередину оксиду утруднюється. Тому швидкість окислювання можна вважати обернено пропорційною товщині плівки d:
 (2.1)
(2.1)
де kn-константа.
Інтегрування рівняння (1.1) приводить до так званого параболічного закону росту товщини плівки:
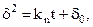 (2.2)
(2.2)
де d0-початкова товщина.
Якщо об’єм окислу менший об’єму металу, з якого окисел утвориться, то окисна плівка пориста і не має захисної дії. У цьому випадку швидкість окислювання не залежить від товщини плівки
 (2.3)
(2.3)
і закон її росту лінійний:
 (2.4)
(2.4)
Поряд із параболічним (2.2) і лінійним (2.4) законами окислювання часто зустрічається логарифмічний закон, особливо при низьких температурах:
 (2.5)
(2.5)
Лінійному закону (2.4) підпорядковується окислювання легких металів: Na, Ca, Mg. Параболічному, закону (2.2) - високотемпературне (Т >300 С) окислювання більшості металів: Cu, Fe, Al, Pb, Ti, V, Mo, W. Низькотемпературне окислювання більшості металів підпорядковується логарифмічному закону (2.5).
Відзначимо, що в монокристалів швидкість окислювання і товщина плівки окислу залежить від напрямку, по якому вирізаний монокристал. Константа kn у рівнянні швидкості окислювання (2.2) экспоненціально залежить від температури через дифузійний механізм окислювання.
Крім кисню, сильний хімічний вплив на властивості поверхні металів має водень. При певних умовах (високий тиск водню і температура 200…6000С) створюються сприятливі термодинамічні умови реакції дисоціації цементиту і обезвуглецювання сталі
Fe3C+2H2+3Fe+CH4. ( 2.6)
Цей процес проходить із зменшенням об’єму, що призводить до виникнення додаткових напружень по границях зерен. Обезвуглецювання суттєво змінює властивості поверхневого шару. Товщина цього шару зменшується із збільшенням відсоткового вмісту вуглецю у сплаві. Так, при вмісті вуглецю в 1% - товщина шару, де ще спостерігається цей процес, досягала величини 1,5 мм, а при вмісті вуглецю в 4% вона зменшується до 1 мм.
Крім плівок окислів на поверхні твердих тіл можуть утворюватися сульфідні, водяні плівки (товщиною до 100 нм), полімерні плівки. Останні утворяться в результаті адсорбції на поверхні твердих тіл парів масел або інших органічних сполук і їхньої наступної полімеризації. Метал часто відіграє роль каталізатора в реакції полімеризації. Ці плівки мають високу міцність.
Поверхневі плівки відіграють значну роль при терті. Основний вплив їх на процеси тертя полягає в тому, що вони перешкоджають утворенню міцних металевих зв'язків, замінюючи їх набагато більш слабкими ван-дер-ваальсовими (таблиця 2.2).
Оскільки на поверхні будь-якого твердого тіла практично завжди знаходяться різноманітного роду плівки, склад і властивості яких залежать від зовнішніх умов варто обережно відносити до наведених у довідниках "універсальних" значень коефіцієнта тертя "сталі по сталі", "бронзи по чавуні" і т.п.
Поверхневі плівки можуть руйнуватися при терті або пластичній деформації, оголюючи чистину поверхню металів. Руйнуванню плівок сприяє та обставина, що захисні плівки , що утворяться, знаходяться в напруженому (стиснутому) стані, тому що Vок>Vмет , і легко розтріскуються; крім того, твердість окислів, як правило, більша твердості металів. Нарешті, якщо швидкість окислювання менше швидкості, стирання плівки, то при терті плівка не встигає наростати і не ізолює поверхні, що труться.
Дослідження механізму взаємодії мастильних матеріалів з металами деталей в процесі тертя привело до відкриття так званого ефекту трибополімеризації. Цей ефект полягає в тому, що в процесі тертя металевих поверхонь в присутності вуглеводневого мастильного матеріалу спостерігається утворення аморфних високомолекулярних продуктів, які були названі полімерами тертя.
Полімерні плівки, які утворюються на поверхнях тертя, забезпечують протизадирні і протизношувальні властивості матеріалів.
Продукти трибополімеризації – полімери тертя – забезпечують поверхневим шарам позитивний градієнт механічних властивостей, що, в свою чергу, викликає різке зниження інтенсивності зношування деталей спряження. В якості мастильних матеріалів, які створюють умови виникнення ефекту трибополімеризації, застосовують масла і окремі їх фракції, індивідуальні вуглеводні (цетан) і інші органічні сполуки.
Дата добавления: 2015-10-19; просмотров: 964;
