Химические цепи.
Состоят из двух электродов, причем один из них обратим относительно катиона (электрод I рода), а другой относительно аниона.
Примером химической реакции являются различные аккумуляторы – накопители электрической энергии в виде химической. Они могут быть щелочными и кислотными.
Рассмотрим кислотный свинцовый аккумулятор:
Отрицательным полюсом (анодом) служит свинцовый электрод. Положительным полюсом (катодом) является электрод из диоксида свинца (PbO2), который в виде пасты заполняет ячейки свинцовой решетки. В качестве электролита используют 25 – 30% р-р серной кислоты.
(-) Pb, PbSO4
Сульфат свинцовый эл-д обратимый, относит. аниона SO4 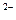
| H2SO4 25÷30 % | PbO2, Pb (+)
Свинцовоокисный H3O 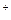 кислоты кислоты
|
Аккумуляторы – гальванические элементы, допускающие многоразовое использование.
Токообразующие вещества в аккумуляторах могут образовываться при пропускании через аккумулятор постоянного электрического тока от другого источника. Процесс регенерации активных веществ называют зарядом аккумулятора.
Дата добавления: 2015-09-07; просмотров: 711;
