ТИПЫ СВЯЗЕЙ МЕЖДУ АМИНОКИСЛОТАМИ В МОЛЕКУЛЕ БЕЛКА
2 группы:
1.КОВАЛЕНТНЫЕ СВЯЗИ - обычные прочные химические связи.
а) пептидная связь
б) дисульфидная связь
2.НЕКОВАЛЕНТНЫЕ (СЛАБЫЕ) ТИПЫ СВЯЗЕЙ: а) Водородная связь; б) ионная связь; в) Гидрофобное взаимодействие
ПЕПТИДНАЯ СВЯЗЬ.
Формируется за счет COOH-группы одной аминокислоты и NH2-группы соседней аминокислоты. В названии пептида окончания названий всех аминокислот, кроме последней, находящейся на «С»-конце молекулы меняются на «ил». Например, тетрапептид: валил-аспарагил-лизил-серин
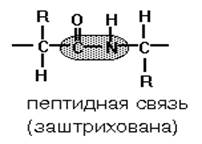
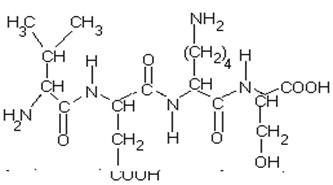
ПЕПТИДНАЯ СВЯЗЬ формируется ТОЛЬКО ЗА СЧЕТ АЛЬФА-АМИНОГРУППЫ И СОСЕДНЕЙ COOH-ГРУППЫ ОБЩЕГО ДЛЯ ВСЕХ АМИНОКИСЛОТ ФРАГМЕНТА МОЛЕКУЛЫ. Если карбоксильные и аминогруппы входят в состав радикала, то они никогда не участвуют в формировании пептидной связи в молекуле белка.
Сама пептидная связь является частично двойной в силу лактим-лактамной таутомерии. Поэтому вокруг нее невозможно вращение, а сама она по прочности в полтора раза превосходит обычную ковалентную связь. На рисунке видно, что из каждых трех ковалентных связей в стержне молекулы пептида или белка две являются простыми и допускают вращение, поэтому стержень (вся полипептидная цепь) может изгибаться в пространстве.
К ковалентным связям в молекуле белка помимо пептидной, относится также ДИСУЛЬФИДНАЯ СВЯЗЬ.
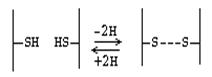
Дисульфидная связь - это ковалентная связь. Однако биологически она гораздо менее устойчива, чем пептидная связь. Это объясняется тем, что в организме интенсивно протекают окислительно-восстановительные процессы. Дисульфидная связь может возникать между разными участками одной и той же полипептидной цепи, тогда она удерживает эту цепь в изогнутом состоянии. Если дисульфидная связь возникает между двумя полипептидами, то она объединяет их в одну молекулу.
Дата добавления: 2015-09-14; просмотров: 1063;
