Гідроліз.
Гідроліз – обмінна реакція речовин з водою, під час якої складові частини речовини сполучаються зі складовими частинами води ( 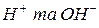 ).
).
Солі гідролізують лише тоді, коли іони води зв’язуються іонами солі у слабкі кислоти або слабкі основи. Отже, гідролізу піддаються солі, утворені слабкими кислотами, слабкими основами.
1. Солі сильних кислот та сильних основ гідролізу не піддаються. Середовище розчину нейтральне, 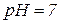 .
.
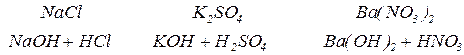
2. Солі сильних основ та слабких кислот гідролізу піддаються. Гідроліз проходить по аніону кислотного залишку (від слабкої кислоти). Середовище розчину лужне, 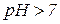 .
.
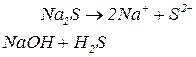
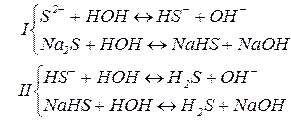
3. Солі слабких основ та сильних кислот гідролізу піддаються. Гідроліз проходить по катіону металу (від слабкої основи). Середовище розчину кисле, 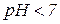 .
.
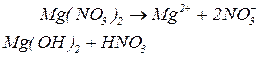
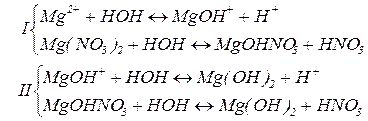
4. Солі слабких основ та слабких кислот гідролізу піддаються. Гідроліз проходить по катіону металу та аніону кислотного залишку (від слабкої основи та слабкої кислоти). Середовище розчину нейтральне, 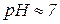 .
.
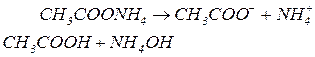
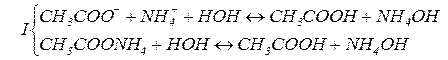
Солі слабких трьохкислотних основ ( 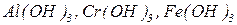 ) та слабких двохосновних кислот (
) та слабких двохосновних кислот ( 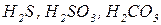 ) гідролізують повністю (в одну стадію) і необоротньо.
) гідролізують повністю (в одну стадію) і необоротньо.
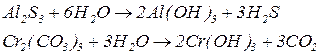
Цей тип гідролізу ускладнює реакції обміну між розчинами солей:
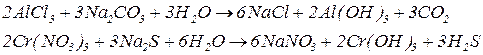
Із солей двохкислотних слабких основ за таких умов утворюються основні солі:
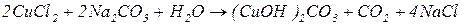
Дата добавления: 2015-09-02; просмотров: 671;
