III тип
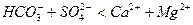 или
или 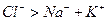 - воды морей и океанов, сильно минерализованных подземных источников.
- воды морей и океанов, сильно минерализованных подземных источников.
IV тип
 - кислые воды.
- кислые воды.
Химические ингредиенты природных вод – главные ионы, растворенные газы, биогенные вещества, микроэлементы, органические вещества.
Главные ионы:
Анионы: 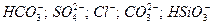
Катионы: 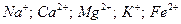
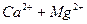 - обусловливают жесткость воды;
- обусловливают жесткость воды;
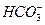 - обусловливает карбонатную жесткость;
- обусловливает карбонатную жесткость;
Соединение 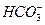 [мг-экв/л] характеризует общую щелочность воды.
[мг-экв/л] характеризует общую щелочность воды.
Растворенные газы:
Кислород поступает из воздуха. В придонных слоях водоемов концентрация кислорода ниже, т.к. он потребляется в процессе окисления донных отложений.
Растворенный кислород придает воде освежающий вкус, усиливает коррозионную активность воды.
Диоксид углерода СО2 – этот газ находится в воде в молекулярном виде и в форме угольной кислоты.
(СО2+Н2СО3) – свободная угольная кислота определяется при анализе воды.
Источник – биохимические процессы распада органических веществ.
Концентрация углекислого газа в воде зависит от М [г/л], рН, t 0С, [Са2+] и характеризуется карбонатным равновесием
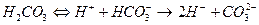
Сероводород.
Воды, не содержащие кислород, содержат сероводород (H2S).
Образуется при растворении сульфидных минералов под действием угольной кислоты, при биохимическом разложении серосодержащих органических соединений, не содержащих кислород.
H2S S2-
 |  |
H2S+HS-

pH=5 pH=9
Биогенные вещества.
 Минеральные и органические соединения азота
Минеральные и органические соединения азота
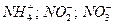 белки + продукты распада
белки + продукты распада
Соединение различных форм азота зависят от условий поступления азотсодержащих соединений в воду, режима окисления водоема.
Фосфор.
Минеральные форм 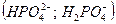 и органические соединения способствуют развитию микроорганизмов.
и органические соединения способствуют развитию микроорганизмов.
Соединения железа.
Fe2+ – только в подземных водах. Поступают в воду при растворении железистых соединений
Fe3+ - в поверхностных водах, содержание мало, ввиду полного гидролиза его солей.
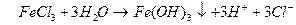
Соединения кремния.
Кремниевая кислота (H2SiO3) и ее соли, частицы различных алюмосиликатов в коллоидном и взвешенном состоянии.
Органические вещества.
Основная часть – гумусовые соединения, которые образуются при разложении растительных остатков.
Концентрация органических веществ в воде характеризуется величиной окисляемости, т.е. количеством кислорода расходуемого на окисление примесей сильными окислителями (KMnO4; K2Cu2O7), перманганатной окисляемостью, ХПК, БПК (для природных вод перманганатная окисляемость - менее 1 мг/л).
Микроэлементы
Li, Rb, Cs, Sr, Ba – типичные катионы
Cu, Ni, Cd – ионы тяжелых металлов
Ci, Mo, V – амфотерные комплексообразователи
I, F, Br – типичные анионы
Радиоактивные элементы.
Дата добавления: 2015-08-11; просмотров: 624;
