Паховый лимфогранулематоз
Определение. Паховый лимфогранулематоз (ПЛГ) — передаваемое половым путем инфекционное заболевание, вызываемое штаммами С. trachomatis, относящимися к сероварам L1—L3, чаще всего к серовару L2. У гетеросексуальных мужчин острое заболевание характеризуется преходящим первичным поражением половых органов, после чего следует развитие многоячеистой, гнойной регионарной лимфаденопатии. У женщин, гомосексуальных мужчин, а иногда и у гетеросексуальных мужчин может развиться геморрагический проктит, сопровождаемый регионарным лимфаденитом. Острый ПЛГ почти всегда сопровождается системными симптомами, такими, как лихорадка и лейкоцитоз, а в редких случаях и системными осложнениями, такими как менингоэнцефалит. После длящегося несколько лет латентного периода развиваются отдаленные осложнения, включая такие, как слоновость половых органов, стриктуры и свищи полового члена, мочеиспускательного канала и прямой кишки.
Эпидемиология. ПЛГ обычно передается половым путем, но были отмечены случаи переноса заболевания при неполовом личном контакте, через предметы обихода или в результате случайного заражения в лабораторных условиях. Лабораторные работы, связанные с возникновением аэрозолей, содержащих эти микроорганизмы (например, размельчение ультразвуком, гомогенизация), следует выполнять с использованием соответствующих биологических ограничителей.
Чаще заболевают лица в возрасте 20—30 лет, ведущие активную половую жизнь. Показатели заболеваемости ПЛГ во всем мире снижаются, но болезнь все еще остается эндемической и является основной причиной заболеваемости в Азии, Африке и Южной Америке. В США в 1982 г. было зарегистрировано только 235 случаев заболевания.
Считают, что частота случаев инфицирования С. trachomatis значительно меньше этого показателя для гонококковой инфекции и сифилиса. У мужчин признаки заболевания выявляют несколько ранее, чем у женщин, которые обычно обращаются к врачу в более поздних стадиях болезни. В США, где, согласно статистике, соотношение полов составляет 3, 4 мужчины на 1 женщину, большинство случаев заболевания приходится на гомосексуальных мужчин, путешественников, моряков и военнослужащих, возвращающихся из-за границы, а также на лиц, относящихся к малоимущим слоям населения, проживающих в регионах с низкой эндемичностью на юго-востоке страны. Предполагают, что главным резервуаром инфекции являются лица с бессимптомным течением заболевания, хотя непосредственных доказательств справедливости такой точки зрения не было приведено.
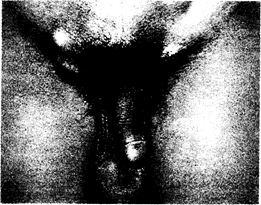
Рис. 150-1. Паховый лимфогранулематоз. Двусторонние паховые бубоны с расположенным между ними «знаком желобка», вызванным аденопатией выше и ниже пупартовой связки (предоставлено A. Brathwaite).
Клинические проявления. У гетеросексуальных лиц первичное поражение половых органов развивается в сроки от 3 сут до 3 нед после контакта с больным партнером. Это поражение представляет собой небольшой безболезненный пузырек, неуплотненную язву или папулу, расположенные на половом члене у мужчин или на половых губах, задней стенке влагалища или уздечке половых губ у женщин. На этот первичный аффект обращают внимание менее 30% заболевших ПЛГ мужчин и лишь в редких случаях — женщины. Заживление первичного поражения происходит через несколько суток без образования рубца, так что даже в тех случаях, когда его появление не осталось незамеченным, его обычно не связывают с ПЛГ. Определенные сомнения возникают лишь тогда, когда появившееся поражение ассоциируется с некоторыми происходившими в прошлом событиями. Иногда С. trachomatis выявляли в язвах половых органов, а также в мочеиспускательном канале мужчин и нижней части шейки матки женщин, обращавшихся по поводу паховой аденопатии. Это заставляло предположить, что в некоторых случаях именно эти области могут быть местом локализации первичного аффекта.
У женщин и гомосексуальных мужчин в результате инфицирования после анального коитуса развивается первичный анальный, или ректальный, аффект. У женщин ректальное инфицирование ПЛГ (или не-ПЛГ)-штаммами С. trachomatis, по-видимому, может также произойти в результате распространения инфицированных секретов по промежности (как при ректальном гонококковом инфицировании) или путем распространения инфекции в прямую кишку через тазовые лимфатические сосуды. От места первичного аффекта, расположенного в мочеиспускательном канале, половых органах, заднепроходном канале или прямой кишке, микроорганизмы распространяются через регионарные лимфатические узлы. Инфекция, локализующаяся в половом члене, наружных половых органах женщины и заднепроходном канале, может вызвать развитие пахового и бедренного лимфаденита. Инфекция, локализующаяся в прямой кишке, вызывает развитие подчревного и глубокого подвздошного лимфаденита. Инфекция, локализующаяся в верхних отделах влагалища и в шейке матки, приводит к увеличению обтурирующих и подвздошных лимфатических узлов. У гетеросексуальных мужчин чаще всего наблюдают паховый синдром, характеризующийся болезненной паховой лимфаденопатией, развившейся через 2—6 нед (реже — через несколько месяцев) после предполагаемого заражения, У 60% больных паховая аденопатия бывает односторонней и на той стороне, где наблюдается увеличение паховых лимфатических узлов, часто пальпируются увеличенные подвздошные и бедренные лимфатические узлы. Постепенно прогрессирующий периаденит приводит к слиянию этих лимфатических узлов в единую массу, которая становится флюктуирующей и гнойной. Покрывающая их кожа становится фиксированной, воспаляется и истончается, и в конечном итоге в ней развиваются множественные сочащиеся гноем свищи. Чрезмерное увеличение цепочек паховых лимфатических узлов, расположенных выше и ниже паховой связки («знак желобка»), — обычное, но не специфическое явление и наблюдается у меньшей части больных (рис. 150-1). Первоначально гистологическая картина инфицированных лимфатических узлов характеризуется небольшими звездообразными абсцессами, окруженными гистиоцитами. Эти абсцессы затем сливаются, образуя большие некротические гнойные очаги. Через несколько месяцев происходит самопроизвольное заживление, оставляющее после себя паховые рубцы или гранулематозные массы разных размеров, сохраняющиеся в течение всей жизни больного. Массивная тазовая лимфаденопатия у женщин или гомосексуальных мужчин может вызвать необходимость диагностической лапаротомии.
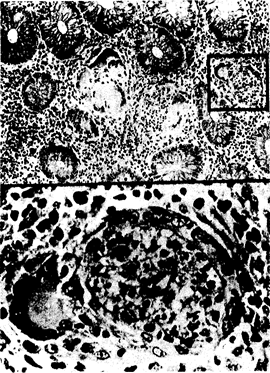
Рис. 150-2. Гистопатологические изменения при ПЛГ-проктите у активного мужчины-гомосексуалиста. Обратите внимание на наличие гранулематозных изменений с гигантскими клетками и крипта-абсцесс с прилегающей гигантской клеткой (вставка). Эти изменения сходны с теми поражениями, которые наблюдаются в прямой кишке при болезни Крона (из Т. С. Quinn et al„ N. Engl. J. Med., 305—195, 1981).
По мере того как расширялось использование бактериологических и серологических методов исследования при инфицировании С. trachomatis, стали выявлять все возрастающее число случаев заболевания ПЛГ-проктитом у гомосексуальных мужчин. У больных наблюдаются аноректальные боли и слизисто-гнойные кровянистые выделения из прямой кишки. Жалобы больных на понос обусловлены частыми болезненными, безуспешными попытками дефекации (тенезмы). При ректороманоскопии обнаруживают язвенный проктит или проктоколит, сопровождаемый выделением гнойного экссудата и кровоточивостью слизистых оболочек. Поскольку возбудитель ПЛГ является облигатным внутриклеточным патогеном, при гистологическом исследовании слизистой оболочки прямой кишки обнаруживают гранулемы с гигантскими клетками, а также крипта-абсцессы и обширное воспаление. Эти клинические и гистопатологические признаки, а также полученная при ректороманоскопии информация могут быть весьма сходными с соответствующими изменениями в прямой кишке, выявляемыми при болезни Крона (рис. 150-2).
В стадии развития регионарной лимфаденопатии обычно наблюдаются конституциональные симптомы, при проктите включающие в себя лихорадку, озноб, головную боль, менингизм, анорексию, миалгии и артралгии. При наличии лимфаденопатии эти симптомы иногда ошибочно принимают за лимфосаркому. К числу других системных осложнений, развивающихся, однако, достаточно редко, относятся артрит, сопровождаемый стерильным выпотом, асептический менингит, менингоэнцефалит, конъюнктивит, гепатит и узловатая эритема. Хламидии были выделены из цереброспинальной жидкости, а в одном случае из крови больного с тяжелыми конституциональными симптомами, что указывало на развитие диссеминированного инфицирования. Заражение в лабораторных условиях, вызванное, вероятно, вдыханием инфицированных аэрозолей, привело к развитию медиастинального лимфаденита, пневмонита и выпоту в плевральную полость.
При лабораторных исследованиях в острой стадии заболевания выявляли лейкоцитоз и небольшое увеличение скорости оседания эритроцитов, а при подостром и хроническом течении — аномальные результаты печеночных проб, гиперглобулинемию, смешанную криоглобулинемию, увеличение активности ревматоиидного фактора и повышение уровней содержания IgG, IgA и IgM. Серологические тесты по выявлению сифилиса редко дают ложноположительные результаты, и, если они оказываются положительными, у больного следует подозревать сифилис.
К числу осложнений нелеченого аноректального инфекционного заболевания относятся периректальный абсцесс, свищ заднего прохода, прямокишечно-влагалищный, пузырно-прямокишечный и седалищно-прямокишечный свищи. В развитии этих осложнений, возможно, играет роль и вторичная бактериальная инфекция. Стриктура прямой кишки является осложнением поздней стадии аноректального инфекционного процесса и обычно локализуется на расстоянии 2—6 см от заднего прохода, в пределах достижимости для пальцевого исследования прямой кишки. Эта стриктура может простираться на несколько сантиметров в глубь прямой кишки, что приводит к ошибочному клиническому и рентгенологическому диагнозу рака прямой кишки.
У некоторых мужчин ПЛГ оставляет такие осложнения, как хроническое прогрессирующее инфильтративное, язвенное или свищевое поражение полового члена, мочеиспускательного канала или мошонки. Может развиться стриктура мочеиспускательного канала, обычно локализованная в его заднем отделе и вызывающая недержание мочи или затрудненное мочеиспускание.
Редким поздним осложнением ПЛГ является слоновость половых органов, представляющая собой хронические индурацию и отек полового члена или наружных половых органов женщины вследствие обструкции лимфатических сосудов. Полипоидные поражения кожи и большие звездчатые гиперпластические келоидные рубцы на половых органах могут сочетаться с индурацией наружных половых органов женщины и лимфедемой и их бывает трудно отдифференцировать от паховой гранулемы и туберкулеза половых органов. Кроме того, могут иметь место хронические изъязвления наружных половых органов женщины (эстиомены) и гладкие, снабженные ножками перианальные разрастания (лимфорроиды). Однако неизвестно, связан ли хронический аноректальный или генитальный ПЛГ со злокачественными изменениями.
Диагностика. Хотя ПЛГ — не очень распространенное заболевание, его следует иметь в виду при дифференциальной диагностике таких распространенных состояний, как паховая лимфаденопатия, пузырчатые, узелковые или язвенные поражения половых органов, а также периректальные абсцессы, свищи в заднем проходе или проктиты.
Самым надежным методом диагностики служит выделение ПЛГ-штаммов (Chlamydia) из аспирированного содержимого бубонов, из прямой кишки, мочеиспускательного канала, шейки матки или других инфицированных тканей. Выделить эти штаммы из бубонов удалось у 30% больных с паховой лимфаденопатией, а из прямой кишки — у большинства страдающих проктитом гомосексуальных мужчин. Ранее при иммунодиагностике чаще всего использовали тест на ПЛГ с фиксацией комплемента (ФК) и внутрикожные реакции Фрея. У большинства больных после появления бубонов величина титра ФК>1:64, что позволяет предположить наличие ПЛГ. При повторных исследованиях сыворотки крови величина титра может не увеличиваться, поскольку большинство больных были инфицированы уже в течение нескольких недель до проведения первого теста. Положительные результаты ПЛГ ФК-теста могут наблюдаться и при инфекциях, вызванных не-ПЛГ-штаммами С. trachomatis, причем у больных с тяжелым течением заболевания титры ФК-антител могут быть достаточно высокими. Кожная реакция Фрея менее чувствительна, чем тест со связыванием комплемента, в связи с этим ее больше не применяют.
Тест с микроиммунофлюоресцирующими антителами выявляет наличие антител к С. trachomatis почти у всех больных ПЛГ с диагнозом, подтвержденным результатами бактериологических исследований посева. Титры микроиммунофлюоресцирующих антител в сыворотке крови больных с ПЛГ составляют обычно >1:512, что превышает самые высокие значения титров, полученных при хламидийном НГУ. Следует отметить, что они обладают характерным широким спектром реактивности против многих иммунотипов С. trachomatis. Гистопатологическая картина ткани лимфатических узлов или результаты исследования биоптатов, взятых из прямой кишки, неспецифичны, но выявление звездчатых абсцессов в лимфатических узлах или гранулемы в ректальном биоптате может вызвать подозрение о наличии ПЛГ и повлечь за собой проведение более специфических тестов. Связанные с флюоресцеином моноклональные антитела против С. trachomatis и против штамма L2 С. trachomatis могут оказаться полезными для выявления микроорганизмов в правильно фиксированных образцах ткани, взятой из лимфатических узлов или других органов, а моноклональные антитела против штамма L2 — для быстрой идентификации этих штаммов, выделенных из клеточных культур.
Лечение. ПЛГ- и не-ПЛГ-штаммы С. trachomatis обладают сходной чувствительностью к действию антимикробных средств. Антимикробная терапия не оказывает значительного влияния на длительность развития и заживления паховых бубонов, но зачастую приводит к быстрому исчезновению острых конституциональных симптомов и улучшению состояния больного (в частности, при ПЛГ-проктите). Антибиотики неэффективны при поздних осложнениях, таких как стриктура прямой кишки или слоновость половых органов, и применять их целесообразно лишь в случае вторичной инфекции. При слоновости половых органов, стриктурах и свищах прямой кишки, полового члена и мочеиспускательного канала обычно требуется хирургическое лечение, хотя иногда больным со стриктурами мочеиспускательного канала и даже прямой кишки показана повторная механическая дилатация.
Больному вводят тетрациклина гидрохлорид по 0,5 г 4 раза в сутки в течение 3 нед. Можно также применять сульфонамиды по 4 г в сутки в течение 3 нед, но некоторые возбудители болезни резистентны к сульфонамидам in vitro. Содержимое флюктуирующих бубонов по мере необходимости (для предотвращения их самопроизвольного разрыва) следует отсасывать путем прокола через кожу шприцем с иглой 18-го калибра. Нередко после начала лечения бубоны увеличиваются в размерах или появляются в другом месте. Хотя бубоны редко развиваются до стадии образования свища, в случае появления флюктуации их содержимое следует отсасывать. Через несколько месяцев у большинства больных, получавших адекватное лечение, происходит 4-кратное и более снижение титра ФК-антител или микроиммунофлюоресцирующих антител. После начала лечения антибиотиками выделить возбудитель из пораженных участков не удается.
Дата добавления: 2015-07-22; просмотров: 1096;
