Бешенство
Бешенство представляет собой остропротекающую вирусную болезнь млекопитающих, характеризующуюся поражением центральной нервной системы и передающуюся с инфицированным секретом, обычно слюной. Чаще всего заражение бешенством происходит во время укуса инфицированного животного, однако в ряде случаев оно может произойти при попадании в организм аэрозольных частиц, содержащих вирус, при использовании в пищу мяса больных животных или в случае трансплантации инфицированных тканей.
Этиология. Вирус бешенства принадлежит семейству рабдовирусов. Вирион имеет форму пули, покрыт оболочкой, содержит одну спираль рибонуклеиновой кислоты (РНК). Диаметр вириона 75—80 нм. Поверхность вириона покрыта гликопротеидными наростами длиной 6—7 нм, имеющими булавовидные утолщения на дистальном конце. Вирусные гликопротеиды способны связываться с ацетилхолиновыми рецепторами и обусловливают нейровирулентность вируса бешенства. Эти поверхностные структуры стимулируют образование нейтрализующих и гемагглютининподавляющих антител, в то время как нуклеокапсидные антигены индуцируют образование комплементсвязывающих антител. Нейтрализующие антитела к поверхностным гликопротеидам играют, видимо, . защитную роль. Антитела против вируса бешенства, используемые в диагностических иммунофлюоресцентных исследованиях, как правило, направлены против нуклеокапсидных антигенов. Вирусы бешенства, выделенные из различных видов животных и из разных областей, имеют разные биологические свойства. Также были обнаружены антигенные вариации у разных штаммов, что может объяснить различия их вирулентности и отсутствие эффекта при использовании некоторых режимов вакцинации. Вирус бешенства индуцирует синтез интерферона, осо бенно в тканях с высокой концентрацией вирусов, что может играть определенную роль в замедлении прогрессирования инфекции.
Эпидемиология. Бешенство существует в двух эпидемиологических формах: городская форма бешенства распространяется главным образом неиммунизированными домашними животными, собаками и/или кошками; лесная форма бешенства распространяется скунсами, лисами, енотами, мангустами, волками и летучими мышами. Инфекция домашних животных чаще всего «выплескивается» из лесного резервуара инфекции. А человек может быть заражен как домашними, так и дикими животными. Таким образом, заболевание у человека, как правило, возникает в областях, где бешенство носит энзоотический или эпизоотический характер, где имеется большое количество неиммунизированных домашних животных и где люди часто контактируют с дикими животными. Несмотря на'то что ВОЗ сообщает лишь о 800 случаях смерти от бешенства ежегодно, общая частота регистрации бешенства во всем мире свидетельствует о том, что ежегодно возникает около 15000 случаев заболевания. Юго-Восточная Азия, Филиппины, Африка и Индийский субконтинент — это те области, где заболевание особенно распространено. Увеличение распространения лесной формы бешенства и частые посещения стран с высоким уровнем городской формы бешенства делают проблему диагностики и профилактики этого заболевания чрезвычайно важной. В США бешенство у человека встречается исключительно редко. Ежегодно сообщают не более чем о пяти случаях.
В большинстве стран мира основным переносчиком вируса бешенства для человека является собака, хотя волки (Восточная Европа, арктические районы), мангусты (Южная Африка, Карибский район), лисы (Западная Европа) и летучие мыши-вампиры (Латинская Америка) также могут выступать в качестве переносчика заболевания. Грызуны редко инфицируются вирусом бешенства. В США наиболее важными источниками заболевания человека служат скунсы, летучие мыши и еноты. Вирус бешенства встречается преимущественно у диких животных (85%) и только у 2—3% домашних собак и кошек. Однако в большинстве случаев профилактические мероприятия против бешенства проводятся после укусов собак.
Сообщалось о передаче бешенства при трансплантации роговицы.
Патогенез. На первом этапе вирус проникает через эпидермис или попадает на слизистую оболочку. Первичная репликация вирусов происходит, видимо, в клетках поперечнополосатых мышц в месте инокуляции вируса. Контакт вируса с периферической нервной системой осуществляется в области нейромышечного и/или нейросухожильного веретена. Затем, возможно по аксоплазме периферического нерва, вирус распространяется афферентно к центральной нервной системе. Развивающейся вирусемии, как показали эксперименты, недостаточно, чтобы играть ведущую роль в генезе естественного заболевания. После того как вирус достиг центральной нервной системы, он начинает реплицироваться в сером веществе мозга, а затем распространяется эфферентно вдоль вегетативных нервов в другие ткани — слюнные железы, кору надпочечников, почки, легкие, скелетные мышцы, кожу и сердце. Нахождение вируса в слюнных железах обусловливает дальнейшее распространение заболевания с инфицированной слюной. Инкубационный период бешенства чрезвычайно вариабелен: от 10 дней до 1 года и более (в среднем 1—2 мес). Его продолжительность, видимо, зависит от количества попавших в организм вирусных частиц, объема пораженной ткани, защитных механизмов макроорганизма, расстояния, которое вирус должен преодолеть от места инокуляции до центральной нервной системы. Исследования у животных показали, что выраженность иммунного ответа макроорганизма и особенности вирусного штамма также влияют на активность заболевания. Аттенуированные штаммы вируса бешенства вызывают более выраженный цитотоксический эффект по сравнению с диким «уличным» вирусом. Животным, у которых развивается паралитическое бешенство (немое бешенство), видимо, свойствен более выраженный иммунный ответ на инфекцию, чем тем, у которых развивается молниеносный энцефалит.
Нейропатология бешенства сходна с изменениями, которые вызывают другие вирусные заболевания, поражающие центральную нервную систему, — гиперемия, хроматолиз различной степени выраженности, пикноз ядер, нейронофагия, лимфоцитарная и плазмоклеточная инфильтрация периваскулярного пространства; инфильтрация микроглии и разрушение нервных клеток паренхиматозных областей. Патогномоничным признаком бешенства является появление телец Бабеша—Негри, представляющих собой эозинофильное образование размером около 10 нм, состоящее из тонкого фибриллярного матрикса и частиц вируса бешенства. Тельца Бабеша—Негри локализуются в мозге, в частности в гиппокампе, коре и стволе мозга, грушевидных нейронах мозжечка, дорсальных ганглиях спинного мозга. Тельца Бабеша—Негри могут отсутствовать приблизительно в 20% случаев бешенства, что, однако, не исключает этого диагноза.
Клинические проявления. Клинические проявления бешенства могут быть разделены на следующие стадии: 1) неспецифический продромальный период; 2) острый энцефалит, сходный с другими вирусными энцефалитами; 3) глубокая дисфункция стволовых центров, сопровождающаяся классической картиной энцефалита при бешенстве, и 4) выздоровление (в редких случаях).
Продромальный период обычно длится в течение 1—4 дней и характеризуется лихорадкой, головными болями, недомоганием, мышечными болями, повышенной утомляемостью, отсутствием аппетита, тошнотой и рвотой, болями в горле, непродуктивным кашлем, а также парестезиями и/или мышечными подергиваниями в области инокуляции вируса (этот симптом присутствует у 50—80% больных).
О начале стадии острого энцефалита обычно возвещает период избыточной двигательной активности, возбуждения и тревоги. Быстро вслед за этим развиваются нарушения сознания, галлюцинации, агрессивность, спутанность мыслей, менингизм, опистотонус, судороги, местные параличи. Характерно, что периоды нарушения сознания перемежаются периодами его полного восстановления (светлые промежутки). Однако по мере прогрессирования заболевания светлые промежутки становятся короче, затем больной впадает в кому. Очень часто имеет место гиперестезия, избыточная чувствительность к яркому свету, громким звукам, прикосновениям и даже легкому дуновению. Температура тела повышается до 40,6°С. Со стороны вегетативной нервной системы отмечают такие изменения, как неравномерное расширение зрачков, повышенное слезотечение, саливация, потоотделение и постуральная гипотензия. Паралич верхнего двигательного нейрона приводит к слабости, повышению глубоких сухожильных рефлексов и разгибательных подошвенных реакций. Часто развивается паралич голосовых связок.
Вскоре после начала стадии острого энцефалита появляются признаки дисфункции ствола мозга. Вовлечение в процесс черепных нервов приводит к появлению диплопии, паралича лицевого нерва, неврита глазного нерва. Характерно затруднение глотания. Сочетание избыточной саливации и затруднения глотания слюны дает традиционную картину «пены у рта». Приблизительно в 50% случаев можно наблюдать гидрофобию, представляющую собой болезненные, сильные, непроизвольные сокращения диафрагмы, дополнительной дыхательной, глоточной и гортанной мускулатуры, развивающиеся в ответ на попытку проглотить жидкость. Поражение миндалевидного тела может вызвать приапизм и спонтанную эякуляцию. Больной впадает в кому, а вовлечение в процесс дыхательного нерва вызывает смерть в результате апноэ. Выраженность ранней дисфункции ствола мозга отличает бешенство от других вирусных энцефалитов и лежит в основе быстрого прогрессирования заболевания. Средний период течения заболевания после появления симптомов составляет 4 дня, максимально 20 дней при условии проведения искусственных поддерживающих мероприятий.
Если проводится интенсивная дыхательная терапия, то может возникнуть целый ряд поздних осложнений, включая нарушение секреции антидиуретического гормона, несахарный диабет, нарушения ритма сердца, сосудистую нестабильность, респираторный дистресс-синдром взрослых, желудочно-кишечное кровотечение, тромбоцитопению и паралитический илеус. Выздоровление бывает очень редко, но если имеет место, то происходит постепенно. Сообщают лишь о трех подобных случаях. В двух случаях пациентам проводили частичную профилактику после контакта с вирусом, а в третьем случае лабораторного бешенства, возникшего, видимо, вследствие вдыхания аэрозоля, пациент получил профилактическое вмешательство еще до контакта с вирусом.
Иногда бешенство может проявляться в виде восходящего паралича (тихое бешенство). Этот клинический вариант развивается чаще всего после укуса ле тучей мыши-вампира или если профилактика заболевания проводилась еще до контакта с вирусом.
Трудность диагностики бешенства в тех случаях, когда оно сочетается с восходящим параличом, подтверждается фактом передачи вируса при трансплантации зараженных вирусом тканей. Трансплантация роговицы от донора, который умер предположительно от восходящего паралича, привела к развитию клинической картины бешенства и смерти у реципиента. Ретроспективное патологическое исследование препаратов мозга обоих пациентов показало наличие телец Бабеша—Негри. Впоследствии из замороженных глазных яблок донора был выделен вирус бешенства.
Лабораторные исследования. На ранних стадиях заболевания показатели гемоглобина и рутинные показатели крови остаются в пределах нормы. Изменения возникают по мере того, как развивается дисфункция гипоталамуса, появляются желудочно-кишечное кровотечение и другие осложнения. Лейкоцитоз периферической крови обычно составляет 12—17•109/л, но может достигать и 30•109/л или, напротив, оставаться в пределах нормы.
Как и при любой вирусной инфекции, специфическая диагностика бешенства зависит от 1) выделения вируса из инфицированных сред организма— слюны, редко спинномозговой жидкости или тканей мозга; 2) серологического подтверждения острой инфекции или 3) обнаружения вирусных антигенов в инфицированных тканях (контактных мазках роговицы, биопсии кожи или мозга). Образцы ткани мозга, полученные либо при аутопсии, либо при биопсии мозга, следует 1) ввести мышам для дальнейшего выделения вируса; 2) обработать флюоресцирующими антителами, позволяющими идентифицировать антигены; 3) подвергнуть гистологическому и/или электронно-микроскопическому исследованию с целью обнаружения телец Бабеша—Негри. Если жизнь пациента поддерживается и в организме присутствует большое количество нейтрализующих антител (в сыворотке и спинномозговой жидкости), то исследования с инокуляцией вируса и прямой обработкой материала флюоресцирующими антителами для обнаружения антигенов являются надежными и чувствительными. Но может произойти «аутостерилизация», и тогда результаты этих методов будут отрицательными. Использование флюоресцирующих антител для обработки препаратов биопсии кожи, контактных мазков роговицы и слюны позволяет обнаружить антигены вируса бешенства и облегчить прижизненную диагностику заболевания. Следует, однако, попытаться подтвердить эти результаты серологическими методами исследования или обнаружением вируса в тканях мозга.
Если больной не получал противорабической иммунизации, то диагностическое значение имеет четырехкратное повышение титра нейтрализующих антител к вирусу бешенства в серии проб сыворотки. Если больной был вакцинирован против бешенства, то ключом к постановке диагноза служат абсолютный титр нейтрализующих антител и наличие антител к вирусу бешенства в спинномозговой жидкости. Профилактика бешенства, проводимая после контакта больного с вирусом, редко приводит к образованию нейтрализующих антител, попадающих в спинномозговую жидкость. Даже если они присутствуют, то обычно их титр невысок, менее 1:64, в то время как при бешенстве титр антител в спинномозговой жидкости у человека варьирует от 1:200 до 1:160000.
Дифференциальная диагностика. Наибольшую помощь при дифференциальной диагностике бешенства оказывает анамнестический факт контакта пациента с вирусом. К другим состояниям, которые следует иметь в виду при проведении дифференциальной диагностики, относятся истерическая реакция на укус животного (псевдогидрофобия), восходящий паралич, полиомиелит и аллергический энцефаломиелит в ответ на введение рабической вакцины. Последний чаще всего развивается после использования вакцины, полученной из нервной ткани, и проявляется через 1—4 нед после вакцинации.
Профилактика и лечение. Ежегодно более 1 млн американцев обращаются по поводу укусов животных. В каждом случае необходимо принимать решение о том, начинать ли постконтактную противорабическую профилактику. Если принимается решение о начале проведения профилактики, то следует иметь в виду следующие положения: 1) имелся ли физический контакт пациента со слюной или другими веществами, способными содержать вирус бешенства; 2) бешенство имеется или только подозревается у животных, обитающих в соответствующей местности (например, все лица, которых на континентальной части США укусила летучая мышь, улетевшая затем в неизвестном направлении, должны получить постконтактную профилактику); 3) обстоятельства, при которых произошел контакт; 4) варианты лечения и возможные осложнения. Алгоритм проведения постконтактной профилактики бешенства представлен на рис. 142-1.
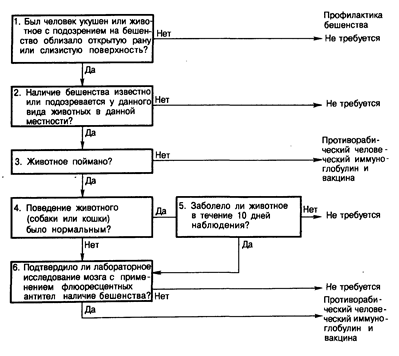
Рис. 142-1. Алгоритм постконтактной профилактики бешенства (домашний скот и невакцинированные собаки и кошки с нормальным поведением требуют индивидуального подхода. Следует обратиться за консультацией в соответствующие местные и государственные официальные учреждения).
Если известно, что данный вид животных поражен бешенством или этот факт нельзя исключить, то животное, укусившее человека, должно быть при возможности изолировано. Диких животных или любых больных, невакцинированных или заблудившихся домашних животных, в особенности животных, неспровоцированно напавших на человека, поведение которых ненормально, подозрительных на бешенство, следует поймать и умертвить. Голову животного следует немедленно отправить в соответствующую лабораторию для обследования на наличие вируса бешенства. Если обследование мозга животных с помощью флюоресцентных методов не выявило наличия вирусного антигена, то можно предположить, что слюна также не содержит вирус и укушенному человеку лечение можно не проводить. Лица, контактировавшие с исчезнувшим диким животным, которое с большой степенью вероятности могло быть заражено вирусом бешенства (летучая мышь, скунс, койот, лиса, енот и т. д.) в области, где наличие бешенства известно или подозревается, должны получить как пассивную, так и активную иммунизацию против бешенства.
Если здоровое животное (собака или кошка) кусает человека, оно должно быть поймано, изолировано и находиться под наблюдением в течение 10 дней. Если за это время развивается заболевание или поведение животного стано вится ненормальным, то его следует умертвить и обследовать с помощью флюоресцентных методов на наличие вируса бешенства.
Постконтактная профилактика. После того как принято решение о необходимости начать постконтактную профилактику бешенства, следует руководствоваться общим принципом терапии при бешенстве, заключающимся в следующем: уменьшить количество вируса в области инокуляции путем местной обработки раны и способствовать формированию раннего и стойкого титра нейтрализующих антител к вирусу бешенства. В большинстве случаев это включает введение глобулина и вакцин. Рекомендуют использовать следующую схему лечения:
1. Местная обработка раны заключается в тщательном ее промывании с применением моющих средств и большого количества воды. Важно как механическое, так и химическое очищение раны. Также целесообразно использовать такие вещества, как 1—4% растворы хлорида бензалкония или 1% раствор бромида цетримония. Однако 0,1% растворы бензалкония менее эффективны, чем 20% мыльные растворы. Обычно вводят также противостолбнячный анатоксин и антибиотики (как правило, пенициллин).
2. Пассивная иммунизация антирабической антисывороткой лошадиного или человеческого происхождения. Предпочтение следует отдавать человеческому антирабическому иммуноглобулину, поскольку после введения лошадиной антисыворотки высока частота возникновения сывороточной болезни (20—40%). Половину общей дозы антирабического иммуноглобулина (составляющую 20 ЕД/кг) или лошадиной сыворотки (составляющую 40 ЕД/кг) вводят местно, инфильтрируя рану, вторую половину вводят внутримышечно.
3. Активная иммунизация антирабической вакциной. В Соединенных Штатах имеется в настоящее время лишь одна инактивированная антирабическая вакцина, приготовленная на основе лабораторного штамма вируса бешенства в культуре диплоидных клеток человека (ВДКЧ). Вакцина, созданная в Европе (Институт Мерьё), основана на использовании цельного вируса. Вакцина ВДКЧ, созданная в США, состоит из субъединиц, растворенных в tri-n-бутилфосфате и затем инактивированных бета-пропиолактоном. Вакцина института Мерьё, видимо, более иммуногенна, и с февраля 1985 г. вакцина Wyeth изъята с рынка США.
Тяжелые поствакцинальные осложнения после введения ВДКЧ редки. Приблизительно у 1 из 650 реципиентов развиваются реакции немедленной гиперчувствительности с появлением уртикарной сыпи. Системные реакции, такие как лихорадка, головные боли и тошнота, протекают обычно легко и встречаются у 1—4% реципиентов. У 15—20% вакцинированных можно наблюдать местные реакции: отек, эритему и уплотнение места инъекции.
Как можно скорее после контакта с вирусом необходимо внутримышечно ввести 5 доз ВДКЧ по 1 мл. Одновременно с введением первой дозы вакцины (день 0) в другую руку больного следует ввести антирабический иммуноглобулин. Последующие дозы вакцины следует вводить на 3-й, 7-й, 14-й и 28-й день.
К настоящему времени наблюдение за 575 лицами, перенесшими укусы животных с подтвержденным диагнозом бешенства, показало, что ни один пациент из тех, кому вводили ВДКЧ в комбинации с антирабическим иммуноглобулином, бешенством не заболел. У всех больных, получивших антирабический иммуноглобулин и 5 доз ВДКЧ внутримышечно, сформировался адекватный титр антител: не менее 1:5 при флюоресцентном экспресс-анализе с подавлением фокуса. Сочетанное введение антирабического иммуноглобулина с внутрикожным введением вакцины в дозе 0,1 мл в восемь участков в день 0, в четыре участка на 7-й день и в один участок на 28-й и 91-й дни также создает хорошую ответную реакцию антител.
Предконтактная профилактика. Лица с высоким риском контакта с вирусом бешенства — ветеринарные врачи, спелеологи, сотрудники лабораторий, лица, работающие с животными,—должны получать предконтактную профилактику с применением антирабической вакцины. Для этой цели предпочтение следует отдавать ВДКЧ: в день 0, на 7-й и с 21-го по 28-й дни следует вводить внутримышечно по три дозы вакцины или в те же дни внутрикожно в области дельтовидной мышцы три дозы по 0,1 мл. После вакцинации необходимо проверить титр нейтрализующих антител. Повторную иммунизацию можно проводить в виде однократного введения 1 мл вакцины внутримышечно или 0,1 мл внутрикожно. Постконтактная профилактика у лиц, ранее получивших пред-контактную терапию, включает только применение вакцины. Как правило, достаточно бывает в день 0 и на 3-й день ввести по 2 дозы ВДКЧ.
Повторную иммунизацию рекомендуется проводить с интервалом в 2 года. Однако при этом у 6% лиц, получивших ВДКЧ внутримышечно, развиваются реакции по типу иммунных комплексов, характеризующиеся появлением уртикарной сыпи, артритов, тошноты, рвоты, а иногда и сосудистого отека. Несмотря на то что эти реакции самокупируются, периодически рекомендуется определять уровни антител. Повторную иммунизацию следует проводить лицам с низкими титрами антител, у которых повышен риск контакта с вирусом.
Дата добавления: 2015-07-22; просмотров: 1527;
