ЛАСИФІКАЦІЯ ЗАБРУДНЮВАЛЬНИХ РЕЧОВИН
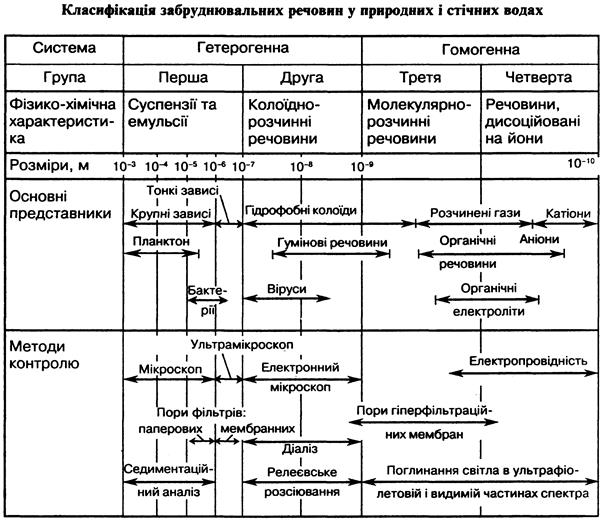
Згідно з класифікацією, запропонованою Л. А. Кульським, забруднювальні речовини за їх фазово-дисперсним станом і відношенням до дисперсійного середовища поділяють на чотири групи. Домішки перших двох груп (крім високомолекулярних сполук) утворюють термодинамічно нестійкі гетерогенні системи, а двох інших – термодинамічно рівноважні оборотні гомогенні системи (див. схему на с. 98).
До першої групи належать не розчинні у воді зависі, а також бактерії та планктон. Вони кінетично нестійкі і підтримуються у завислому стані динамічними силами водяного потоку. В стані спокою зависі осідають. Розмір їх часточок становить 10-3-10-7 м.
Друга група домішок поєднує гідрофільні й гідрофобні мінеральні та органо-мінеральні колоїдні часточки ґрунтів, недисоційовані і нерозчинні форми високомолекулярних гумусових речовин, детергенти та інші речовини. До цієї групи належать також віруси і мікроорганізми, які за своїми розмірами близькі до колоїдних часточок. Розміри дисперсних часточок знаходяться в межах 10-7-10-9 м. Кінетична стійкість гідрофобних домішок характеризується співвідношенням сил гравітаційного поля і броунівського руху. Агрегативна стійкість їх зумовлена електростатичним станом міжфазної поверхні і утворенням на поверхні частинок стабілізувальних шарів.
Третя група забруднювальних домішок включає молекулярно-розчинні сполуки розміром менш ніж 10-9 м. До неї відносять розчинені гази, органічні речовини біологічного походження та інші домішки, що можуть міститися в складі промислових і господарсько-побутових стоків. У водному середовищі можливий перебіг двох процесів: сполучення різнорідних молекул (гідратація) і сполучення однорідних молекул (асоціація). Молекулярно-розчинні речовини здатні за рахунок водневих зв'язків утворювати з водою неміцні сполуки, що існують лише в розчині. Велике значення ці зв'язки мають також при асоціації молекул розчиненої речовини. Необхідною умовою їх виникнення є достатня полярність валентних зв'язків гідрогену у вихідних речовинах.
 |
До четвертої групи забруднювальних домішок належать електроліти – речовини з йонним або сильно полярним зв'язком, які під впливом полярних молекул води дисоціюють на йони. Кристалічні структури цих речовин руйнуються переважно в результаті процесу гідратації.
Для кожної групи домішок можна виділити деякі специфічні фізико-хімічні методи контролю їх вмісту. При цьому враховують розмір часточок, рухливість в електричному полі, взаємодію зі світловим випромінюванням, кінетичну нестійкість системи «вода – домішка» та інші особливості.
Дата добавления: 2015-05-26; просмотров: 1258;
