Десорбционное охлаждение.
Процесс физической адсорбции можно использовать для создания систем охлаждения. Метод предложен и впервые осуществлен Ф. Симоном (1928 г.). Рабочая среда находится в газообразном состоянии, а уменьшение энтропии происходит в результате проявления адсорбционных сил, возникающих между поверхностью твердого тела и адсорбируемым газом. Природа этих сил обусловлена ионным взаимодействием. В качестве адсорбентов обычно используют активированный уголь, цеолиты и другие поверхностно-активные материалы. Процесс адсорбции и обратный ему процесс – десорбция – сопровождаются тепловыми эффектами.
 Захват молекул газа поверхностью твердого тела (адсорбция) приводит к выделению теплоты, эквивалентной изменению кинетической энергии молекул газа. Отрыв молекул от поверхности адсорбента (десорбция) требует затрат энергии и сопровождается поглощением теплоты. Десорбция, проведенная в адиабатных условиях, приводит к снижению температуры.
Захват молекул газа поверхностью твердого тела (адсорбция) приводит к выделению теплоты, эквивалентной изменению кинетической энергии молекул газа. Отрыв молекул от поверхности адсорбента (десорбция) требует затрат энергии и сопровождается поглощением теплоты. Десорбция, проведенная в адиабатных условиях, приводит к снижению температуры.
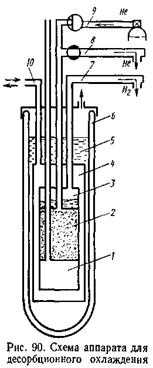
На рис. 90 приведена схема аппарата для реализации этого процесса охлаждения. Аппарат состоит из сосуда Дьюара 6, в котором расположен вакуумный кожух 4. Внутри кожуха имеется сосуд 3, заполненный адсорбентом 2 (активированным углем). Охлаждаемая камера 1 предназначена для экспериментальных целей. Сосуд Дьюара заполнен жидким водородом 5, а вакуумный кожух – теплообменным газом (гелием) для установления теплового контакта между жидкими Н2 и адсорбентом. Охлажденный водородом адсорбент интенсивно поглощает газообразный гелий, поступающий по линии 9. Выделяющаяся теплота адсорбции поглощается жидким водородом; процесс изотермичен. Температура водорода является исходным уровнем процесса (T0). Откачкой водорода из сосуда 3 вакуумным насосом по линии 7 можно обеспечить Т0 до 10 К. Затем теплообменный газ удаляется вакуумированием по линии 10, адсорбент адиабатически изолируется, начинается десорбция гелия откачкой его вакуумным насосом через линию 8; в результате в изолированном сосуде 2 (с адсорбентом) температура падает до Tх≈4,0 К при Т0=14…10 К.
Если вместо водорода использовать жидкий воздух или кислород (T0≈90 К), а вместо гелия – неон, то в интервале давлений 0,17–1,6 МПа можно достичь температуры Тх≈68 К (∆Τ=22 К).
Десорбционное устройство просто по конструкции; холодопроизводительность достаточно велика, однако в его классическом варианте (показанном на рис. 90) возможна реализация лишь периодического процесса без регенерации теплоты.
20. Процессы охлаждения, основанные на использовании свойств 4Не и 3Не.
Охлаждение растворением 3Не в 4Не. В 1951 г. Г. Лондон обосновал метод получения сверхнизких температур, основанный на использовании теплового эффекта при растворении жидкого 3Не в 4Не. Поглощение теплоты в процессе растворения возможно благодаря особым свойствам и характеру взаимодействия этих ожиженных изотопов. 4He имеет нулевой ядерный спин; его квантово-механическое описание подчиняется статистике Бозе–Эйнштейна. 3He имеет ядерный спин 1/2; поведение его следует статистике Ферми–Дирака. Этим объясняется различие свойств 3Не и 4Не.
В рассматриваемой области температур (<1 К) жидкий 4Не находится в сверхтекучем состоянии, имеет почти нулевую вязкость и энтропию, которая снижается пропорционально T3. Эта жидкость является инертной в гидродинамическом и тепловом отношении. Другому изотопу 3Не такое поведение несвойственно; он не переходит в сверхтекучее состояние вплоть до 3·10-3 К, его энтропия существенно выше, чем у 4Не. Теплоемкость 3Не также значительно больше теплоемкости 4Не. При растворении 3Не в 4Не атомы этих жидкостей не взаимодействуют между собой из-за инертности 4Не, следовательно, переход 3Не в объем, заполненный 4Не, где концентрация атомов 3Не мала, аналогичен процессу его расширения в пустоту, сопровождающемуся поглощением энергии. При этом в слабом растворе возникает как бы газообразная фаза из атомов 3Не, для которых 4Не является лишь поддерживающей средой.
Таким образом, процесс растворения приводит к изменению (уменьшению) упорядоченности системы в результате перехода жидкость–газ; энтропия 3Не возрастает. Растворение сопровождается поглощением теплоты перехода из одной фазы (чистый 3Не) в другую (слабый раствор 3Не), как и при испарении обычной жидкости. Растворение в адиабатных условиях приводит к охлаждению.
Охлаждение адиабатной кристаллизацией(эффект Померанчука). В 1950 г. И.Я. Померанчук предложил метод охлаждения, основанный на особых свойствах изотопа 3Не. Кривая плавления p=f(T), отражающая равновесие жидкой и твердой фаз для 3Не, имеет совершенно особый характер по сравнению с остальными веществами. При температуре 0,32 К и равновесном давлении 2,93 МПа кривая плавления 3Не имеет минимум. В этой точке энтропии твердой и жидкой фаз одинаковы и равны s=R×ln2. При дальнейшем снижении температуры ход изменения энтропии обеих фаз определяется особыми квантово-механическими свойствами 3Не. В обычных системах энтропия жидкости всегда больше энтропии кристалла, поскольку в кристалле упорядоченность выше. В 3Не при Т<0,32 К энтропия твердой фазы, наоборот, больше энтропии жидкости, которая имеет более высокую упорядоченность.
Вследствие этого переход жидкость–кристалл в результате сжатия при Т=const сопровождается скачком энтропии и поглощением теплоты Q. При адиабатных условиях (s=const) это приводит к снижению температуры.
Дата добавления: 2015-05-16; просмотров: 2203;
