Химические свойства.
Фенольный гидроксил – гидроксил, связанный с ароматическим циклом.
1. Кислотно–основные свойства обусловлены наличием в фенольном гидроксиле подвижного атома водорода. Электронная пара гидроксила смещена в сторону ароматического цикла, поэтому кислотные свойства более сильные, чем у спиртов. Так pKa угольной кислоты = 6,35, а pKa фенола = 9,89.
Фенолы растворяются в водных растворах щелочей с образованием фенолятов (феноксидов):

Однако кислотный характер фенолов выражен настолько незначительно, что даже такая слабая кислота как угольная, вытесняет фенолы из их солей:
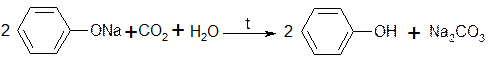
Поэтому фенолы, растворяясь в щелочах, не могут растворяться в карбонатах, т.к. освобождающаяся при этом угольная кислота тотчас же разлагает фенолят:
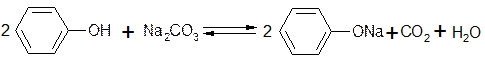
Это свойство фенолов отличает их от карбоновых кислот.
При повышении температуры реакция идет в прямом направлении. Феноляты щелочных металлов, как соли сильных оснований и слабых кислот, частично гидролизованы в водных растворах, поэтому растворы фенолятов обладают щелочной реакцией.
2. Реакция этерификации (аналогично спиртовому гидроксилу).
Образование простых эфиров – реакция фенолятов и галоидных алкилов (или алкилсульфатов).
C6H5ONa+JCH3®C6H5OCH3+NaJ
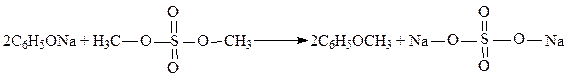 Сложные эфиры образуются при взаимодействии фенолятов натрия с ангидридами (или хлорангидридами кислот).
Сложные эфиры образуются при взаимодействии фенолятов натрия с ангидридами (или хлорангидридами кислот).
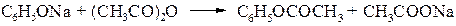
3. Окислительно – восстановительные свойства.
Фенолы проявляют сильные восстановительные свойства, очень легко окисляются даже слабыми окислителями, при этом образуются окрашенные соединения хиноидной структуры.
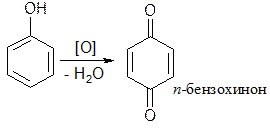
| [О] – CaOCl2, H2O2, Cl2, Br2 |
Примером реакции окисления является образование индофенолового красителя: образующийся хинон при взаимодействии с NH3 превращается в хинонимин, который взаимодействует с не прореагировавшим фенолом. В присутствии аммиака образуется индофенол, окрашенный в синий цвет.
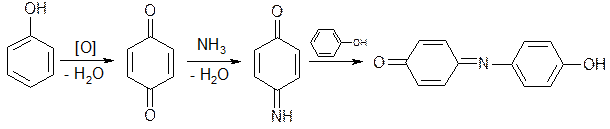
хинонимин индофенол
n-бензохинонимин
Разновидностью индофеноловой реакции является нитрозореакция Либермана, которая характерна для тех фенолов, у которых нет заместителей в орто- и пара-положениях.
При действии нитрита натрия в кислой среде образуется n-нитрозофенол, изомеризующийся в монооксим n-бензохинона, который затем, реагируя с избытком фенола в кислой среде, дает индофенол.
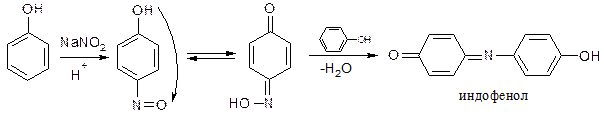
Наблюдается окрашивание, изменяющееся при добавлении раствора щелочи:
фенол – темно-зеленое, переходящее в вишнево-красное;
тимол – сине-зеленое, переходящее в фиолетовое;
резорцин – фиолетово-черное, переходящее в фиолетовое;
гексэстрол (синэстрол) – красно-фиолетовое, переходящее в вишневое.
4. Реакция комплексообразования с ионами железа.
В зависимости от количества фенольных гидроксилов, наличия в молекуле других функциональных групп, их взаимного расположения, pH среды, температуры, образуются комплексные соединения различного состава и окраски (исключение – тимол).
4.1.
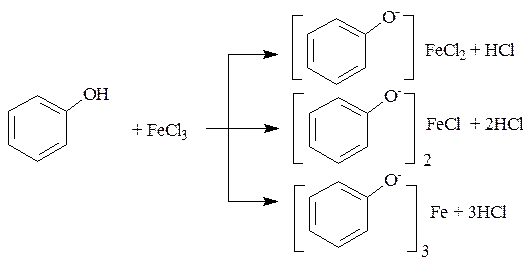
4.2.
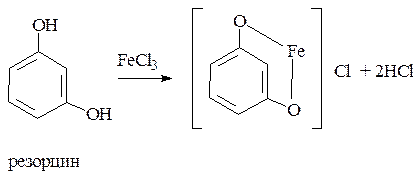
4.3.
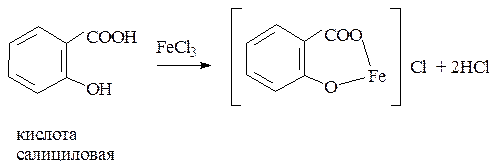
Комплексы окрашены:
фенол – синий цвет;
резорцин – сине-фиолетовый цвет;
кислота салициловая – сине-фиолетовый или красно-фиолетовый цвет;
осалмид (оксафенамид) – красно-фиолетовый цвет;
натрия пара-аминосалицилат – красно-фиолетовый цвет;
хинозол – синевато-зеленый цвет.
Реакция является фармакопейной для большинства фенольных соединений.
5. Реакции электрофильного замещения – SE атома водорода в ароматическом кольце (бромирование, конденсация с альдегидами, сочетание с солями диазония, нитрование, нитрозирование, йодирование и др.). Способность фенолов вступать в реакции электрофильного замещения объясняется взаимодействием неподеленной электронной пары атома кислорода с π-электронами бензольного кольца. Электронная плотность смещается в сторону ароматического кольца. Наибольший избыток электронной плотности наблюдается у атомов углерода в о- и n-положениях по отношению к фенольному гидроксилу (ориентанту I рода).
5.1. Реакция галогенирования (бромирование и йодирование).
5.1.1. При взаимодействии с бромной водой образуются белые или желтые осадки бромпроизводных.
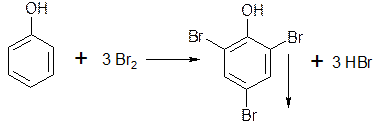
При избытке брома происходит окисление:
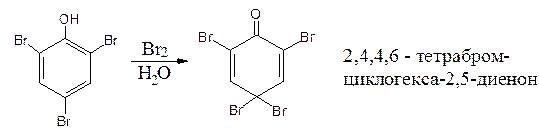
Реакция бромирования фенолов зависит от природы и положения заместителей.
Аналогично происходит йодирование, например:
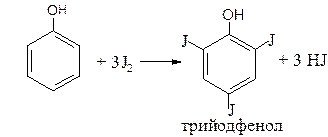
5.1.2. При наличии заместителей в о- и n-положениях ароматического кольца в реакцию вступают незамещенные атомы водорода ароматического кольца.
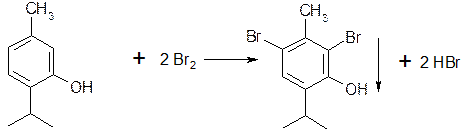
5.1.3. Если в о- и n-положениях по отношению к фенольному гидроксилу находится карбоксильная группа, то при действии избытка брома происходит декарбоксилирование:
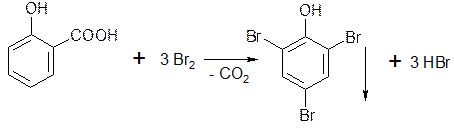
5.1.4. Если соединение содержит два фенольных гидроксила в м-положении, то при действии брома образуются трибромпроизводные (согласованная ориентация):
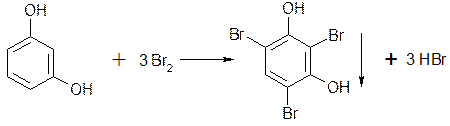
5.1.5. Если две гидроксильные группы расположены по отношению друг к другу в о- или n-положениях, то реакция бромирования не протекает (несогласованная ориентация)
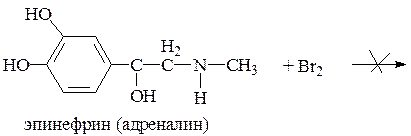
5.2. Реакции конденсации
5.2.1. С альдегидами.
Примером конденсации фенолов с альдегидами является реакция с реактивом Марки. При нагревании фенолов с раствором формальдегида в присутствии концентрированной H2SO4 образуются бесцветные продукты конденсации, при окислении которых получаются интенсивно окрашенные соединения хиноидной структуры. Серная кислота играет в данной реакции роль дегидратирующего, конденсирующего средства и окислителя.
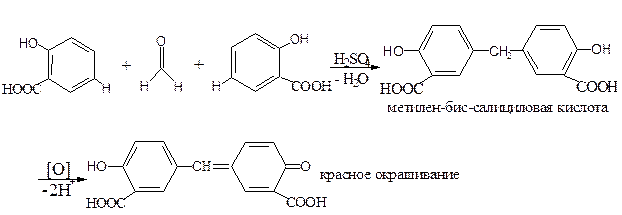
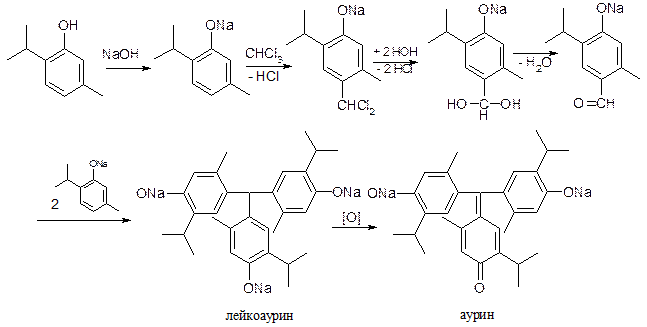
5.2.2. Реакция фенолов с хлороформом (CHCl3) с образованием ауриновых красителей.
При нагревании фенолов с CHCl3 в щелочной среде образуются аурины – трифенилметановые красители:
Аурины окрашены:
фенол – желтый цвет;
тимол – желтый цвет, переходящий в фиолетовый;
резорцин – красно-фиолетовый цвет.
5.2.3. С ангидридами кислот.
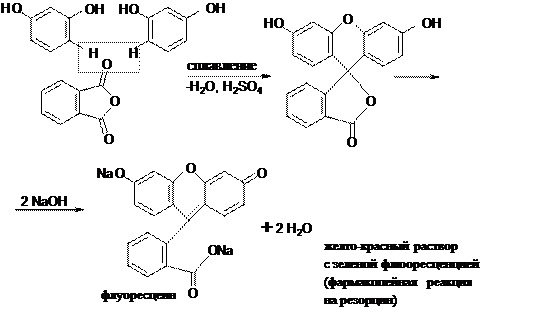
А. Реакция образования флуоресцеина (конденсация резорцина с фталевым ангидридом).
|

Б. Реакция образования фенолфталеина (конденсация фенола с фталевым ангидридом).
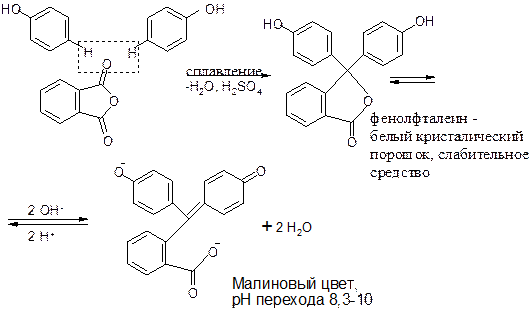
При большом избытке щелочи образуется трехзамещенная натриевая соль.
Конденсация тимола с фталевым ангидридом идет аналогично реакции образования фенолфталеина, образуется тимолфталеин, имеющий синее окрашивание в щелочной среде.
5.3. Реакция нитрования
Фенолы вступают в реакцию с разбавленной азотной кислотой (HNO3) и образуют орто- и пара-нитропроизводные. Добавление раствора натрия гидроксида усиливает окраску вследствие образования хорошо диссоциированной соли.
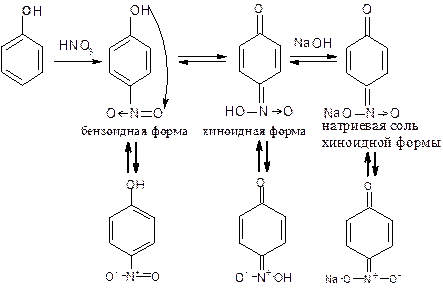
5.4. Реакция азосочетания фенолов с солью диазония в щелочной среде.
При взаимодействии фенолов с солью диазония при pH 9-10 образуются азокрасители, окрашенные в желто-оранжевый или красный цвет. Реакция азосочетания протекает в орто- и пара-положениях по отношению к фенольному гидроксилу. В качестве диазореактива обычно применяют диазотированную сульфаниловую кислоту.


В случае фенола


Дата добавления: 2015-04-29; просмотров: 8007;
