Виды взаимодействия частиц в кристаллах
1. Молекулярное взаимодействие (силы Ван-дер-Ваальса. Атомы инертных веществ)
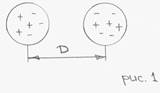
● в основе такого взаимодействия лежит явление поляризации (образование диполей), следовательно, электростатического притяжения;
● каждая частица окружает себя соседями, значит, укладка плотная;
● все соседи равноценны, т.е. связь ненаправленная;
● энергия связи мала (Есв ~ 0,1 кДж/моль);
● диэлектрики с низкой tпл.
2. Обменное взаимодействие (ковалентное)
Атомы IV и V групп: Si, Ge, C (4-валентные), Sb, Bi (5-валентные).
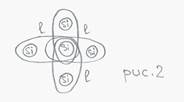
● в основе такого метода лежит обмен валентными электронами;
● число соседей точно известное и небольшое (3 или 4);
● соседи не равноценны, значит, связи направленные, Есв ~ 102 кДж/моль;
● очень твердые и очень хрупкие кристаллы;
● полупроводники и диэлектрики.
3. Ионное взаимодействие
Ме + нМе
Na – 1ē —> Na+
Cl + 1ē —> Cl-
● в основе взаимодействия лежит переход валентных электронов;
● число соседей большое;
● укладка плотная;
● связи ненаправленные, очень сильные, Есв ~ 102 кДж/моль;
● твердые кристаллы с высокой tпл;
● диэлектрики, полупроводники.
4. Металлическое взаимодействие
Все Ме.
● в основе лежит коллектив электронов, это облако электронов связывает все свободные элементы;
● укладка наиплотнейшая;
●связи ненаправленные, Есв ~ 10 кДж/моль;
●все Ме пластичные, прочные, электропроводны.
Выводы:
1. Различные виды взаимодействия имеют одинаковую электростатическую природу.
2. При электростатическом взаимодействии преобладают либо силы притяжения, либо силы отталкивания в зависимости от расстояния между частицами.
§2. Особенности расположения частиц в кристаллах
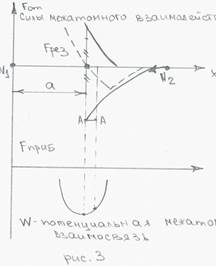
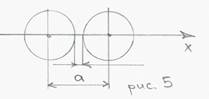
1. При электростатическом взаимодействии наиболее устойчивое положение занимает частица на определенном расстоянии а (когда Fпр = Fот), следовательно, расположение частиц в кристаллах должно быть регулярным.
2. При регулярном расположении части энергия межатомного взаимодействия будет минимальной. Кристаллы будут находиться в равновесии.
3. При любом смещении частицы от положения равновесия на ∆а на нее начинает действовать Fрезультир., значит, потенциальная энергия увеличивается на ∆W.
∆W = ∆а ● Fрезультир.
Кристалл будет находиться не в равновесии. У смещенных частиц будет более сильная межатомная связь, их труднее разорвать.
4. Регулярно расположенные частицы в пространстве образуют правильную кристаллическую решетку, но способ укладки у каждого вещества строго индивидуальный, значит, индивидуальны свойства.
§3. Элементарная ячейка кристаллической решетки
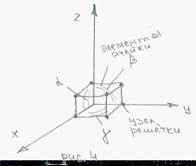
Элементарная ячейка – минимальный объем, который отображает положение частицы в кристалле.
- а, b, с – периоды решетки;
- α, β, γ – углы между осями.
Примечание:
Элементарная ячейка позволяет:
1. Задать направление.
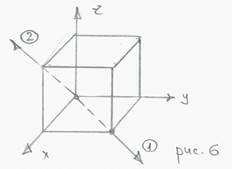
Направление задается тремя цифрами [U, V, W], где U, V, W координаты узла.
Координаты в периодах решетки
(1) [1; 1; 0],
(2) [1; 0; 1] <1; 1; 0> семейство равноценных направлений.
2. Задать любую плоскость.
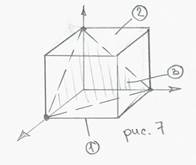
Любая плоскость задается тремя цифрами, которые называются индексами плоскости (h; k; l)
h = 1/m, k = 1/n, l = 1/p,
где m, n, p – отрезки, отсекаемые плоскостью по всем осям координат.
(1) m = 1, n = ∞, p = ∞;
h = 1, k = 0, l = 0. (1; 0; 0)
(2) (0; 0; 1)
(3) (1; 1; 1)
{1; 0; 0} – семейство равновесных плоскостей.
3. Определить плоскость укладки атомов (решетки Ме).
1) ОЦК – объемно-центрированный куб (W, V, Mo, Ta, Nb, Cr)
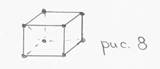
n = 2 =(1 + 8● 1/8)
k = 8
0.68
2) ГЦК – гранецентрированный куб (Ar, Pt, Au, Al, Cu, Ni)
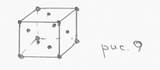
n = 4, k = 12, 0.74
3) Гексагональная (Mg, Be)
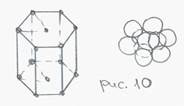
n = 6, k = 12, 0.74
Показатели:
- n – число атомов, приходящихся на одну ячейку;
- k – координационное число, число ближайших равноудаленных соседей;
- ГПУ – гексагональная плотноупакованная;
- коэффициент заполнения = Vатома/Vячейки
- два способа наиплотнейшего уложения атомов в ГЦК и ГПУ
§4. Влияние способов укладки на свойства кристаллов
Примеры:
1. Явление теплового расширения (при нагреве все кристаллические тела расширяются из-за усиления амплитуды колебания атомов). Чем плотнее уложены атомы в решетке, тем интенсивней тепловое расширение, αГЦК > αОЦК.
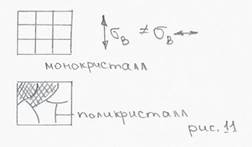
2. Явление анизотропии (различных свойств в кристаллической решетке в зависимости от направления). Чем симметричней решетка, тем меньше проявляется анизоропия (ОЦК – самая изотропная, ГПУ – самая анизотропная).
Примечание:
4. Явление полиморфизма (несколько решеток у одного и того же вещества)
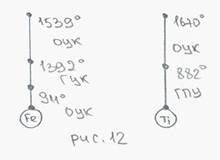
Благодаря полиморфизму:
1) в сплавах железа и титана можно используя быстрое охлаждение (закалку) получить необходимые структуры и особую прочность;
2) можно в некоторых сплавах получить явление памяти формы:
● при нагреве получить требуемую форму изделия

исходная кристаллическая решетка;
● с помощью деформации придать форму, удобную для применения
новая решетка подвержена влиянию деформации;
● при нагреве в условиях эксплуатации изделия принимать прежнюю форму
рис.15 (см. выше)
восстанавливается исходная решетка.
Применение:
- сосудорасширители (36,6°);
- датчики пожаротушения (40-50°);
- соединение термопроводников без сварки (комнатная температура);
- антенны (80-110°);
Чтобы реализовать явление памяти формы, нужно:
- специальные материалы, у которых решетка меняется при нагреве и деформации (полиморфные) – нитинолы - 50% Ni + 50%Ti + добавки;
- для получения третьей стадии памяти формы необходимо две стадии обработки.
Дата добавления: 2015-04-25; просмотров: 2294;
