Микроциркуляторное русло. Гистамин, ацетилхолин (спазм) Соединительнотканные тучные клетки, содержащие набор биологически активных веществ (гистамин
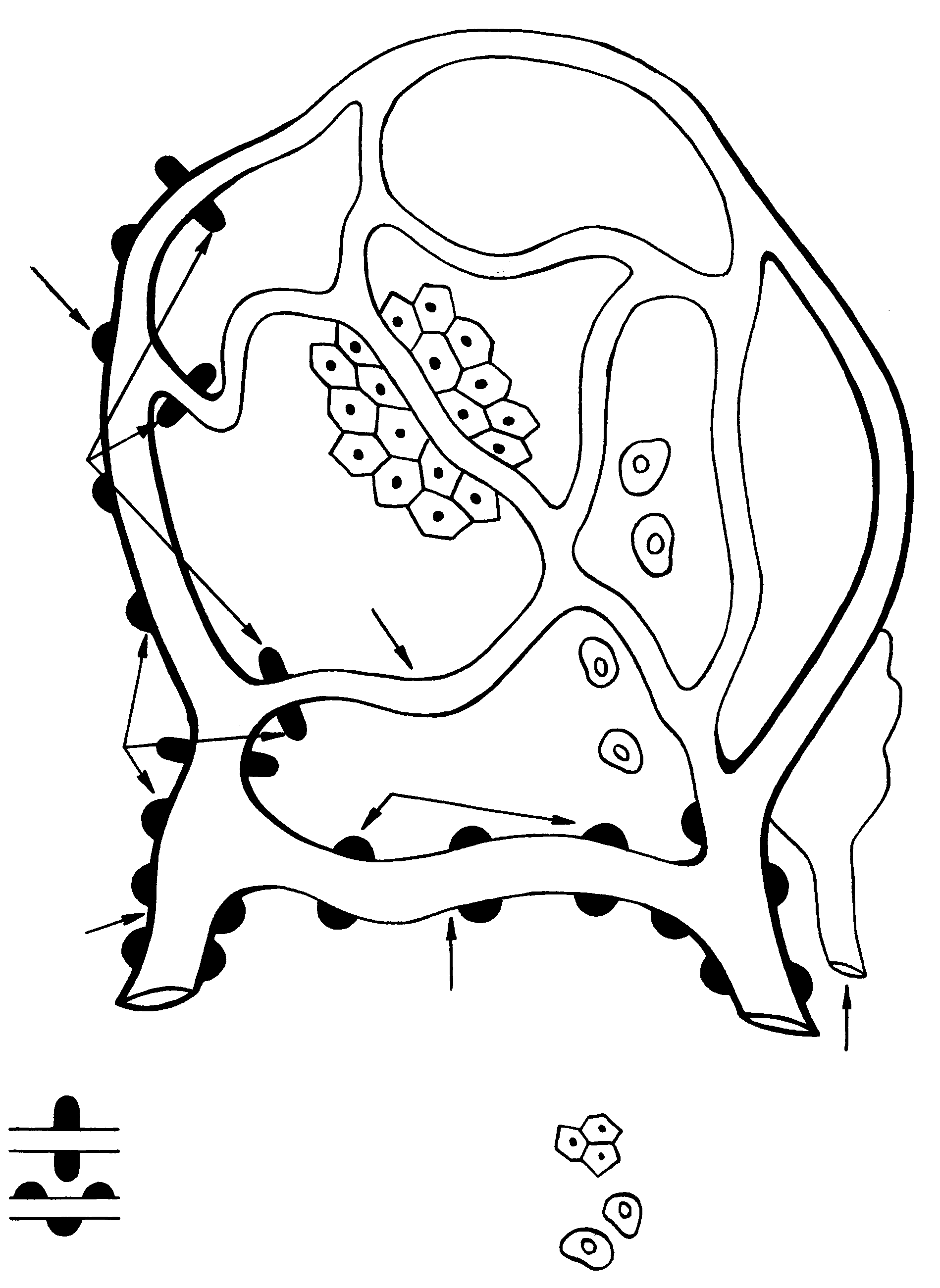
Рис.5
| Гистамин, ацетилхолин (спазм) |
| Соединительнотканные тучные клетки, содержащие набор биологически активных веществ (гистамин, серотонин и др.) |
| Паренхиматозные клетки |
| Венула |
| Артериола |
| Мышцы сосудов |
| Прекапиллярные сфинктеры |
| Прекапил-лярные сфинктеры |
| Норадреналин, адреналин (сужение) |
| Серотонин, простагландин F2 (сужение) |
| Лимфатический сосуд |
| Артериовенозный анастомозз |
| Гистамин (повышение проницаемости) |
| Гистамин, брадикинин, простагландин Е2 (расширение) |
| Капилляры |
Нарушения кровообращения в системе сосудов микроциркуляции всегда сопровождают расстройства общей и периферической гемодинамики. Наиболее распространенными из них являются стаз крови, сладж-феномен, централизация кровообращения и ДВС-синдром. Именно они опосредуют последующую метаболическую и структурно-функциональную патологию клеток.
Стаз крови представляет собой остановку кровотока в микрососудах органа или ткани. Различают истинный или первичный стаз и вторичный стаз.
Этиологическими факторами истинного стаза являются первичное повреждение эндотелия капилляров и форменных элементов крови, а также повышенная концентрация плазменных белков - гиперпротеинемия, вызванная обезвоживанием. Этиология вторичного стаза связана с ишемией или венозной гиперемией, в ходе которых вначале прекращается капиллярный кровоток, а уже потом происходит повреждение эндотелиальных и кровяных клеток.
Основупатогенеза, как первичного, так и вторичного стаза составляет повышение вязкости крови - сладж-феномен (от англ. Sludge – тина, ил, густая грязь). Механизмы сладжирования инициируются следующими факторами:
♦- эндотелиальными проагрегантами – АДФ, тромбоксаном А2, простагландинами F и Е, катехоламинами, агглютининами и др.;
♦- «перезарядкой» отрицательного мембранного заряда клеток крови локальным избытком катионов К, Са, Nа, Мg, возникающим при гибели клеток;
♦- «снятием» мембранного заряда форменных элементов крови амфотерными плазменными белками;
♦- повышением адгезивных свойств эндотелия и клеток крови, адсорбированными на их мембранах белками.
Реализация этих механизмов обеспечивает агрегацию и агглютинацию форменных элементов крови, образование их более или менее крупных конгломератов и фиксацию на поверхности сосудистой стенки. Быстрое устранение причин стаза восстанавливает капиллярный кровоток и не вызывает каких либо существенных последствий. Его неустранение обусловливает дистрофические изменения в тканях, а затем и их гибель (инфаркт).
«Централизация кровообращения» - феномен вызываемый сбросом крови в артериоло-венулярные анастомозы, минуя капиллярную сеть. Наиболее частой его причиной является эмоциональное стрессирование, сопровождающееся значительным повышением содержания в крови катехоламинов. Норадреналин и адреналин, стимулируя α-адренорецепторы прекапиллярных сфинктеров, вызывают их сокращение и закрытие просвета прекапилляров, блокируя поступление крови в капиллярную сеть. Вследствие этого кровь направляется в юкстакапиллярные анастамозы (Рис.4). Этот феномен призван обеспечить аварийное перераспределение крови из сосудистого бассейна кожи и пищеварительной системы в пользу жизненно важных органов – мозг, сердце, мышцы, легкие, не имеющих таких артериоло-венулярных шунтов.
Чрезмерно длительное симпатоадреналовое стрессирование способствует стойкой ишемии слизистой пищеварительной системы и является этиопатогенетическим механизмом гипоацидной язвы желудка.
4.2.5.1. Диссеминированное внутрисосудистое свертывание крови - ДВС синдром (тромбогеморрагический синдром – ТГС, коагулопатия потребления) представляет собой распространенное в системе микроциркуляции и цикличное нарушение в свертывающей и антисвертывающей системах крови. (диссеминированное) внутрисосудистое свертывание крови. Он может быть не только рассеянным, но и локальным, не только острым, но и хроническим. ДВС –синдром является опасным осложнением большого числа септических инфекций, неинфекционной патологии – массивных травм и ожогов, сосудистых заболеваний и кровопотерь, которые являются его этиологическимифакторами.
Патогенез ДВС-синдрома характеризуется тремя, чередующимися стадиями:
1. Стадия гиперкоагуляции или тромбоза начинается с массивного поступления в кровь из поврежденных тканей и агглютинированных тромбоцитов тканевого и тромбоцитарного тромбопластина – тромбокиназы. Тромбокиназа активирует плазменный каскадный механизм свертывания крови, в ходе которого факторы свертывания расходуются на образование многочисленных микротромбов.
2. Стадия коагулопатии потребления или геморрагическая характеризуется резким перевесом антисвертывающей - фибринолитической активности крови из-за повышенного потребления на формирование тромбов факторов свертывания. Она проявляется массивными геморрагиями и часто завершается летальным исходом.
3. Стадия остаточного тромбоза или восстановительная стадия характеризуется незначительным превалированием активности свертывающей системы крови над антисвертывающей и появлением в системе микрососудов отдельных тромбов.
При хронических и локальных формах ТГС последовательность этих периодов такая же, но они прогрессируют медленнее, а геморрагии проявляются периодически - толчками в момент активации фибринолиза.
Механизмы формирования ДВС-синдрома представлены на рис. 6.
Дата добавления: 2015-02-28; просмотров: 934;
