Тема 1. Вступ до курсу.
Схема установки для кондуктометричного титрування показана на рис. 9.
Розчин кислоти невідомої концентрації наливають в електрометричну комірку, яка складається з хімічної склянки 1 і вміщеного в неї магніта 2.
Оскільки титрування відбувається швидко, термостатування комірки не проводиться.
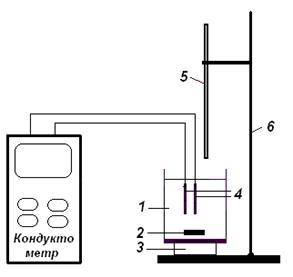
| У склянку поміщають досліджуваний розчин кислоти, ставлять на магнітну мішалку 3 і занурюють у розчин електроди 4 (графітові – N-5981 або платинові). Електроди повинні бути занурені так, щоб рівень рідини був приблизно на 1 см вище оголеної частини електродів (у разі необхідності додають дистильовану воду). Вмикають живлення електромішалки і регулюють її на помірне обертання магніта. Заповнюють бюретку 5 стандартним розчином NаОН і встановлюють рівень розчину на позначку “0”. |
| Рис. 9. Схема установки для кондуктометричного титрування |
Закріпляють бюретку в штативі 6 по центру комірки і під'єднують вилку електродів до кондуктометра.
Вмикають кондуктометр в мережу електричного струму і вимірюють електричну провідність згідно з інструкцією.
Відраховують і записують у таблицю покази кондуктометра W за шкалою 0 – 100 при об'ємі титранта 0 мл.
До розчину кислоти додають із бюретки по 0,5 мл розчину NaOH. Після встановлення стабільних показників значення електропровідності записують у таблицю.
Таблиця
| № | V(NaOH), мл | W, ум. одиниці |
Спочатку електрична провідність зменшується, а потім збільшується. Титрування припиняють після вимірювання 4 – 6 значень від початку збільшення електропровідності.
Після закінчення титрування вимикають живлення мішалки і кондуктометра. Від'єднують електроди від кондуктометра, виймають їх з електрометричної комірки, виливають із неї розчин, споліскують комірку і магніт дистильованою водою.
За отриманими даними будують графік у координатах W - V(NaOH) i розраховують вміст кислоти (мг) у розчині:
m(HCl) = C(NaOH)·V(NaOH) ·M(HCl).
Тема 1. Вступ до курсу.
Дата добавления: 2015-02-28; просмотров: 892;
