КАРДИОГЕННЫЙ ШОК
Шок — это клинический синдром, проявляющийся значительным снижением ударного и минутного сердечного выброса, которое не может быть компенсировано повышением сосудистого сопротивления.
Кардиогенный шок является одной из частых причин летального исхода при инфаркте миокарда. Он развивается на фоне выраженной сердечной недостаточности.
Это обычно происходит в первые часы возникновения инфаркта.Все усилия, направленные на лечение кардиогенного шока, нередко оказываются неэффективными. Некоторые авторы считают, что применение стрептокиназы и других фибринолитических средств, а также баллонной ангиопластики в первые 4 ч развития инфаркта миокарда существенно улучшает прогноз [Сыркин А.Л., 1991].
Диагноз основывается на характерном симптомокомплексе, отражающем нарушение перфузии тканей как в отдельных органах, так и в организме в целом.
Клиническая картина типична: заостренные черты лица, серовато-бледные, иногда с цианотичным оттенком кожные покровы, холодные, покрытые липким потом; адинамия, больной почти не реагирует на окружающее. Пульс частый, нитевидный, иногда не прощупывается. АД нередко ниже 80 мм рт.ст., но у больных с исходной артериальной гипертензией симптомы шока могут появляться и при нормальных показателях систолического АД (95—120 мм рт.ст.). Пульсовое давление — 20—25 мм рт.ст. и ниже. Характерным симптомом, опасным в прогностическом отношении, является олигурия (анурия) до 20 мл в час и менее. К признакам шока относят метаболический ацидоз.
Исходя из особенностей возникновения кардиогенного шока, его клинической картины и эффективности лечения, выделяют следующие его формы: рефлекторный, истинный кардиогенный, ареактивный, аритмический [Чазов Е.И., 1982].
Рефлекторный шок. Развитие этой формы шока обусловлено рефлекторными изменениями и выраженным болевым синдромом, вызывающими нарушение регуляции сосудистого тонуса с последующим депонированием крови в сосудах и выход жидкой фракции крови в интерстициальное пространство, что приводит к уменьшению венозного притока к сердцу. Вследствие патологических рефлекторных влияний, особенно при инфаркте миокарда задней стенки, может развиться синусовая брадикардия, что ведет к значительному сокращению МОС, снижению АД (до 90—100 мм рт.ст.), уменьшению ОПСС.
У больных с этой формой шока достаточный и быстрый эффект достигается адекватным обезболиванием и введением сосудистых средств (симпатомиметиков). Для обезболивания применяют наркотические анальгетики и препараты для нейролептаналгезии. Из симпатомиметиков чаще всего применяют 1 % раствор мезатона (0,3—0,5— 1 мл) или 0,2 % раствор норадреналина (2—4 мл) внутривенно капельно на изотоническом растворе натрия хлорида или 5 % растворе глюкозы методом титрования, или вводят 25 мг допамина в 125 мл изотонического раствора натрия хлорида. При брадикардии показано внутривенное введение 0,5—1 мл 0,1 % раствора атропина. Чтобы увеличить приток крови к сердцу, следует приподнять ноги больного на 15—20°. Проводят оксигенотерапию через носовой катетер или маску.
Для повышения ОЦК, притока крови к сердцу, давления наполнения -левого желудочка, СВ и ликвидации артериальной гипотензии показано ведение кровезаменителей. Предпочтительно использование реополиглюкина (200—400 мл со скоростью 20 мл/мин). Он улучшает реологические свойства крови и микроциркуляцию. Проводят тромболитическую юрапию.
Истинный кардиогенный шок. В развитии этой формы шока основное значение приобретает резкое падение пропульсивной (сократительной) функции левого желудочка. Уменьшение МОС не компенсируется повышением ОПСС, что приводит к снижению АД. Систолическое АД ниже 90 мм рт.ст., у больных с артериальной гипертензией — ниже 100 мм рт.ст.; пульсовое давление меньше 20 мм рт.ст. Возникают глубокие нарушения кровообращения во всех органах и тканях, развивается олигурия, анурия.
При лечении этой формы кардиогенного шока проводят в первые часы от начала инфаркта миокарда обезболивающую и тромболитическую терапию, применяют лекарственные препараты, обладающие положительным инотропным действием (в первую очередь — катехоламины). Норадреналин в малых дозах оказывает преимущественно инотропное действие на миокард, а в высоких дозах — сосудосуживающее. Вводят препарат внутривенно капельно 1—2 мг (0,5—1 мл 0,2 % раствора) в 200 мл изотонического раствора хлорида натрия или 5 % раствора глюкозы. Скорость введения регулируется в зависимости от уровня АД (среднее АД = 80—90 мм рт.ст.) и ритма сердца. АД не должно быть выше 110— 115 мм рт.ст. (у больных с предшествующей стойкой и высокой гипертензией — 130—140 мм рт.ст.). Средние дозы норадреналина от 4 до 16 мкг/мин. Показанием к его применению является кардиогенный шок с низким ОПСС.
При кардиогенном шоке эффективен также допамин, оказывающий положительное инотропное действие и уменьшающий сопротивление коронарных, мозговых, почечных и мезентериальных сосудов. Вводят его внутривенно капельно со скоростью 2—10 мкг/кг/мин под мониторным наблюдением, так как он может вызвать аритмию. Допамин разводят из расчета 25 мг на 125 мл или 200 мг на 400 мл 5 % раствора глюкозы или изотонического раствора, т.е. в 1 мл раствора 200 или 500 мкг допамина. Начальная скорость введения 1—5 мкг/кг/мин (~200 мкг/мин).
У больных с не очень выраженной степенью гипотензии может оказаться полезным добутамин, который является синтетическим симпатомиметическим амином, оказывающим в обычных дозах (2,5—10 мкг/кг/мин) минимальное положительное инотропное и периферическое сосудосуживающее действие. Его не следует использовать в тех случаях, когда желательно добиться сосудосуживающего эффекта, и необходимо применять тогда, когда нежелательно положительное хронотропное действие (мало влияет наЧСС). Начальная скорость внутривенного введения 2,5 мкг/кг/мин каждые 15—30 мин, максимальная скорость инфузии 10—15 мкг/кг/мин.
Сердечные гликозиды при кардиогенном шоке у больных инфарктом миокарда малоэффективны. Не оправдано и применение кортикостероидов.
При безуспешности лекарственной терапии «истинного» кардиогенного шока необходимо проводить контрапульсацию. Важный метод лечения этого вида шока — восстановление кровотока по окклюзированной венечной артерии (тромболизис, транслюминальная ангиопластика).
Ареактивный шок. О наличии этой формы шока говорят в тех случаях, когда введение возрастающих доз норадреналина или гипертензина в течение 15—20 мин не ведет к повышению АД. В настоящее время не удается достаточно эффективно лечить таких больных, что обусловливает их высокую смертность.
Аритмический шок. У больных отмечается четкая связь падения АД и появления периферических симптомов шока с нарушениями ритма и проводимости. При восстановлении сердечного ритма, как правило, исчезают и признаки шока. Первостепенная задача лечения — восстановление нормальной частоты желудочковых сокращений.
В остром периоде инфаркта миокарда аритмии возникают практически у каждого больного. Для профилактики желудочковых аритмий наиболее эффективен лидокаин. Вводят его внутривенно в первоначальной дозе 100—120 мг (5—6 мл 2 % раствора), а затем внутривенно капельно со средней скоростью 1—4 мг/мин. При необходимости показано повторное струйное введение 60—100 мг лидокаина. Эту же дозу вводят при рецидиве экстрасистолии. Некоторые авторы указывают на прямое антигипоксическое действие лидокаина путем стабилизации клеточных мембран кардиоцитов. Лидокаин оказывает очень слабое отрицательное инотропное влияние, при этом АД и СВ существенно не меняются. Суточная доза — не более 2—3 г (у больных старше 70 лет при кардиогенном шоке, недостаточности кровообращения и нарушениях функции печени дозы лидокаина уменьшают вдвое).
При неэффективности лидокаина можно применить новокаинамид до 1 г под контролем ЭКГ и АД после каждых 100 мг (1 мл 10 % раствора) либо блокаторы бета-адренорецепторов (индерал из расчета 1 мг на 10 кг массы тела) внутривенно.
В последнее время считают, что лечение аритмий лучше начинать с быстрого определения и коррекции электролитных нарушений — гипокалиемии и гипомагнезиемии. При гипокалиемии (уровень К+ менее 3,5 ммоль/л) 10 ммоль хлорида калия растворяют в 50—100 мл раствора глюкозы и вводят внутривенно капельно в течение 30 мин. Введение этой дозы повторяется каждый час до достижения уровня K+ в плазме 4—4,5 ммоль/л. Меньшая степень гипокалиемии может быть скорригирована с помощью оральной терапии. При гипомагнезиемии (уровень Mg++ в плазме крови менее 0,7 ммоль/л) 1—2 г сульфата магния разводят в 50—100 мл изотонического раствора натрия хлорида и вводят в течение 50—60 мин, затем — от 0,5 до 1 г каждый час до 24 ч. Скорость и продолжительность инфузии зависят от клинической картины или степени магнезиемии. Введение раствора сульфата магния безопасно и сокращает частоту желудочковых аритмий.
Новый метод антиаритмической защиты миокарда при инфаркте миокарда — внутривенное лазерное облучение крови гелий-неоновым лазером. Его применяют в остром периоде заболевания. Лазерное облучение крови дает анальгетический эффект, уменьшает количество желудочковых экстрасистол более чем на 90 % и приводит к быстрой положительной динамике на ЭКГ.
Аритмии, наиболее опасные для жизни больного:
• желудочковая тахикардия (рис. 15.1), которая может перейти в ФЖ. При длительной ЖТ применяют препараты, дающие мембранный эффект. Препаратом выбора является лидокаин с последующей его комбинацией с пропранололом или проксинамидом. Если аритмия сохраняется и имеются нарушения гемодинамики, проводят электроимпульсную терапию (дефибрилляцию);
• фибрилляция (мерцание) желудочков (рис. 15.2). Для прекращения фибрилляции проводят немедленную электродефибрилляцию, которая эффективна лишь при тонической (высокоамплитудной) фибрилляции. С целью перевода атонической (низкоамплитудной фибрилляции) в тоническую внутривенно вводят адреналин в дозе 0,3—0,5 мл 0,1 % раствора. Для обеспечения хорошей оксигенации и перфузии миокарда перед дефибрилляцией необходимо проведение адекватной вентиляции кислородом и наружного массажа сердца. Кардиоверсия осуществляется постоянным током, начиная с 50 Дж, при отсутствии эффекта увеличивают разряд каждый раз на 50 Дж;
• желудочковые экстрасистолы очень опасны для жизни больного, так как могут переходить в мерцание и трепетание желудочков. Существует большая опасность развития ЖТ и ФЖ при выявлении одного или нескольких следующих критериев:
1) частота желудочковых экстрасистол 6 и более в 1 мин (рис. 15.3);
2) политопные экстрасистолы (рис. 15.4);
3) групповые желудочковые экстрасистолы (рис. 15.5; 15.6; 15.7);
4) ранние желудочковые экстрасистолы типа «R и Г» (рис. 15.8).
Внутривенное введение лидокаина является методом выбора при желудочковых экстрасистолиях и аритмиях. Препарат начинает действовать быстро и так же быстро исчезают его эффекты (в течение 15—20 мин после введения). Для быстрого достижения эффекта препарат вводят внутривенно болюсно из расчета 1 мг/кг. Для поддержания эффекта проводят постоянную инфузию лидокаина из расчета 2—4 мг/мин. Если аритмия сохраняется, то через 10 мин после введения первого болюса вводят второй в дозе 0,5 мг/кг.При застойной сердечной недостаточности дозу лидокаина уменьшают вдвое. Эффект наступает через 72—96 ч. Общая доза лидокаина до 2000 мг/сут.
Синусовая брадикардия. Мнения о значении брадикардии как фактора, предрасполагающего к развитию фибрилляции желудочков, противоречивы. Синусовая брадикардия, возникающая в первые часы острого инфаркта миокарда, может привести в последующем в отличие от брадикардии, возникающей в более поздние сроки острого инфаркта миокарда, к появлению эктопических желудочковых ритмов. Лечение синусовой брадикардии проводят в тех случаях, когда она вызывает нарушения гемодинамики или когда на ее фоне развивается выраженная эктопическая активность желудочков. Для ускорения синусового ритма используют атропин (внутривенно в дозе 0,4—0,6 мг). Если пульс сохраняется менее 60 в минуту, возможно повторное введение атропина по 0,2 мг до тех пор, пока общая доза не составит 2 мг. Но необходимо помнить, что атропин может усугублять ишемию или вызывать желудочковую тахикардию или фибрилляцию. При стойкой брадикардии (менее 40 в минуту), латентной к введению атропина, требуется проведение электрической стимуляции сердца. Временная терапия чрескожной или чреспищеводной кардиостимуляцией, инфузией допамина или эпинефрина может быть необходима при слишком медленном сердечном ритме для поддержания адекватного СВ. Наиболее эффективной у таких больных является трансвенозная электрокардиостимуляция.
Нарушения проводимости встречаются при инфаркте миокарда довольно часто, особенно в 1—2-й день болезни. Они могут возникать на различных уровнях проводящей системы сердца: в области предсердно-желудочкового узла, предсердно-желудочкового пучка (пучок Гиса) или в более дистальных отделах проводящей системы. Ишемия предсердно-желудочкового узла обычно встречается при инфаркте миокарда правого желудочка, потому что данный узел снабжается кровью через правую коронарную артерию. Это может привести к атриовентрикулярной блокаде разной степени, вплоть до полной, резистентной к атропину. В подобной ситуации необходима последовательная атриовентрикулярная электростимуляция, в то время как электростимуляции желудочка следует избегать из-за отсутствия эффекта и возможного вреда.
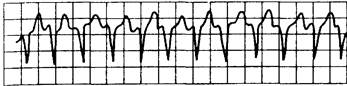
Рис. 15.1. Желудочковая тахикардия.
Зубцы Р не выявляются, комплексы QRS имеют патологическую форму.
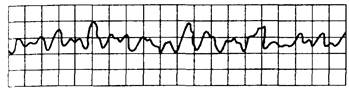
Рис. 15.2. Мерцание (фибрилляция) желудочков.
Синусоида нерегулярная, неритмичная; комплексы QRST отсутствуют, частота волн мерцания более 250 в минуту.
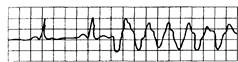
Рис. 15.3. Три и более (обычно до 9) последовательных желудочковых экстрасистол.
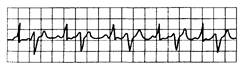
Рис. 15.4. Бигеминия: каждый синусовый импульс сопровождается преждевременным желудочковым комплексом (экстрасистолой).
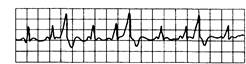
Рис. 15.5. Тригеминия: за каждыми двумя синусовыми сокращениями следует экстрасистола.
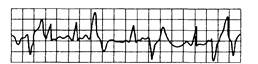
Рис. 15.6. Мультиформные желудочковые экстрасистолы.
Морфологически различные преждевременные желудочковые комплексы (экстрасистолы).
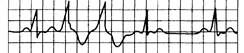
Рис. 15.7. Спаренные желудочковые экстрасистолы.
Две последовательные экстрасистолы за синусовым ритмом.
|
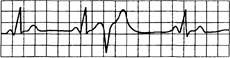
Рис. 15.8. Желудочковые экстрасистолы типа «R на Т».
Комплекс QRS экстрасистолы наслаивается на вершину или нисходящее колено предшествующего зубца Т.
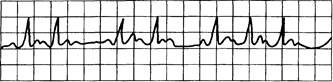
Рис. 15.9. АВ-блокада II степени (Венкебаха, Мобиц-1).
Постоянное удлинение интервала PQ с выпадением комплекса QRST; интервалы R—R прогрессивно укорачиваются; Р—Р — относительно постоянны.
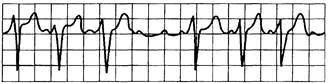
Рис. 15.10. АВ-блокада II степени (Мобиц-II).
Интервалы PQ постоянные, могут быть удлиненными, выпадение желудочковых комплексов QRST, длинные паузы равны удвоенному интервалу Р—Р; Р : QRS = 3:2; 4:3; 5:4.
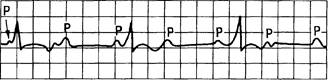
Рис. 15.11. АВ-блокада III степени (полная).
Интервалы R—R и Р—Р постоянные; частота Р больше частоты комплексов QRS, комплексы (?/?5'нормальной продолжительности или расширены и деформированы.
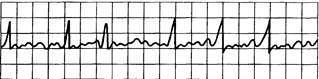
Рис. 15.12. Мерцание (фибрилляция) предсердий.
Отсутствие четких зубцов Р, комплексы QRS неправильной формы, частоты и вольтажа. Частота сокращения предсердий около 350 и более в минуту.
Наиболее опасные нарушения проводимости сердца:
• блокада сердца II степени (промежуточная атриовентрикулярная блокада) возникает в том случае, когда часть импульсов не достигает желудочков. АВ-блокада типа Мобиц I (АВ-блокада Венкебаха) является следствием нарушения проводимости на уровне предсердно-желудочкового узла (рис. 15.9). В редких случаях блокада типа Мобиц I может прогрессировать до полной блокады сердца.
АВ-блокада типа Мобиц II (рис. 15.10) имеет тенденцию к прогрессированию вплоть до полной блокады сердца. Подчиненный водитель ритма, включающийся в нижних отделах системы Гиса—Пуркинье вследствие ускользания, обладает нестабильным, медленным ритмом. Прогноз часто неблагоприятный. В этом случае показана имплантация кардиостимулятора.
• АВ-блокада III степени (рис. 15.11) характеризуется тем, что ни один предсердный импульс не поступает к желудочкам. Полная АВ-блокада представляет значительную опасность для жизни больного. Клинически может проявляться аритмогенным шоком или приступами Морганьи—Адамса—Стокса, одним из проявлений которого является потеря сознания. Приступы чаще всего возникают в результате длинной предавтоматической паузы при переходе от неполной АВ-блокады к полной. Происходит резкое замедление деятельности сердца до полной его остановки, наступает гипоксия мозга или появляются групповые политопные экстрасистолы с переходом в трепетание и мерцание желудочков. При АВ-блокаде III степени наиболее эффективна трансвенозная электрокардиостимуляция.
• Пароксизмальная предсердная тахикардия, трепетание и мерцание предсердий (рис. 15.12) при инфаркте миокарда встречаются редко. При мерцании (фибрилляции) предсердий могут возникать заметные расстройства гемодинамики, обмороки, сердечная недостаточность. При нестабильной гемодинамике показано устранение мерцания и трепетания предсердий путем срочной кардиоверсии или электростимуляции предсердий с частотой, превышающей частоту трепетания предсердий. Кардиоверсию проводят одиночным импульсом постоянного тока (заряд 200 Дж и менее).
Дата добавления: 2015-02-23; просмотров: 1161;
