Озонирование
Впервые этот способ обработки воды был опробован во Франции, где начали проводить опыты в 1886 г. В России в 1901 г. на Пятом водопроводном съезде было принято постановление "Об испытании способа озонирования в России в применении к делу снабжения городов речными и поверхностными водами". В 1905 г. уже действовала экспериментальная установка на невской воде при Петропавловской больнице.
В результате принятых постановлений на русских водопроводных съездах (V в 1901 г. и VII в 1907 г.) на Главной водопроводной станции Петрограда в 1911 г. была введена первая и самая крупная в мире производственная установка с производительностью 56 тыс. м3/сут. И только через 40 лет во Франции заработала более крупная озонаторная станция Сен-Мор (Париж). В 1974 г. она обрабатывала 300 тыс. м3/сут, т. е. 30% всей воды, необходимой Парижу. Станция была оборудована пластинчатыми озонаторами фирмы "Отто". В 1965 г. были разработаны трубчатые озонаторы, более пригодные для больших станций. Фирма "Трейлигаз" (Франция) значительно увеличила их производительность (800 тыс. м3/сут – Шаузи ле Руа; 300 м3/сут – в Орли). В настоящее время около полутора тысяч водоочистных станций городов Европы оборудованы озонаторными установками.
Молекула озона неустойчива и диссоциирует на молекулу и атом кислорода. Эта реакция экзотермическая, чем и объясняется взрывоопасностьозона при его концентрации в озоно-кислородной или озоно-воздушной смеси более 10% (15–20%). Озон весьма токсичен: предельное содержание его в воздухе помещений, где находятся люди, соответствует 0,1 мг/м3, а концентрация 0,018 г/м3 вызывает удушье.
Схема процессов, происходящих при добавлении озона в воду приведена на рис. 12.1.*
______________________
* В. Ф. Кожинов, И. В. Кожинов. Озонирование воды. М., Стройиздат, 1974 г.-160 с.
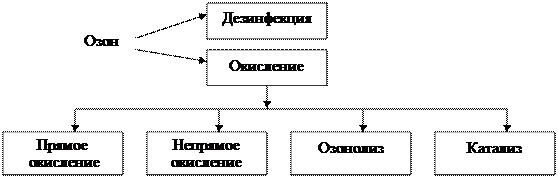 |

Рис. 12.1
Прямое окисление – это окисление озоном веществ до окислов вида
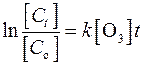 ,
,
где 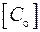 и и 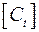 – –
| соответственно начальная и конечная концентрация вещества, мг/л; |
| k – | константа скорости реакции; |
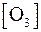 – –
| средняя концентрация озона в процессе реакции окисления, мг/л; |
| t – | продолжительность озонирования, с. |
Непрямое окисление – это окисление образующимися активными радикалами, например, ОН– и др., которые образуются при переходе озона из газовой фазы в жидкость и при его саморазложении.
Процесс замедляется с увеличением загрязняющих веществ в обрабатываемой воде. Непрямому окислению чаще подвергаются органические кислоты с небольшим молекулярным весом.
В ряде случаев может применяться прямое и непрямое окисление, происходящее последовательно или одновременно (параллельно).
При озонолизе происходит сорбция озона на двойных и тройных углеродных связях с дальнейшим разрушением этих связей и образованием озонидов, которые также разлагаются.
Катализ– действие озона, усиливающее окисляющую способность кислорода. При распаде озона в щелочной среде образуется озонидный ион-радикал 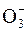 . По мере распада
. По мере распада 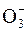 в водном растворе может накапливаться супероксидный ион-радикал
в водном растворе может накапливаться супероксидный ион-радикал 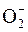 , который также нестабилен и разлагается до пероксида водорода.
, который также нестабилен и разлагается до пероксида водорода.
И, наконец, обеззараживание воды озоном и сопутствующими ему соединениями происходит путем непосредственного влияния на цитоплаз-
му и ядро живой клетки бактерии, что угнетает и прекращает активность обмена веществ в ее клетке. Уничтожение вирусов происходит при полном окислении их материи, состоящей из белка и нуклеиновой кислоты.
Озон обеззараживает воду быстрее хлора в 15 раз. Время контакта определено для хлора (ГПХ, хлорной извести) – 30 мин, для озона – 12 мин.
При обработке цветных вод дозами озона (до 3–5 мг/л), необходимыми для дезинфекции воды, образуются полупродукты окисления, часть из которых токсичны (альдегиды: глиоксаль, метилглиоксаль; формальдегид (ПДК = 0,05 мг/л), муравьиная кислота, бензальдегид – 0,003 мг/л, ацетальдегид – 0,2 мг/л). При наличии в воде некоторых типов пестицидов при озонировании образуются сверхтоксичные продукты окисления, которые не поддаются дальнейшему разрушению озоном и другими реагентами.
Для полного окисления примесей воды (и без образования вторичных загрязнений) требуется 1,1…1,5 мг озона на 1 мг перманганатной окисляемости воды. При цветности воды 70…100° ее окисляемость составляет едва ли ~ 20 мг О2/л при минимально необходимой дозе озона 22–30 мг/л, что совершенно неприемлемо в практике водоподготовки.
Известно, что озон не обладает пролонгированным действием в сети трубопроводов и при дополнительном хлорировании воды перед подачей в сеть концентрация формальдегида может увеличиться в сети до трех раз. При этом образуются хлорцианы и хлоргидраты[2], а при биоразложении альдегидов происходит биообрастание трубопроводов и вторичное ухудшение микробиологических показателей воды. При наличии в воде подземных источников, например бромидов, при озонировании образуются бромсодержащие тригалометаны (в том числе бромоформ), броматы (бромат-ионы – ПДК = 0,01 мг/л при одновременном использовании хлор- и аммиаксодержащих реагентов при дезинфекции).
Таким образом, применение озона для обеззараживания питьевой воды далеко не однозначно в связи с образованием побочных продуктов, отрицательно влияющих на здоровье человека, и может провоцировать интенсивный бактериальный рост в воде, т. к. образуются продукты окисления, являющиеся более биоразлагающимися, чем исходные вещества. Кроме того, здесь особо необходимо подчеркнуть мутагенный характер воздействия формальдегида на человека и малую сорбционную емкость по формальдегиду активированных углей, применяемых как безопасный способ.
Дата добавления: 2015-02-19; просмотров: 2102;
