Теплоемкость твердых тел. В качестве модели твердого тела рассмотрим правильно построенную кристаллическую решетку, в узлах которой частицы (атомы
В качестве модели твердого тела рассмотрим правильно построенную кристаллическую решетку, в узлах которой частицы (атомы, ионы, молекулы), принимаемые за материальные точки, колеблются около своих положений равновесия — узлов решетки — в трех взаимно перпендикулярных направлениях. Таким образом, каждой составляющей кристаллическую решетку частице приписывается три колебательных степени свободы, каждая из которых, согласно закону равнораспределения энергии по степеням свободы (см. § 50), обладает энергией kT. Внутренняя энергия моля твердого тела
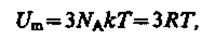
где NA— постоянная Авогадро; NAk = R (R— молярная газовая постоянная). Молярная теплоемкость твердого тела
 Дж/(моль-К), (73.1)
Дж/(моль-К), (73.1)
т. е. молярная (атомная) теплоемкость химически простых тел в кристаллическом состоянии одинакова (равна 3.R) и не зависит от температуры. Этот закон был эмпирически получен французскими учеными П. Дюлонгом (1785—1838) и Л. Пти (1791—1820) и носит название закона Дюлонга - Пти.
Если твердое тело является химическим соединением (например, NaCl), то число частиц в моле не равно постоянной Авогадро, а равно nNФ, где п — число атомов в молекуле (для NaCl число частиц в моле равно 2NA, так, в одном моле NaCl содержится NА атомов Na и NA атомов С1). Таким образом, молярная теплоемкость твердых химических соединений
Сv = 3nR ≈ 25n Дж/(моль×К),
т. е. равна сумме атомных теплоемкостей элементов, составляющих это соединение.
Таблица 4
| Вещество | С, Дж/(моль-К) | |
| Теоретическое значение | Экспериментальное значение | |
| Алюминий А1 Алмаз С Бериллий Be Бор В Железо Fe Серебро Ag NaCl AgCl СаCl2 | 25,5 5,9 15,6 13,5 26,8 25,6 50,6 50,9 76,2 |
Как показывают опытные данные (табл. 4), для многих веществ закон Дюлонга и Пти выполняется с довольно хорошим приближением, хотя некоторые вещества (С, Be, В) имеют значительные отклонения от вычисленных теплоемкостей. Кроме того, так же как и в случае газов (см. § 53), опыты по измерению теплоемкости твердых тел при низких температурах показали, что она зависит от температуры (рис. 113). Вблизи нуля кельвин теплоемкость тел пропорциональна Т3,и только при достаточно высоких температурах, характерных для каждого вещества, выполняется условие (73.1). Алмаз, например, имеет теплоемкость, равную 3К при 1800 К! Однако для большинства твердых тел комнатная температура является уже достаточно высокой.

Рис. 113
Расхождение опытных и теоретических значений теплоемкостей, вычисленных на основе классической теории, объяснили, исходя из квантовой теории теплоемкостей, А. Эйнштейн и П. Дебай.
Дата добавления: 2015-02-13; просмотров: 957;
