Нервно-мышечные заболевания пищевода. К нервно-мышечным заболеваниям относят кардиоспазм, ахалазию кардии, диффузный эзофагоспазм (синдром Барсони-Тешендорфа) и некоторые другие моторные
К нервно-мышечным заболеваниям относят кардиоспазм, ахалазию кардии, диффузный эзофагоспазм (синдром Барсони-Тешендорфа) и некоторые другие моторные расстройства, связанные с нарушением иннервации пищевода.
Нервно-мышечные заболевания - наиболее часто встречающаяся после рака и Рубцовых стриктур патология пищевода.
При ахалазии кардииотмечается отсутствие расслабления нижнего пищеводного сфинктера во время акта глотания.
Выключение физиологического рефлекса раскрытия нижнего пищеводного сфинктера приводит к нарушению тонуса и моторики пищевода, что вызывает задержку пищи.
Кардиоспазм- стойкое спастическое сужение терминального отдела пищевода, проявляющееся дисфагией и в далеко зашедших стадиях сопровождающееся органическими изменениями его вышележащих отделов.
Этиология и патогенез нервно-мышечных заболеваний пищевода окончательно не выяснены.
Существуют теории врождённого спазма, патологических изменений в окружающих органах, инфекционная, рефлекторная, психогенная и др.
В последнее время большое значение в развитии этих заболеваний придаётся снижению содержания оксида азота, что приводит к нарушениям обмена ионов кальция и передачи нервно-мышечного импульса.
В настоящее время кардиоспазм и ахалазия кардии рассматриваются как два различных патологических процесса, входящих в группу нервно-мышечных заболеваний.
При кардиоспазме наблюдается повышенное давление в зоне нижнего пищеводного сфинктера, градиент пищеводно-желудочного давления может достигать 20 мм рт. ст. и более при норме 10 ± 3 мм рт. ст.
Для начальных стадий кардиоспазма характерна усиленная непропульсивная моторика пищевода.
Морфологически находят дегенеративно-дистрофические изменения в преганглионарных нейронах дорсальных ядер блуждающих нервов и в меньшей степени - постганглионарных нейронах ауэрбахова сплетения пищевода.
Считается, что в связи с нарушением центральной иннервации при кардиоспазме гладкая мускулатура нижнего пищеводного сфинктера становится более, чем обычно, чувствительной к своему физиологическому регулятору - эндогенному гастрину.
Таким образом, при данном варианте течения заболевания наблюдается истинный спазм кардии.
При ахалазии кардии, напротив, поражаются преимущественно постганглионарные нейроны, в результате выпадает рефлекс раскрытия кардии на глоток.
Манометрически находят нормальный или даже сниженный градиент пищеводно-желудочного давления, наблюдается значительное ослабление моторики пищевода.
При ахалазии нет условий для возникновения повышенной чувствительности гладкой мускулатуры нижнего пищеводного сфинктера к гастрину - сохраняется центральная иннервация.
Необходимо отметить, что нарушение рефлекса раскрытия кардии и моторики пищевода - два параллельных процесса, идущих одновременно.
Согласно наиболее распространённой классификации Б. В. Петровского,различают четыре стадии кардиоспазма:
I стадия - пищевод не расширен, рефлекс раскрытия кардии сохранён, но моторика пищевода усилена и дискоординирована;
II стадия - рефлекс раскрытия кардии отсутствует, отмечается расширение пищевода до А - 5 см;
III стадия - значительное расширение пищевода до 6 - 8 см, задержка в нём жидкости и пищи, отсутствие пропульсивной моторики; ^стадия - резкое расширение, удлинение и искривление пищевода с атонией стенок, длительной задержкой жидкости и пищи.
При ахалазия кардии и кардиоспазме наблюдаются следующие основные симптомы:дисфагия, регургитация, распирающие боли в груди.
Дисфагия часто носит интермиттирующий характер, может усиливаться при волнении, нередко имеет парадоксальный характер: хорошо проходит твёрдая пища, жидкость задерживается.
Больные отмечают, что для того, чтобы пища проходила, им приходится запивать её водой или прибегать к другим приёмам, например к повторным глотательным движениям.
Регургитация возникает вначале сразу после еды, а при прогрессировании заболевания через более или менее значительное время после приёма пищи.
Регургитация может наблюдаться во время сна (симптом «мокрой подушки»), что грозит опасностью аспирации и развитием легочных осложнений.
Боль обычно носит распирающий характер, появляется во время или после еды по ходу пищевода, иррадиирует в спину, между лопатками.
Иногда сильный спазм пищевода во время приёма пищи может быть расценен как приступ стенокардии.
Основные методы диагностикинервно-мышечных заболеваний пищевода - рентгенологическое, эндоскопическое и манометрическое исследования.
Рентгенологическое исследованиепозволяет в большинстве случаев правильно поставить диагноз.
Характерным рентгенологическим признаком является расширение пищевода в той или иной степени с наличием узкого сегмента в терминальном его отделе (симптом «мышиного хвостика», «перевёрнутого пламени свечи»).
Стенки пищевода, в том числе и в суженной части, сохраняют эластичность.
Газовый пузырь желудка обычно отсутствует.
При эзофагоскопиив начальных стадиях заболевания каких-либо характерных изменений в пищеводе не выявляется.
В далеко зашедших стадиях болезни виден большой зияющий просвет пищевода, иногда с жидкостью, слизью, остатками пищи.
Слизистая оболочка пищевода обычно воспалена, утолщена, могут выявляться эрозии, язвы, участки лейкоплакии, изменения нарастают в дистальном направлении.
Эндоскоп практически всегда проходит в желудок.
Если этого не происходит, следует думать об органическом стенозе (пептическая стриктура, рак).
Большое значение в диагностике нервно-мышечных заболеваний пищевода придаётся эзофагоманометрии,позволяющей провести окончательную дифференциальную диагностику между ахалазией кардии и кардиоспазмом.
При кардиоспазме градиент пищеводно-желудочного давления больше 20 мм рт. ст, при ахалазии кардии - меньше 20 мм рт. ст., отсутствует рефлекс раскрытия нижнего пищеводного сфинктера на глотание.
Основным методом лечения ахалазии кардии и кардиоспазма в настоящее время является кардиодилатация,которая при повторных проведениях приводит к разрыву рубцовой ткани, парезу в области нижнего пищеводного сфинктера, уменьшая тем самым градиент пищеводно-желудочного давления и обеспечивая восстановление пассивного (за счёт силы тяжести) пассажа пищи.
Наиболее часто выполняется пневматическая кардиодилатация.
Кардиодилататор состоит из резинового или пластмассового зонда с баллоном, укреплённым на конце, диаметром 25, 35 и 45 мм.
Кардиодилатацию проводят под рентгеновским или эндоскопическим контролем, начиная с дилататора диаметром 25 мм с давлением в нём от 180 до 240 мм рт. ст.
Дилатацию обычно выполняют через день, постепенно увеличивая диаметр баллона и повышая давление до 320 мм рт. ст.
В среднем курс лечения состоит из 5 - 6 процедур, в некоторых случаях число кардиодилатаций приходится увеличивать до 10 -12.
Об эффективности кардиодилатаций судят по клиническим проявлениям (исчезновение дисфагии) и снижению градиента пищеводно-желудочного давления.
Не следует уменьшать градиент давления ниже 7 - 8 мм рт. ст., так как это может привести к развитию рефлюкс-эзофагита.
Форсированная пневмокардиодилатация может осложниться надрывами слизистой оболочки пищевода и провоцировать обострение эзофагита.
Самым тяжёлым осложнением кардиодилатаций является перфорация пищевода (0,5 - 1 %).
Разрыв пищевода служит показанием к экстренной операции, при которой рана ушивается, линия швов укрепляется стенкой желудка по типу неполной фундопликации.
Показаниями к оперативному лечению ахалазии кардии и кардиоспазма являются:
• невозможность проведения кардиодилататора через кардию;
• неуверенность в правильном диагнозе при обоснованном подозрении на рак кардиоэзофагеальной зоны;
• неадекватное восстановление проходимости кардии после законченного курса пневматической кардиодилатаций, неэффективность трёх курсов кардиодилатаций;
• сочетание с другими заболеваниями, требующими оперативного лечения;
• функциональная непроходимость кардии на фоне нормального тонуса нижнего пищеводного сфинктера.
Предложено более 60 способов оперативного лечения нервно-мышечных заболеваний пищевода, что говорит о сложности данной проблемы.
В настоящее время оптимальной операцией следует считать эзофагокардиомиотомию по Геллеру с неполной фундопликацией.
При IV стадии заболевания, особенно у больных, уже перенесших неудачные кардиопластические операции, осложнившиеся развитием рефлюкс-эзофагита и пептической стриктуры, операцией выбора является субтотальная резекция пищевода с одномоментной эзофагопластикой.
В последнее время широкое распространение получили оперативные вмешательства с использованием видеоэндохирургической техники.
Основным видом видеоэндохирургической операции является экстрамукозная эзофагокардиомиотомия с неполной фундопликацией.
Операция может быть выполнена как из торакоскопического, так и из лапароскопического доступов.
Проведённые анатомические исследования выявили, что у лиц долихоморфного типа телосложения, а также у лиц мезоморфного типа телосложения при протяжённости нижнего пищеводного сфинктера более 6 см, наилучший подход к пищеводу обеспечивается при использовании торакоскопического доступа.
У пациентов брахиморфного и мезоморфного типа телосложения при протяжённости нижнего пищеводного сфинктера менее 6 см более предпочтительным является лапароскопический доступ.
При торакоскопическом подходе после введения троакаров в плевральную полость и проведения осмотра пересекают лёгочную связку, лёгкое отводят кпереди.
Боковую стенку пищевода визуализируют между перикардом и нисходящей частью грудной аорты, рассекают медиастинальную плевру, мобилизацию пищевода производят только по переднелатеральной его стенке, то есть непосредственно над линией планируемого рассечения его мышечной оболочки.
Производят эзофагомиотомию на протяжении 6 см.
При выполнении миотомии особое внимание необходимо уделять полноте пересечения циркулярных мышечных волокон, чему способствует увеличение объекта оперативного вмешательства, а также интраоперационное применение эзофагогастроскопии.
Выполняют сагиттальную диафрагмотомию, диафрагмальную вену клипируют и пересекают.
Миотомический разрез продолжают на кардиальный отдел желудка на протяжении 1,5 - 2 см (рис.6).
Наибольшие трудности возникают в области пищеводно-желудочного перехода, так как в этом отделе отмечаются выраженные рубцовые изменения мышечного слоя, именно на этом уровне чаще всего происходит повреждение слизистой оболочки.
Рассечение мышечных волокон кардиального отдела часто сопровождается кровотечением из мелких сосудов стенки желудка, для остановки которого обычно достаточно применения биполярной электрокоагуляции или клипирования сосудов.
Дно желудка выводят в плевральную полость и фиксируют к краям мышечного дефекта пищевода отдельными интракорпоральными узловыми швами (фиксация клипсами ненадёжна). Отдельными узловыми швами диафрагму фиксируют к желудку.
Плевральную полость дренируют через разрез в VII межреберье по заднеподмышечной линии.
В последнее время лапароскопический подход считается более предпочтительным в хирургическом лечении ахалазии кардии и кардиоспазма.
Лапароскопический доступ менее травматичен, не требует однолёгочной вентиляции и мероприятий, связанных с ретракцией лёгкого.
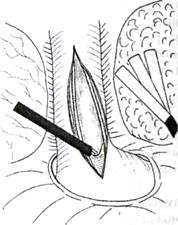
Рис. 6. Торакоскопическая эзофагокардиомиотомия
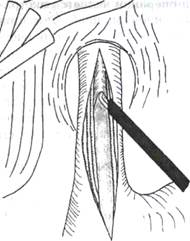
Рис. 7. Лапароскопическая эзофагокардиомиотомия
Абдоминальный отдел пищевода обычно доступен для манипуляций, а выделение нижнегрудного отдела возможно из лапароскопического доступа даже без использования диафрагмотомии.
Операцию начинают с ревизии органов брюшной полости.
Тракция желудка в каудальном направлении должна выполняться мягким зажимом для исключения повреждения серозной оболочки и быть дозированной.
При этом пищевод становится более доступным для манипуляций.
Левую долю печени отводят трёхлепестковым ретрактором.
Не следует пересекать левую треугольную связку, так как излишне мобильная левая доля печени может затруднять выполнение оперативного вмешательства.
Рассекают брюшину, покрывающую абдоминальный отдел пищевода и кардиальный отдел желудка.
Диафрагму отслаивают острым и тупым путём, при этом хорошо визуализируются клетчаточные пространства средостения.
С помощью электрохирургического крючка последовательно рассекают вначале продольные, а затем циркулярные мышечные волокна на протяжении 6 - 7 см по пищеводу и 1,5 -2 см по желудку (рис.7).
Этот этап операции очень ответственный, все манипуляции необходимо проводить при хорошей визуализации тканей, чтобы исключить повреждение плевральных листков и перикарда.
Повреждение слизистой оболочки пищевода чаще всего встречается в месте наибольших рубцовых изменений, но обычно не требует конверсии.
Дефект слизистой оболочки ушивают отдельными узловыми швами на прямой или лыжеобразной атравматической игле.
После эзофагокардиомиотомии должно быть выполнено закрытие дефекта мышечной оболочки.
Для этой цели наиболее часто применяют переднюю фундопликацию по Дору.
По данным большинства исследователей, при хирургическом лечении ахалазии кардии и кардиоспазма фундопликация по Ниссену в различных модификациях не имеет никаких преимуществ перед передней, но технически значительно сложнее.
Фундопликация по Дору не требует пересечения связочного аппарата и коротких сосудов желудка и производится путём подшивания стенки дна желудка к краям разреза мышечной оболочки отдельными узловыми швами с предварительно введённым в просвет пищевода зондом. Брюшную полость дренируют.
В IV стадии заболевания, особенно при рецидивах после оперативных вмешательств, операцией выбора является экстирпация пищевода, которая может быть выполнена из торакоскопического доступа.
Диффузный спазм пищевода, или синдром Барсони-Тешендорфа- заболевание, обусловленное спастическими сокращениями стенки пищевода при сохранении нормальной, как правило, сократительной способности нижнего пищеводного сфинктера.
Выделяют первичный и вторичный эзофагоспазм.
Под вторичным понимают эзофагоспазм, развившийся на фоне других заболеваний пищевода.
Ведущими симптомами диффузного спазма пищевода являются дисфагия и боль в грудной клетке.
Реже встречаются регургитация, похудание, общая слабость.
Рентгенологически при диффузном эзофагоспазме выявляют «чёткообразный», а в других случаях - «штопорообразный» пищевод, задержки в пищеводе контрастного вещества и сужения дистального отдела пищевода не отмечается.
Эндоскопическое исследование не выявляет характерных признаков заболевания.
При эзофагоманометрии по всему длиннику пищевода наблюдаются сегментарные непропульсивные сократительные волны, возникающие одновременно на разных уровнях вне зависимости от глотка, цифры градиента пищеводно-желудочного давления нормальные.
Лечение первичного эзофагоспазма консервативное, кардиодилатация не даёт выраженного эффекта.
Комплексная консервативная терапия включает в себя назначение антагонистов кальция (нифедепин, коринфар), нитратов, седативных препаратов, витаминотерапии, спазмолитических препаратов (но-шпа, платифиллин, папаверин), физиопроцедур (электрофорез с новокаином, сульфатом магния, хлоридом калия).
При неэффективности консервативного лечения выполняют операцию -эзофагомиотомию на протяжении от уровня дуги аорты до нижнего пищеводного сфинктера (операция Биокка).
К оперативному лечению диффузного спазма пищевода прибегают достаточно редко.
Операцию производят из правостороннего торакоскопического доступа в положении больного на левом боку.
После создания пневмоторакса и введения инструментов пересекают лёгочную связку, отводят правое лёгкое, визуализируют грудной отдел пищевода.
Рассекают медиастинальную плевру от диафрагмы до непарной вены, затем производят эзофагомиотомию от нижнего пищеводного сфинктера до v. azygos с обязательным полным пересечением как продольных, так и циркулярных мышц под контролем эзофагоскопа (рис. 8).
Образовавшийся дефект мышечного слоя пищевода не укрывают. Плевральную полость дренируют.
Дата добавления: 2014-12-14; просмотров: 1356;
