Химические свойства. Сопряженные диены дают все химические реакции, характерные для двойных связей
Сопряженные диены дают все химические реакции, характерные для двойных связей. Отличительные особенности:
1. Более высокая термодинамическая стойкость.
2. Более высокая реакционная способность из-за очень большой поляризуемости.
3. Способность к присоединению по концам цепочки сопряженных связей.
1. Реакции присоединения
1. Присоединение водорода, галогенов, галогеноводородов может идти в положении 1,2 и в положении 1,4. Например, присоединение НCl, происходящее по электрофильному (ионному) механизму:
1 2 3 4 + +



 СH2=CH-CH=CH2 + H+
СH2=CH-CH=CH2 + H+ 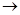 CH2=CH-CH-CH3
CH2=CH-CH-CH3 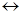 CH2-CH=CH-CH3
CH2-CH=CH-CH3 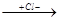
CH2=CH-CH-CH3 CH2-CH=CH-CH3 CH2-CH=CH-CH3 CH3-CH-CH=CH2
Cl Cl Cl Cl
Продукт присоединения продукт присоединения
HCl в положение 1,2 HCl в положение 1,4
3-хлор-1-бутен 1-хлор-2-бутен
Наблюдается резонанс 1 и 2 структур карбкатиона.
Выход продукта возрастает при повышении температуры, полярности и поляризуемости реагента.
2. Реакция диенового синтеза (реакция Дильса-Адлера) – реакция присоединения, характерная только для сопряженных диенов. Эта реакция используется для качественного и количественного определения сопряженных диенов под действием непредельных соединений (диенофилов), у которых двойная связь активирована электроноакцепторными заместителями благодаря сопряжению с электроотрицательными атомами.
Например:
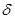 -
- 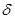 +
+
СH3 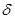 +CH2
+CH2 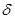 - CH2
- CH2
 C CH
C CH
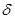 - CH
- CH 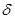 + +
+ + 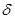 +C=O
+C=O 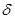 -
-
CH2 H
Изопрен акролеин

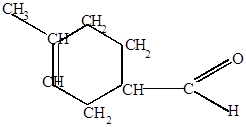
4-метил-3-циклогексенкарбальдегид
Роль диенофила могут выполнять и сами диеновые углеводороды (реакция Лебедева):

|
CH2
+СH-CH=CH2 
| 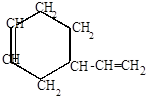
|
4-винил-1-циклогексен
2. Реакции окисления
Диены легко окисляются за счет активных двойных связей. Реакции идут так же, как у олефинов, за счет разрыва двойной связи.
1. Под действием озона:
СH2=CH-CH=CH2 + 2O3  CH2-CH-CH-CH2
CH2-CH-CH-CH2  CH2 + CH-CH + CH2
CH2 + CH-CH + CH2
O-O-O O-O-O -H2O2 O O O O
2. Окисление молекулярным кислородом протекает:
а) с образованием перекисных олигомеров
 CH2=CH-CH=CH2 + O2
CH2=CH-CH=CH2 + O2 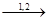 (-CH-CH2-O-O-)n
(-CH-CH2-O-O-)n
CH
CH2
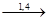 (-CH2-CH=CH-CH2-O-O-)n
(-CH2-CH=CH-CH2-O-O-)n
б) могут образовываться циклоперекисные продукты, здесь молекула кислорода работает как диенофил.

|
+ O  O
O
| 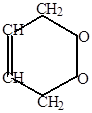
|
в) при высоких температурах и при наличии насыщенных звеньев может идти реакция окисления в a-звене.
H
CH2=CH-CH=CH-CH3 + O2  CH2=CH-CH=CH-CH
CH2=CH-CH=CH-CH 
H O-O-H
 H2O + CH2=CH-CH=CH-C
H2O + CH2=CH-CH=CH-C
O
Винилакролеин
3. Реакции полимеризации
Полимеризация диеновых углеводородов происходит в основном за счет 1,4-присоединения, хотя известны и 1,2-полимеры. Механизм реакций может быть ионным (металлические, металлорганические катализаторы) или свободно-радикальлным (в присутствии перекисного индикатора)

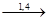 (-CH2-CH=CH-CH2-)n 1 тип
(-CH2-CH=CH-CH2-)n 1 тип
СH2=CH-CH=CH2 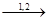 (-CH2-CH- )n 2 тип
(-CH2-CH- )n 2 тип
CH=CH2
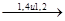 (-(CH2-CH=CH-CH2)x-(CH2-CH))n
(-(CH2-CH=CH-CH2)x-(CH2-CH))n
CH
CH2 3 тип
III тип полимеризации наблюдается при использовании щелочных металлов в качестве катализатора. I и II тип полимеризации наблюдается при использовании катализатора Циглера.



 Пространственная структура полимеров, полученная в присутствии катализатора Циглера, отличается регулярностью повторения однотипных звеньев, такие полимеры называются стереорегулярными. При этом наблюдается несколько видов стереоизомерии. 1,4-стереорегулярные полимеры могут иметь цис- или транс-строение.
Пространственная структура полимеров, полученная в присутствии катализатора Циглера, отличается регулярностью повторения однотипных звеньев, такие полимеры называются стереорегулярными. При этом наблюдается несколько видов стереоизомерии. 1,4-стереорегулярные полимеры могут иметь цис- или транс-строение.
H H H CH2-
C=C C=C
-CH2 CH2- -CH2 H n
цис- транс-
1,2-стереорегулярные полимеры могут быть изотактическими или синдиотактическими.
CH2
CH
(-СH2-CH-)n (-CH2-CH-CH2-CH-)n
CH CH
CH2 CH2
изотактический синдиотактический
Нестереорегулярные полимеры – атактические с беспорядочным расположением ответвлений.
Полимеры диеновых углеводородов представляют собой очень эластичные каучукообразные вещества и применяются как заменители или синтетические аналоги натурального каучука в производстве резиновых изделий.
Дата добавления: 2014-12-24; просмотров: 1122;
