Углекислого газа.
Энергия не производится ради самого производства энергии. В промышленно развитых странах основная часть вырабатываемой энергии приходится на промышленность, транспорт, обогрев и охлаждение зданий. Во многих недавно выполненных исследованиях показано, что современный уровень потребления энергии в промышленно развитых станах может быть существенно снижен за счёт применения энергосберегающих технологий. Так, было рассчитано, что если бы США перешли бы при производстве товаров широкого потребления и в сфере услуг на наименее энергоёмкие из уже имеющихся технологий при том же объёме производства, то количество поступающего в атмосферу 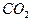 уменьшилось бы на 25%. Результирующее уменьшение выбросов
уменьшилось бы на 25%. Результирующее уменьшение выбросов 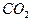 в целом по земному шару при этом составило бы 7%. Подобный эффект имел бы место и в других промышленно развитых странах. Дальнейшего снижения скорости поступления
в целом по земному шару при этом составило бы 7%. Подобный эффект имел бы место и в других промышленно развитых странах. Дальнейшего снижения скорости поступления 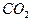 в атмосферу можно достичь путём изменения структуры экономики в результате внедрения более эффективных методов производства товаров и усовершенствований в сфере предоставления услуг населению.
в атмосферу можно достичь путём изменения структуры экономики в результате внедрения более эффективных методов производства товаров и усовершенствований в сфере предоставления услуг населению.
Углерод в природе.
Среди множества химических элементов, без которых невозможно существование жизни на Земле, углерод является главным. Химические превращения органических веществ связаны со способностью атома углерода образовывать длинные ковалентные цепи и кольца. Биогеохимический цикл углерода, естественно, очень сложный, так как он включает не только функционирование всех форм жизни на Земле, но и перенос неорганических веществ как между различными резервуарами углерода, так и внутри них. Основными резервуарами углерода являются атмосфера, континентальная биомасса, включая почвы, гидросфера с морской биотой и литосфера. В течение последних двух столетий в системе атмосфера - биосфера - гидросфера происходят изменения потоков углерода, интенсивность которых примерно на порядок величины превышает интенсивность геологических процессов переноса этого элемента. По этой причине следует ограничиться анализом взаимодействий в пределах этой системы, включая почвы.
Основные химические соединения и реакции.
Известно более миллиона углеродных соединений, тысячи из которых участвуют в биологических процессах. Атомы углерода могут находиться в одном из девяти возможных состояний окисления: от +IV до -IV. Наиболее распространённое явление - это полное окисление, т.е. +IV, примерами таких соединений могут служить 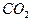 и
и  . Более 99% углерода в атмосфере содержится в виде углекислого газа. Около 97% углерода в океанах существует в растворённой форме (
. Более 99% углерода в атмосфере содержится в виде углекислого газа. Около 97% углерода в океанах существует в растворённой форме ( 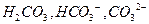 ), а в литосфере - в виде минералов. Примером состояния окисления +II является малая газовая составляющая атмосферы
), а в литосфере - в виде минералов. Примером состояния окисления +II является малая газовая составляющая атмосферы 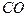 , которая довольно быстро окисляется до
, которая довольно быстро окисляется до 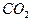 .Элементарный угрерод присутствует в атмосфере в малых количествах в виде графита и алмаза, а в почве - в форме древесного угля. Ассимиляция углерода в процессе фотосинтеза приводит к образованию восстановленного углерода, который присутствует в биоте, мёртвом органическом веществе почвы, в верхних слоях осадочных пород в виде угля, нефти и газа, захоронённых на больших глубинах, и в литосфере - в виде рассеянного недоокисленного углерода. Некоторые газообразные соединения, содержащие недоокисленный углерод
.Элементарный угрерод присутствует в атмосфере в малых количествах в виде графита и алмаза, а в почве - в форме древесного угля. Ассимиляция углерода в процессе фотосинтеза приводит к образованию восстановленного углерода, который присутствует в биоте, мёртвом органическом веществе почвы, в верхних слоях осадочных пород в виде угля, нефти и газа, захоронённых на больших глубинах, и в литосфере - в виде рассеянного недоокисленного углерода. Некоторые газообразные соединения, содержащие недоокисленный углерод 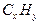 , в частности метан, поступают в атмосферу при восстановлении веществ, происходящем в анаэробных процессах. Хотя при бактериальном разложении образуется несколько различных газообразных соединений, они быстро окисляются, и можно считать, что в систему поступает
, в частности метан, поступают в атмосферу при восстановлении веществ, происходящем в анаэробных процессах. Хотя при бактериальном разложении образуется несколько различных газообразных соединений, они быстро окисляются, и можно считать, что в систему поступает 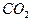 . Исключением является метан, поскольку он также влияет на парниковый эффект. В океанах содержится значительное количество растворённых соединений органического углерода, процессы окисления которых до
. Исключением является метан, поскольку он также влияет на парниковый эффект. В океанах содержится значительное количество растворённых соединений органического углерода, процессы окисления которых до 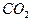 известны ещё недостаточно хорошо.
известны ещё недостаточно хорошо.
Изотопы углерода.
В природе известно семь изотопов углерода, из которых существенную роль играют три. Два из них - 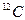 и
и 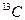 - являются стабильными, а один -
- являются стабильными, а один -  - радиоактивным с периодом полураспала 5730 лет. Необходимость изучения различных изотопов углерода обусловлена тем, что скорости переноса соединений углерода и условия равновесия в химических реакциях зависят от того, какие изотопы углерода содержат эти соединения. По этой причине в природе наблюдается различное распределение стабильных изотопов углерода. Распределение же изотопа
- радиоактивным с периодом полураспала 5730 лет. Необходимость изучения различных изотопов углерода обусловлена тем, что скорости переноса соединений углерода и условия равновесия в химических реакциях зависят от того, какие изотопы углерода содержат эти соединения. По этой причине в природе наблюдается различное распределение стабильных изотопов углерода. Распределение же изотопа  , с одной стороны, зависит от его образования в ядерных реакциях с участием нейтронов и атомов азота в атмосфере, а с другой - от радиоактивного распада.
, с одной стороны, зависит от его образования в ядерных реакциях с участием нейтронов и атомов азота в атмосфере, а с другой - от радиоактивного распада.
Углерод в атмосфере.
Дата добавления: 2014-12-22; просмотров: 861;
