Комплексометрия. Комплесонометрическое титрование
Комплесометрия основана на реакциях образования комплексов. Несмотря на их огромное разнообразие, метод не нашел широкого распространения, т.к. эти реакции проходят в несколько стадий. Из множества реакций применение в титриметрии нашли только реакции с участием ионов:
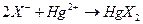 1) Ртути (II) - меркурометрия
1) Ртути (II) - меркурометрия
(где Х = Cl-, Br-, J-, SCN-)
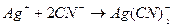 2) CN- - цианометрия
2) CN- - цианометрия
3) F- - фторометрия
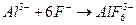 |
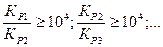 Для того, чтобы на кривой титрования получились скачки, соответствующие отдельным ступеням комплексообразования, необходимо выполнение условия дифференцированного титрования
Для того, чтобы на кривой титрования получились скачки, соответствующие отдельным ступеням комплексообразования, необходимо выполнение условия дифференцированного титрования
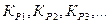 где - константы равновесия реакции комплексообразования по I, II, III,… ступеням.
где - константы равновесия реакции комплексообразования по I, II, III,… ступеням.
Для большинства реакций коплексообразования различие между константами равновесия образования комплексов отдельных ступеней составляют 102 – 104. Для таких реакций получается кривая титрования с одним скачком титрования.
Широкое практическое применение метод комплексообразования нашел с открытием новых комплексообразователей – производных аминополикарбоновых кислот - комплексонов. Метод анализа с применением комплексонов получил название комплексонометрия.
Метод комплексонометрического титрования основан на реакциях образования внутрикомплексных соединений ионов металлов с комплексонами. Ионы металлов, участвующие в комплексообразовании, являются акцепторами электронных пар, тогда как аминополикарбоновые кислоты - их донорами.
Достоинствами метода являются:
- реакция одностадийная, протекает быстро, состав образующегося комплекса прост и отвечает соотношению металл-лиганд 1:1(для МоО22+ может быть 2:1);
- комплекс очень устойчив вследствие циклообразования (за счет энтропийного фактора) и хорошо растворим в воде.
С помощью комплексонов можно определить почти все металлы и этот метод начинает вытеснять осадительное титрование, гравиметрию, окислительно-восстановительное титрование.
Наиболее распространены 3 комплексона:
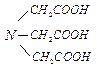 |
нитрилотриуксусная кислота – комплексон I (Н3Y);
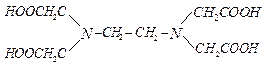 |
этилендиаминтетрауксусная кислота (ЭДТА) – комплексон II (H4Y;)
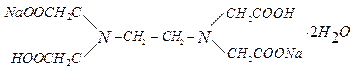 |
динатриевая соль ЭДТА - комплексон III (трилон Б).
Cокращенно пишут Na2H2Y4 · 2Н2О.
В связи с лучшей растворимостью в воде наиболее широкое практическое применение нашел трилон Б.
Образование трилоном Б внутрикомплексного соединения с каким-нибудь двухзарядным катионом происходит путем замещения металлом атомов водорода карбоксильных групп и одновременного взаимодействия катиона с атомами азота аминогрупп (за счет координационной связи):
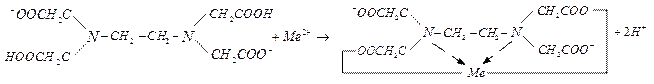 |
Такие реакции комплексообразования можно представить в виде: 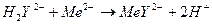
Повышение кислотности среды препятствует образованию комплекса МеY2¯, поэтомупри комплекс. титровании используют буферные растворы.
Чтобы реакция комплексообразования прошла с достаточной полнотой (99,99 %) и могла быть использована в количественном анализе константа образования комплекса должна быть больше 108. В этом случае остаточные концентрации [Ме2+] и [Y4¯] в момент эквивалентности не превышают 1·10-4 от единицы. Общая константа образования комплекса или устойчивость комплекса β выражается уравнением 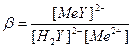
Устойчивость комплексов металл-ЭДТА различна в зависимости от природы иона металла, его зарядности и меняется в зависимости от рН среды. р- и d – элементы могут образовать комплексы с ЭДТА и в кислой среде. К ним относятся комплексы с Bi3+, Fe3+, Cr3+ и т.д. В то же время определение Ва2+, Mg2+, Cr2+ комплексонометрическим титрованием проводят в щелочной среде.
Как видно из уравненеия реакции комплексообразования. При титровании комплексоном III происходит выделение ионов водорода, для связывания которых в анализируемый раствор вводят буферный раствор.
Дата добавления: 2017-11-04; просмотров: 810;
