Рентгеновская компьютерная томография.
Определяются метастазы рака предстательной железы в печень.
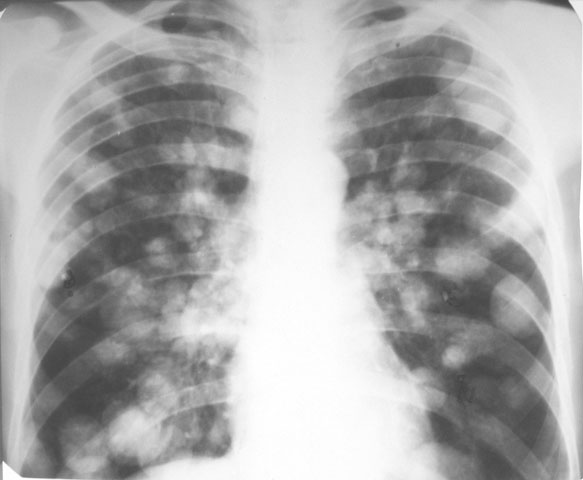 Рентгенография органов грудной клетки. Метастазы рака предстательной железы в легкие.
Рентгенография органов грудной клетки. Метастазы рака предстательной железы в легкие.
Лечение.
При лечении РПЖ в настоящее время используются практически все методы специфического воздействия, применяемые в онкологии — хирургический, лучевой, гормональный, лекарственный. Выбор метода лечения определяется клинической стадией опухоли на момент постановки диагноза, возрастом больного, общим состоянием его здоровья, а также пожеланием пациента относительно предстоящей терапии. Необходимо принимать во внимание степень дифференцировки опухоли, уровень простатического специфического антигена (ПСА) до лечения и его динамику после. Поскольку РПЖ, особенно в начальных стадиях — медленно протекающее заболевание, во многом выбор метода оказания помощи определяет предполагаемая продолжительность жизни больного. Например, при локализованном РПЖ у пациента, который из-за возраста или сопутствующих заболеваний может прожить менее 10 лет, желательно избегать активного вмешательства, поскольку в течение данного отрезка времени болезнь не успеет прогрессировать.
Существует 4 основных метода лечения первичного РПЖ: выжидательная тактика (динамическое наблюдение), хирургическое, лучевое и гормональное.
Лечение локализованного рака предстательной железы.При локализованном РПЖ (Т1—2) применяются:
· выжидательная тактика
· лучевая терапия
· хирургическое лечение.
Выжидательная тактика чаще используется при стадии Т1 (опухоль, не определяемая клинически, обнаруженная случайно при гистологическом исследовании), у больных пожилого возраста с высокодифференцированными формами опухолей. Применяется при обнаружении очень маленьких фокусов высокодифференцированного рака в предстательной железе, что может представлять собой т.н. «гистологический РПЖ», который почти никогда не развивается в «клинический»; при бессимптомном раке — у очень пожилого либо страдающего тяжелой болезнью пациента, а также у любого больного, который отказывается от активного вмешательства из-за нежелания подвергаться риску побочных эффектов.
В таких случаях после постановки диагноза лечение не проводится до развития симптомов рака либо признаков, говорящих о прогрессировании РПЖ (например, рост ПСА). Подход получил распространение после анализа результатов наблюдения за пожилыми мужчинами с локализованными высокодифференцированными опухолями в скандинавских странах: активации РПЖ не происходило в течение длительного времени, и большинство больных умирали от других, преимущественно сердечно-сосудистых заболеваний. Основная проблема — точность оценки предполагаемой продолжительности жизни конкретного пациента и риска прогрессирования РПЖ за этот период. Однако при локализованной форме рака простаты более распространенным является активный лечебный подход, включающий применение лучевой терапии или операцию.
Хирургическое лечение. По мнению большинства урологов, лучшим методом лечения ограниченного РПЖ является радикальная простатэктомия. Данная операция целесообразна в тех случаях, когда предполагаемая продолжительность жизни больного составляет не менее 10 лет. Эта операция, выполняемая, как правило, позадилобковым доступом, что позволяет выполнить тазовую лимфаденэктомию, подразумевает удаление предстательной железы вместе с капсулой, семенными пузырьками, простатической частью уретры, шейкой мочевого пузыря, регионарными лимфатическими узлами. Наиболее исчерпывающее описание позадилобковой простатэктомии сделано Walsh (1983). Преимуществами радикальной простатэктомии являются полное удаление опухоли, точное определение стадии заболевания, излечение сопутствующей аденомы предстательной железы, надежное подавление уровней ПСА ниже предела чувствительности качественного анализа. К недостаткам следует отнести послеоперационную летальность (до 0,5%) и такие осложнения, как импотенция (50—90%), стриктура пузырно-уретрального анастомоза (5—17%), недержание мочи (3—36%).
Лучевая терапия. При лечении локализованного и местно-распространенного РПЖ могут использоваться дистанционное облучение и интерстициальная лучевая терапия (брахитерапия). Дистанционное облучение предстательной железы и окружающей клетчатки проводится с четырех полей. Разовая доза — 1,8–2,0 Гр, суммарная — 65–70 Гр.
Совершенствование методов планирования и технического обеспечения лучевой терапии привело к внедрению т.н. конформного облучения, которое обеспечивает точное соответствие объема облучения пораженному органу. Для его проведения необходимо получить трехмерное изображение предстательной железы и соседних органов при помощи реконструкции КТ-сканов. Затем производится планирование полей облучения с использованием специальных компьютерных программ, целью которого является обеспечение доставки возможно большей дозы к предстательной железе при возможно меньшей дозе облучения, приходящейся на мочевой пузырь и прямую кишку. Эти технологические достижения дают возможность использовать бльшие дозы облучения (около 70 Гр) без увеличения осложнений. Поскольку считается, что эффект лучевой терапии дозозависим, одним из направлений улучшения ее результатов является эскаляция дозы. Ряд исследователей продемонстрировали возможность подведения дозы свыше 80 Гр без существенной токсичности и с лучшими результатами, преимущественно среди больных с местно-распространенным РПЖ. Близость прямой кишки, мочевого пузыря, кавернозных нервов и полового члена к предстательной железе обусловливает спектр осложнений лучевой терапии: постлучевые ректиты, циститы, эректильная дисфункция. Проктиты и циститы, встречаются в 5—20% случаев, недержание мочи, импотенция — в 30% случаев.
Внутритканевая лучевая терапия (брахитерапия) получила распространение в последние годы благодаря техническому обеспечению и использованию новых радиоактивных источников. Преимущество — возможность подведения очень большой дозы к железе (до 160 Гр) без существенных побочных эффектов из-за быстрого поглощения энергии облучения окружающими тканями. Применяются две методики — высоко- и низкодозного облучения.
При высокодозном используется кратковременное воздействие изотопом иридия-92. Часто сочетается с дистанционной лучевой терапией.
 .
.
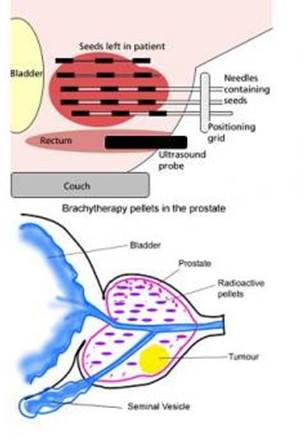
Брахитерапия рака простаты (схема).На верхнем рисунке показана имплантация изотопа в ткань предстательной железы при помощи специальных игл. На нижнем – положение изотопов в ткани предстательной железы пеосле имплантации.
Низкодозная брахитерапия — это перманентная имплантация изотопов палладия-103 или йода-125 в предстательную железу. Период полураспада 103Pd — 17 дней, 125I — 60. Таким образом, предстательная железа облучается в течение 3 или 10 месяцев — в зависимости от используемого изотопа. Зерна с изотопом имплантируются в простату по специальным иглам, которые под контролем ТрУЗИ вводятся в простату через кожу промежности. Кроме обычных осложнений лучевой терапии, при таком лечении часто развивается острая задержка мочи, что требует длительной катетеризации мочевого пузыря.
Лечение диссеминированного рака предстательной железы. В связи с особенностями клинического течения заболевания и несовершенством ранней диагностики в нашей стране 60—80% больных РПЖ при первичном обращении уже имеют метастазы. Выбор методов лечения и их последовательность зависят от стадии заболевания, общего состояния пациента и чувствительности опухоли к тому или иному лечебному воздействию. Рак простаты – гормонозависимая опухоль, гормонотерапия является первичным методом лечения больных, у которых невозможно провести радикальное лечение, то есть радикальную простатэктомию. Нормальные и малигнизированные клетки простаты чувствительны к андрогенам. Еще в 1941 году Huggius and Hodges впервые показали, что кастрация и введение эстрогенов способны воздействовать на эти клетки. Существуют два основных источника андрогенов в организме: клетки Лейдига яичек, которые продуцируют тестостерон (до 95% всех андрогенов) и надпочечники, продуцирующие дегидроандростерон, дегидроандростерона сульфат и андростендион. Функционирование клеток Лейдига яичек регулируется лютеинизирующим гормоном (ЛГ) гипофиза, продукция которого, в свою очередь, стимулируется рилизинг-гормоном лютеинизирующего гормона (ЛГРГ), вырабатываемым в гипоталамусе. Существует механизм отрицательной обратной связи, когда низкие уровни тестостерона в крови стимулируют выработку ЛГРГ, что приводит к усилению выработки ЛГ и повышению уровня тестостерона. Секреция андрогенов надпочечниками регулируется адренокортикотропным гормоном. Синтез самого активного андрогена — 5a-дигидротестостерона — происходит путем трансформации тестостерона при участии фермента 5a-редуктазы, содержащегося в ткани предстательной железы. Свое действие андрогены реализуют путем связывания с внутриклеточным рецептором, после чего комплекс рецептор-гормон взаимодействует с определенными участками ДНК, стимулируя ее транскрипцию.
Дата добавления: 2016-03-05; просмотров: 1325;
