Мембранное равновесие Доннана.
Мембранное равновесие, связанное с различием концентрации солей внутри и вне клеток, известно давно. В 1911 г. Ф. Доннан объяснил это явление, впоследствии названное его именем.
Мембранное равновесие Доннана связано с переносом некоторого количества вещества низкомолекулярного электролита внутрь пространства, содержащего полимер, и, вследствие этого, неравномерного распределения концентраций этого электролита по обе стороны полупроницаемой мембраны.
Когда мембрана ионоселективна, а раствор содержит несколько типов свободных ионов, то происходит неэквивалентное распределение ионов в порах мембраны. Следовательно, должна появиться величина, определяемая разностью осмотического и электрического потенциалов, называемая «потенциалом Доннана», или мембранным потенциалом. Полученные Доннаном результаты согласовались с простой теорией идеальных растворов.
Эффект Доннана обычно наблюдается в двух случаях: для растворов сильных электролитов и для коллоидных систем. Как правило, коллоидные частицы электролитов слишком велики, чтобы проникнуть через мембрану, поэтому она действует как ионоселективная, пропуская только небольшие (обычные) ионы.
Итак, представим себе следующую систему. Водный раствор NaCl разделен мембраной на две секции, как это показано на рис.26. Мембрана проницаема как для ионов Na+, так и для ионов Cl-. В одну из секций добавим немного натриевой соли NaX, полностью диссоциирующей на ионы Na+ и X-
Общий ион Na+ и ион Cl- будут проходить через мембрану на другую сторону до тех пор, пока не восстановится равновесие, хотя добавленный ион X-, для которого мембрана непроницаема, останется в прежней секции.
Условия термодинамического равновесия требуют, чтобы активности любого диффундирующего компонента были равны с обеих сторон мембраны:
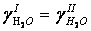 (54)
(54)
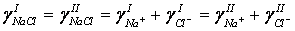 (55)
(55)
Полагая, что раствор идеальный, заменим активности на концентрации:
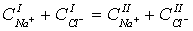 (56)
(56)
Условие термодинамического равновесия можно представить в следующем виде:
 (57)
(57)
где ZNa+ = ZCl- = 1 – валентности ионов Na+ и Cl-.
Условие электронейтральности требует также, чтобы 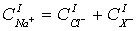
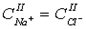 (58)
(58)
Решая совместно уравнения (57) и (58) получаем:
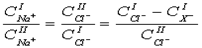 (59)
(59)
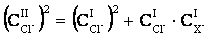 или
или
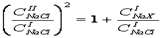 (60)
(60)
Уравнение (60) носит название соотношение Доннана. Из этого уравнения видно, что неэквивалентное распределение диффундирующей соли достигается в равновесных условиях. Соотношение концентраций NaCl в двух секциях всегда больше единицы, поскольку величины концентраций не могут принимать отрицательные значения
Дата добавления: 2016-01-16; просмотров: 2691;
