ВИДИ КОЛОЇДНИХ ЧАСТИНОК
| Мінеральні колоїдні частинки | Осадочні породи, колоїдні глини, гідрооксиди і солі металів |
| Органічні колоїдні частинки | Гумінові і фульвокислоти, що утворюються при розкладанні рослинних і тваринних решток, барвники, поверхнево – активні речовини |
| Біологічні колоїдні частинки | Мікроорганізми (як хвороботворні, так і не хвороботворні), включаючи бактерії, планктон, водорості і віруси |
Проте, яким би не було їх походження, ці колоїдні частки дуже малі – менше 1 мікрона в діаметрі. Внаслідок цього відношення їх поверхні до маси стає настільки великим, що сумарний від’ємний електричний заряд на їх поверхні викликає взаємне відштовхування часток, а електростатичні сили відштовхування перешкоджають самовільному зливанню колоїдних частинок і утворенню великих мас, які б могли легко видалятися в процесі очищення.
Термін коагуляція походить від латинського “coagulare”, що означає “збирати разом”. Коагуляція являє собою комплекс хімічних і фізичних взаємодій між від’ємно зарядженими колоїдними частинками і катіонами (позитивно зарядженими хімічними реагентами). Вона використовує різні сили відштовхування і притягання, які забезпечують стійкість або, навпаки, нестійкість дисперсної системи, а саме:
§ сили електростатичного відштовхування;
§ броунівський рух;
§ сили притягання Ван дер Ваальса;
§ силу всесвітнього тяжіння.
Коагуляція дестабілізує дисперсну систему за допомогою двох різних механізмів:
§ нейтралізації заряду:
§ хімічного зв’язування.
Із цих двох процесів найбільш важлива роль належить нейтралізації заряду. При нейтралізації заряду позитивно заряджені коагулянти нейтралізують від’ємний заряд, що оточує колоїдні частки. Коли заряд навколо кожної частки нейтралізований, вони поступово зближаються, зменшуючи свій ефективний радіус, стають нестійкими і можуть зіштовхуватись одна з одною. При зіткненні частки з’єднуються за рахунок водневих зв’язків чи, наприклад, сил Ван дер Ваальса, утворюючи великі маси або пластівці. Енергія перемішування, яка застосовується в процесі очищення стічної води, збільшує кількість і частоту таких зіткнень часток, посилюючи агломерацію твердої речовини і сприяючи утворенню пластівців.

При хімічному зв’язуванні утворенню пластівців сприяє полімерна природа коагулянтів. Їх довгі молекулярні ланцюжки підхоплюють агломеровані частки, утворюють містки від однієї поверхні до іншої, зв’язуючи разом окремі пластівці у великі, легко відділювані маси.
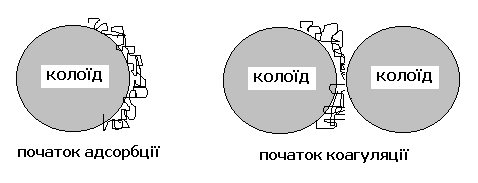
Низькомолекулярні неорганічні або органічні електроліти, що спричиняють агрегацію часточок, називають коагуляторами. Як коагулятори можна використовувати коагулянти і флокулянти. Коагулянти – це солі, що гідролізуються, наприклад, сульфати або галоген іди багатозарядних катіонів, переважно алюмінію і феруму, рідше титану та інших металів. Неорганічні коагулянти застосовувались до появи синтетичних органічних полімерів. З появою цих речовин їх почали застосовувати спочатку як добавки до неорганічних коагулянтів для більш інтенсивного утворення пластівців, а сьогодні ці полімери використовують як основні коагулянти, повністю або частково замінюючи ними неорганічні.
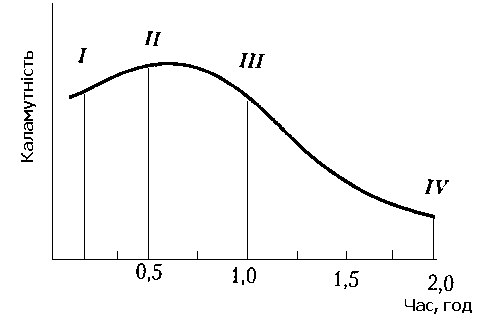
Весь процес прояснення води за допомогою коагуляції умовно можна поділити на декілька етапів.
Дата добавления: 2015-12-11; просмотров: 914;
