Изотопы
Разновидности атомов одного элемента, обладающие одинаковыми зарядами ядер, но разными массовыми числами (одинаковым числом протонов и разным числом нейтронов), называются изотопами. Химические свойства всех изотопов одного элемента одинаковы.
Каждый изотоп характеризуется двумя величинами: массовым числом (проставляется вверху слева от химического знака) и порядковым номером (проставляется внизу слева от химического знака) и обозначается символом соответствующего элемента. Например, элемент водород имеет три изотопа. 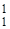 Н – протий (1 р);
Н – протий (1 р); 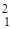 D (
D ( 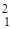 Н) - дейтерий (1р, 1 n);
Н) - дейтерий (1р, 1 n); 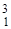 T (
T ( 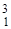 Н) - тритий (1 р, 2 n).
Н) - тритий (1 р, 2 n).
Задание.Сколько протонов и нейтронов содержат ядра изотопов 36Ar, 38 Ar, 40Ar?
36–18 = 18; 38 – 18 = 20; 40 – 18 = 22.
Относительная атомная масса элемента в периодической системе элементов Д. И. Менделеева - это среднее арифметическое масс атомов его изотопов с учетом их распространенности в природе.
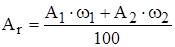
Например, природный хлор - это смесь 77,4% изотопа 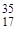 С1 и 22,6% изотопа
С1 и 22,6% изотопа 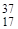 Сl. Поэтому
Сl. Поэтому
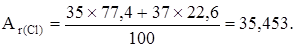
Задание. Медь состоит из изотопов 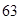 Cu и
Cu и 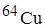 . Сколько процентов каждого изотопа содержится в меди, если
. Сколько процентов каждого изотопа содержится в меди, если 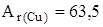 46?
46?
w( 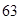 Cu)=х%, w(
Cu)=х%, w( 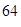 Cu)=(100–х)%,
Cu)=(100–х)%,
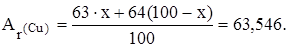
6354,6=63х+6400–64х
х=6400–6354,6, х = 45,4; w( 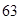 Cu)= 45,4%.
Cu)= 45,4%.
w( 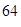 Cu)=100–45,4=54,6%,
Cu)=100–45,4=54,6%,
Дата добавления: 2015-10-21; просмотров: 1097;
