Пентозофосфатный путь
n По этому пути идет не более 25-30% глюкозы поступившей в клетки
n Протекает во всех клетках организма, наиболее интенсивно в печени, эритроцитах, надпочечниках, жировой ткани
n Протекает в цитоплазме, состоит из 2-х этапов: окислительного и неокислительного.
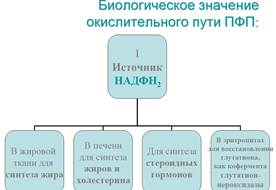
Пентозофосфа́тный путь (пентозный путь, гексозомонофосфатный шунт[1], путь Варбурга — Диккенса — Хорекера[2]) — альтернативный путь окисления глюкозы (наряду с гликолизом и путём Энтнера — Дудорова), включает в себя окислительный и неокислительный этапы.
Суммарное уравнение пентозофосфатного пути:
3 глюкозо-6-фосфат + 6 НАДФ+ → 3СО2 + 6 (НАДФH + Н+) + 2 фруктозо-6-фосфат +глицеральдегид-3-фосфат[3].
В дальнейшем глицеральдегид-3-фосфат превращается в пируват с образованием двух молекулАТФ[2].
Пентозофосфатный путь распространён у растений и животных, а у большинства микроорганизмовимеет только вспомогательное значение[2]. Ферменты пентозофосфатного пути располагаются вцитозоле и животных, и растительных клеток; кроме того, в клетках млекопитающих они располагаются также в эндоплазматическом ретикулуме, а у растений — в хлоропластах[4].
Подобно гликолизу, пентозофосфатный путь, по-видимому, имеет очень древнюю эволюционнуюисторию. Возможно, в древних водах архея ещё до возникновения жизни происходили реакции пентозофосфатного цикла, катализируемые не ферментами, как в живых клетках, а ионамиметаллов, в частности, Fe2+[5].
Биологическое значение неокислительного пути ПФП:
n Совокупность большого количества обратимых реакций
n Каждая из них - это перенос 2-х или 3-х углеродного фрагмента с одного моносахарида на другой
n Реакции неокислительного этапа катализируются ферментами трансальдолазами и транскетолазами
n В состав кофермента транскетолаз входит витамин В1 (тиамин)
n В результате образуется глюкозо-6-фосфат, который может вступать в другие внутриклеточные пути метаболизма глюкозы
Глюкуронатный путь обмена углеводов сопровождается образованием гликозамингликанов, которые составляют основу артропатий при сахарном диабете.
Интенсивный синтез гликопротеидов способствует прогрессированию ангиопатий.
Гликозилирование белков сопровождается повышением содержания гликозилированного гемоглобина.
Перечисленные пути внеинсулинового усвоения глюкозы не обеспечивают основную функцию углеводов - энергетическую. В итоге развивается парадокс метаболизма - кровь насыщена глюкозой, а клетки испытывают энергетический голод. Активируются пути эндогенного образования глюкозы из гликогена и белка (глюконеогенез), однако и эта глюкоза клетками не усваивается из-за недостатка инсулина. Угнетается пентозо-фосфатный шунт и аэробный гликолиз, возникают стойкая гипергликемия, энергетическая недостаточность и гипоксия клеток. Увеличивается концентрация гликозилированного гемоглобина, который не является носителем кислорода, что усугубляет гипоксию.
Нарушение обмена белка. Снижается биосинтез энергетических белков-рибонуклеотидов, что приводит к уменьшению макроэргов в скелетных мышцах и миокарде, составляя компонент мышечной слабости. Уменьшается образование циклических нуклеотидов, которые являются посредниками внутриклеточных гормональных реакций. Подавляется биосинтез транспортной, рибосомальной и матричной РНК в печени, мышцах, почках, жировой ткани. Снижается биосинтез ДНК, в том числе в ядре клеток. Активизируется распад белка. В целом наблюдается нарушение обмена белка с преобладанием катаболических процессов.
Нарушение обмена липидов. Активизируется распад липидов и усиливаются процессы перекисного окисления, что сопровождается накоплением токсичных субстратов, повреждающих сосуды. Нарушается синтез липидов из пищевых компонентов. В связи с угнетением цикла Кребса в крови накапливаются промежуточные компоненты метаболизма - липидо-ацетоуксусная и -оксимасляная кислоты, способствующие развитию кетоацидоза.
Биологическая роль глюкуронатного пути:
n Глюкуроновая кислота входит в состав гликозаминогликанов
n Глюкуроновая кислота участвует в детоксикации экзогенных и эндогенных токсических веществ
Полиольный путь глюкозы:
Глюкоза => Сорбит => Фруктоза
Физиологическая роль полиольного пути:
n При нормальном уровне глюкозы крови через полиольный путь проходит всего 3% потребляемой глюкозы
n Фруктоза является источником энергии в семенных пузырьках
n Сорбит осуществляет баланс осмолярности в клетках почек в соответствии с осмолярностью мочи
8. Глюконеогенез. Локализация, исходные субстраты, ключевые ферменты, обходные реакции, биологическое значение.
Глюконеогенез или обратный гликолиз –это процесс образования глюкозы из веществ неуглеводной природы, протекающий в основном в печени.
Субстраты глюконеогенеза: Лактат Пируват Глицерин Аминокислоты
Первый обходной путь глюконеогенеза:
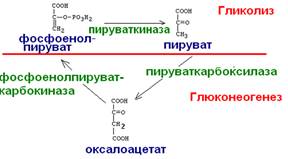
Второй обходной путь глюконеогенеза:

Третий обходной путь глюконеогенеза:
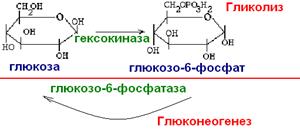
люконеогене́з — метаболический путь, приводящий к образованию глюкозы из неуглеводных соединений (в частности, пирувата). Наряду сгликогенолизом, этот путь поддерживает в крови уровень глюкозы, необходимый для работы многих тканей и органов, в первую очередь, нервной ткани иэритроцитов. Он служит важным источником глюкозы в условиях недостаточного количества гликогена, например, после длительного голодания или тяжёлой физической работы[1][2]. Глюконеогенез является обязательной частью цикла Кори, кроме того, этот процесс может быть использован для превращения пирувата, образованного при дезаминировании аминокислот аланина и серина[3].
Суммарное уравнение глюконеогенеза выглядит следующим образом:
2 Пируват + 4ATP + 2GTP + 2NADH + 2H+ + 4H2O → глюкоза + 4ADP + 2GDP + 6Pi + 2NAD+[4].
Глюконеогенез протекает в основном в печени, но менее интенсивно он протекает также в корковом веществе почек[en] и слизистой кишечника[2].
Глюконеогенез и гликолиз регулируются реципрокно: если клетка снабжена энергией в достаточной степени, то гликолиз приостанавливается, и запускается глюконеогенез; напротив, при активизации гликолиза происходит приостановление глюконеогенеза[5].
Биологическая роль глюконеогенеза:Поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок
9. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
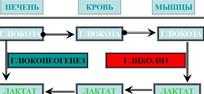
Цикл Кори — совокупность биохимических ферментативных процессов транспорта лактата из мышц в печень, и дальнейшего синтеза глюкозы из лактата, катализируемое ферментами глюконеогенеза.
Биологическое значение.
При интенсивной мышечной работе, а также в условиях отсутствия или недостаточного числа митохондрий (например, в эритроцитах или мышцах) глюкоза вступает на путь анаэробного гликолиза с образованием лактата. Лактат не может далее окисляться, он накапливается (при его накоплении в мышцах раздражаются чувствительные нервные окончания, что вызывает характерное жжение в мышцах). С током крови лактат поступает в печень. Печень является основным местом скопления ферментов глюконеогенеза (синтез глюкозы из неуглеводных соединений), и лактат идет на синтез глюкозы.
Реакция превращения лактата в пируват катализируется лактатдегидрогеназой, далее пируват подвергается окислительному декарбоксилированию или может подвергаться брожению.
10. Гормональная регуляция уровня глюкозы крови. Гипер- и гипогликемические гормоны. Инсулин: химическая природа, место синтеза, особенности образования гормонально активной формы, ткани-мишени, эффекты на углеводный обмен в тканях-мишенях.
Инсули́н — гормон пептидной природы, образуется в бета-клетках островков Лангерганса поджелудочной железы. Оказывает многогранное влияние на обмен практически во всех тканях. Основное действие инсулина заключается в снижении концентрации глюкозы в крови.
Инсулин увеличивает проницаемость плазматических мембран для глюкозы, активирует ключевые ферменты гликолиза, стимулирует образование в печени и мышцах из глюкозы гликогена, усиливает синтез жиров и белков. Кроме того, инсулин подавляет активность ферментов, расщепляющих гликоген и жиры. То есть, помимо анаболического действия, инсулин обладает также и антикатаболическим эффектом.
Нарушение секреции инсулина вследствие деструкции бета-клеток — абсолютная недостаточность инсулина — является ключевым звеном патогенеза сахарного диабета 1-го типа. Нарушение действия инсулина на ткани — относительная инсулиновая недостаточность — имеет важное место в развитии сахарного диабета 2-го типа.
Гипергликемия — увеличение уровня сахара в крови.
В состоянии гипергликемии увеличивается поступление глюкозы как в печень, так и в периферические ткани. Как только уровень глюкозы зашкаливает, поджелудочная железа начинает вырабатывать инсулин.
Гипогликемия — патологическое состояние, характеризующееся снижением уровня глюкозы периферической крови ниже нормы (<3,3 ммоль/л при оценке по цельной капиллярной крови, <3,9 ммоль/л — по венозной плазме). Развивается вследствие передозировки сахароснижающих препаратов или избыточной секреции инсулина в организме. Тяжёлая гипогликемия может привести к развитию гипогликемической комы и вызвать гибель человека.
Дата добавления: 2015-10-19; просмотров: 3408;
