Получение лактонов
Лактоны могут быть получены циклизацией соответствующих гидрокси- или галогенокислот. Особенно легко происходит образование пяти- и шестизвенных лактонов (γ- и δ-лактонов). Подобные лактоны образуются при простом нагревании реагентов в присутствие минеральных кислот (т. е. в условиях реакции этерификации), а нередко даже при комнатной температуре:
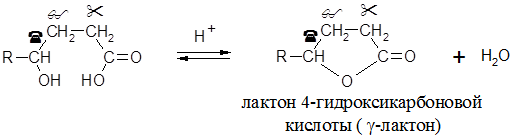
Лактоны с бóльшим числом атомов в цикле в подобных условиях не образуются, т.к. вместо лактонизации происходит межмолекулярная реакция поликонденсации с образованием линейных полиэфиров:
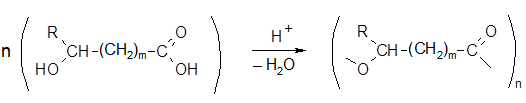
Исходные гидрокси- или галогенокислоты доступны далеко не всегда, поэтому для получения γ- и δ-лактонов часто используют иные методы. γ-Лактоны октановой, нонановой и декановой гидроксикислот получают конденсацией альдегидов с шестью, семью и восемью атомами углерода с малоновой кислотой (реакция Кневенагеля) с последующим декарбоксилированием и лактонизацией, например:
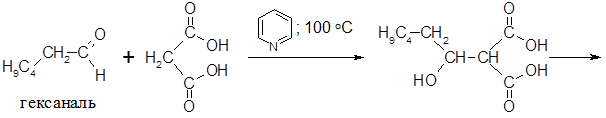
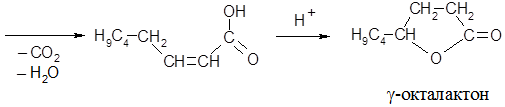
Лактонизация первоначально образующейся 2-октеновой кислоты происходит с перемещением двойной связи и образованием наиболее термодинамически выгодного пятизвенного цикла.
δ-Декалактон получают окислением 2-пентилциклопентанона перекисью водорода или надкислотами по реакции Байера – Виллигера:
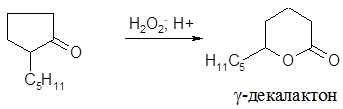
Получение макроциклических лактонов отличается многостадийностью и сложностью процессов. Примером может служить один из методов синтеза пентадеканолида. В качестве исходного вещества используют 10-ундеценовую кислоту, которую в свою очередь получают пиролизом касторового масла. Первой стадией синтеза является гидробромирование 10-ундеценовой кислоты:
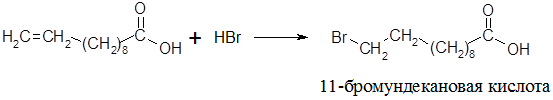
Присоединение бромоводорода происходит против правила Марковникова; реакция является иллюстрацией известного эффекта Хараша – в присутствие кислорода воздуха присоединение HBr протекает не по типу АЕ, а как цепной радикальный процесс (АR).
Далее 11-бромундекановую кислоту ацетилируют ацетатом натрия:
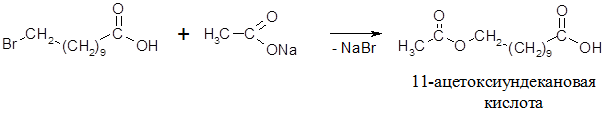
Полученную 11-ацетоксиундекановую кислоту подвергают электроконденсации с моноэтиловым эфиром адипиновой кислоты. Окисление на аноде карбоксильных групп реагентов приводит к образованию СО2 и соответствующих радикалов, рекомбинация которых позволяет удлинить цепь и получить этиловый эфир 15-ацетоксипентадекановой кислоты:
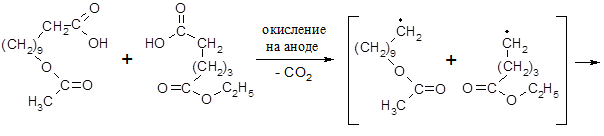

Для получения 15-гидроксипентадекановой кислоты осуществляют омыление эфира и последующее подкисление реакционной массы:
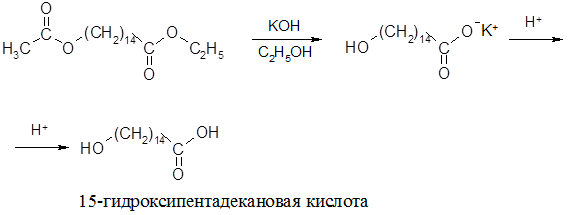
Лактонизацию 15-гидроксипентадекановой кислоты проводят в две стадии по методу Карозерса и Спенэйджела. Сначала получают полиэфир, нагревая гидроксикислоту в присутствие минеральной кислоты и отгоняя реакционную воду:
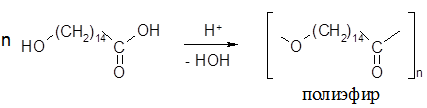
Далее полиэфир подвергают термической деполимеризации с использованием таких катализаторов, как SnO, SnCl2, MgO, алкоголяты щелочных металлов. Образующийся лактон отгоняют из реакционной массы под вакуумом:
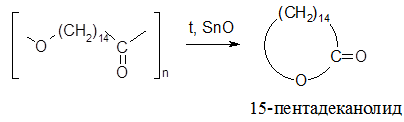
2.1.10 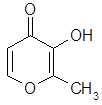 Мальтол, С6Н6О3, МR 126,1– распространенное в природе гетероциклическое соединение с атомом кислорода в шестизвенном цикле, не относящееся к классу лактонов. Бесцветные кристаллы с температурой плавления 164 0С. Благодаря наличию трех гидрофильных функциональных групп мальтол заметно растворим в воде (1,2 %); растворимость в спирте составляет 3,3 %. В углеводородах (неполярных растворителях) мальтол растворим плохо.
Мальтол, С6Н6О3, МR 126,1– распространенное в природе гетероциклическое соединение с атомом кислорода в шестизвенном цикле, не относящееся к классу лактонов. Бесцветные кристаллы с температурой плавления 164 0С. Благодаря наличию трех гидрофильных функциональных групп мальтол заметно растворим в воде (1,2 %); растворимость в спирте составляет 3,3 %. В углеводородах (неполярных растворителях) мальтол растворим плохо.
Обладает фруктово-карамельным запахом.
Широко распространен в природе. Содержится в хвое пихты, сосны, ели; присутствует в корнях цикория, молоке, хлебной корке.
Находит применение в рецептурах пищевых эссенций, парфюмерных композиций, косметических отдушек.
Получают экстракцией игл хвойных деревьев.
Дата добавления: 2015-09-29; просмотров: 8368;
